La adenilato quinasa ( EC 2.7.4.3) (también conocida como ADK o mioquinasa ) es una enzima fosfotransferasa que cataliza la interconversión de los diversos adenosín fosfatos (ATP, ADP y AMP). Al monitorear constantemente los niveles de nucleótidos de fosfato dentro de la célula, ADK desempeña un papel importante en la homeostasis de la energía celular .
La reacción catalizada es:
ATP + AMP ⇔ 2 ADP
La constante de equilibrio varía según la condición, pero es cercana a 1. [1] Por lo tanto, ΔG o para esta reacción es cercana a cero. En el músculo de una variedad de especies de vertebrados e invertebrados, la concentración de ATP suele ser de 7 a 10 veces mayor que la de ADP y, por lo general, mayor de 100 veces mayor que la de AMP . [2] La tasa de fosforilación oxidativa está controlada por la disponibilidad de ADP. Así, la mitocondria intenta mantener altos los niveles de ATP debido a la acción combinada de la adenilato quinasa y los controles de la fosforilación oxidativa .
Hasta la fecha se han identificado nueve isoformas de la proteína ADK humana . Si bien algunos de ellos están omnipresentes en todo el cuerpo, otros se localizan en tejidos específicos. Por ejemplo, ADK7 y ADK8 sólo se encuentran en el citosol de las células; y ADK7 se encuentra en el músculo esquelético, mientras que ADK8 no. [3] No sólo varían las ubicaciones de las diversas isoformas dentro de la célula, sino que la unión del sustrato a la enzima y la cinética de la transferencia de fosforilo también son diferentes. ADK1, la isoenzima ADK citosólica más abundante, tiene una Km aproximadamente mil veces mayor que la Km de ADK7 y 8, lo que indica una unión mucho más débil de ADK1 a AMP. [4] La localización subcelular de las enzimas ADK se realiza incluyendo una secuencia de dirección en la proteína. [3] Cada isoforma también tiene una preferencia diferente por los NTP. Algunos solo usarán ATP, mientras que otros aceptarán GTP, UTP y CTP como transportador de fosforilo.
Algunas de estas isoformas prefieren por completo otras NTP. Existe una GTP:AMP fosfotransferasa mitocondrial, también específica para la fosforilación de AMP, que sólo puede utilizar GTP o ITP como donante de fosforilo. [5] ADK también se ha identificado en diferentes especies bacterianas y en levaduras. [6] Se sabe que otras dos enzimas están relacionadas con la familia ADK, es decir, la uridina monofosfoquinasa de levadura y la quinasa UMP-CMP del moho limoso. Algunos residuos se conservan en estas isoformas, lo que indica cuán esenciales son para la catálisis. Una de las zonas más conservadas incluye un residuo Arg, cuya modificación inactiva la enzima, junto con un Asp que reside en la hendidura catalítica de la enzima y participa en un puente salino.
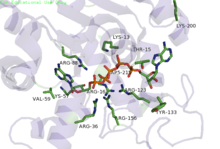
La transferencia de fosforilo sólo se produce al cerrar la "tapa abierta". Esto provoca una exclusión de las moléculas de agua que acerca los sustratos entre sí, [7] reduciendo la barrera energética para el ataque nucleofílico del α-fosforilo del AMP sobre el grupo γ-fosforilo del ATP, lo que resulta en la formación de ADP por transferencia. del grupo γ-fosforilo a AMP. En la estructura cristalina de la enzima ADK de E. coli con el inhibidor Ap5A, el residuo Arg88 se une al Ap5A en el grupo α-fosfato. Se ha demostrado que la mutación R88G produce una pérdida del 99% de la actividad catalítica de esta enzima, lo que sugiere que este residuo está íntimamente involucrado en la transferencia de fosforilo. [8] Otro residuo altamente conservado es Arg119, que se encuentra en la región de unión a adenosina de la ADK y actúa intercalando la adenina en el sitio activo. Se ha sugerido que la promiscuidad de estas enzimas a la hora de aceptar otros NTP se debe a estas interacciones relativamente intrascendentes de la base en la bolsa de unión de ATP. [9] Una red de residuos conservados positivos (Lys13, Arg123, Arg156 y Arg167 en ADK de E. coli ) estabilizan la acumulación de carga negativa en el grupo fosforilo durante la transferencia. Dos residuos de aspartato distales se unen a la red de arginina, lo que hace que la enzima se pliegue y reduzca su flexibilidad. También se requiere un cofactor de magnesio , esencial para aumentar la electrofilia del fosfato en AMP, aunque este ion magnesio sólo se mantiene en la bolsa activa mediante interacciones electrostáticas y se disocia fácilmente. [9]

La flexibilidad y la plasticidad permiten que las proteínas se unan a ligandos , formen oligómeros , se agreguen y realicen trabajo mecánico. [10] Los grandes cambios conformacionales en las proteínas juegan un papel importante en la señalización celular. La adenilato quinasa es una proteína transductora de señales; así, el equilibrio entre conformaciones regula la actividad proteica. ADK tiene un estado desplegado localmente que se despobla al vincularse. [11]

Un estudio de 2007 realizado por Whitford et al. muestra las conformaciones de ADK cuando se une con ATP o AMP. [10] El estudio muestra que hay tres conformaciones o estructuras relevantes de ADK: CORE, Open y Closed. En ADK, hay dos pequeños dominios llamados LID y NMP. [12] El ATP se une en el bolsillo formado por los dominios LID y CORE. AMP se une en el bolsillo formado por los dominios NMP y CORE. El estudio de Whitford también informó hallazgos que muestran que regiones localizadas de una proteína se despliegan durante las transiciones conformacionales. Este mecanismo reduce la tensión y mejora la eficiencia catalítica. El despliegue local es el resultado de energías de deformación competitivas en la proteína. [10]
Se ha demostrado que la estabilidad local (termodinámica) de los dominios de unión al sustrato ATP lid y AMP lid es significativamente menor en comparación con el dominio CORE en ADK E. coli . [13] Además, se ha demostrado que los dos subdominios ( tapa ATP y tapa AMP ) pueden plegarse y desplegarse de una "manera no cooperativa". [13] La unión de los sustratos provoca preferencia por conformaciones "cerradas" entre aquellas que son muestreadas por ADK. Se supone que estas conformaciones "cerradas" ayudan con la eliminación de agua del sitio activo para evitar el desperdicio de hidrólisis de ATP, además de ayudar a optimizar la alineación de los sustratos para la transferencia de fosforilo. [14] Además, se ha demostrado que la apoenzima seguirá muestreando las conformaciones "cerradas" de los dominios de la tapa de ATP y de la tapa de AMP en ausencia de sustratos. [7] Al comparar la velocidad de apertura de la enzima (que permite la liberación del producto) y la velocidad de cierre que acompaña a la unión del sustrato, se encontró que el cierre es el proceso más lento.
La capacidad de una célula para medir dinámicamente los niveles energéticos le proporciona un método para monitorear los procesos metabólicos. [15] Al monitorear y alterar continuamente los niveles de ATP y otros fosfatos de adenilo (niveles de ADP y AMP), la adenilato quinasa es un regulador importante del gasto de energía a nivel celular. [16] A medida que los niveles de energía cambian bajo diferentes tensiones metabólicas, la adenilato quinasa puede generar AMP; que a su vez actúa como molécula de señalización en otras cascadas de señalización. Este AMP generado puede, por ejemplo, estimular varios receptores dependientes de AMP, como los implicados en las vías glucolíticas, los canales K-ATP y la proteína quinasa activada por AMP 5' ( AMPK ). [15] Los factores comunes que influyen en los niveles de nucleótidos de adenina y, por lo tanto, en la actividad de ADK son el ejercicio, el estrés, los cambios en los niveles hormonales y la dieta. [15] Facilita la decodificación de información celular al catalizar el intercambio de nucleótidos en la "zona de detección" íntima de los sensores metabólicos. [15]
La adenilato quinasa está presente en los compartimentos mitocondrial y miofibrilar de la célula y produce dos fosforilos de alta energía (β y γ) de ATP disponibles para ser transferidos entre moléculas de nucleótidos de adenina. [15] [16] En esencia, la adenilato quinasa transporta ATP a sitios de alto consumo de energía y elimina el AMP generado en el transcurso de esas reacciones. Estos retransmisiones secuenciales de fosfotransferencia en última instancia dan como resultado la propagación de los grupos fosforilo a lo largo de conjuntos de moléculas de ADK. [15] Este proceso puede considerarse como una brigada de moléculas ADK que produce cambios en el flujo metabólico intracelular local sin cambios globales aparentes en las concentraciones de metabolitos. [15] Este proceso es extremadamente importante para la homeostasis general de la célula. [15]
La nucleósido difosfato (NDP) quinasa cataliza la síntesis in vivo dependiente de ATP de ribo y desoxirribonucleósido trifosfato. En Escherichia coli mutada que tenía una nucleósido difosfato quinasa alterada , la adenilato quinasa realizaba funciones enzimáticas duales. ADK complementa la deficiencia de nucleósido difosfato quinasa. [17]
La eliminación de AK1 altera la sincronía entre el fosfato inorgánico y el recambio en los sitios consumidores de ATP y los sitios de síntesis de ATP. Esto reduce la comunicación de señales energéticas en el corazón post-isquémico y precipita un reflujo coronario inadecuado después de la isquemia-reperfusión. [18]
La deficiencia de adenilato quinasa 2 ( AK2 ) en humanos causa defectos hematopoyéticos asociados con sordera neurosensorial . [19] La disgenesia reticular es una forma autosómica recesiva de inmunodeficiencia combinada humana . También se caracteriza por una maduración linfoide alterada y una detención temprana de la diferenciación en el linaje mieloide. La deficiencia de AK2 da como resultado una ausencia o una gran disminución en la expresión de proteínas. AK2 se expresa específicamente en la estría vascular del oído interno , lo que indica por qué las personas con una deficiencia de AK2 tendrán sordera neurosensorial. [19]
La ablación genética de AK1 disminuye la tolerancia al estrés metabólico. La deficiencia de AK1 induce una variación específica del tipo de fibra en grupos de transcripciones en la glucólisis y el metabolismo mitocondrial. [20] Esto apoya el metabolismo energético muscular.
"El crecimiento mejorado y el aminoácido fotosintético elevado se asocian con la deficiencia de adenilato quinasa plastidial en Arabidopsis thaliana ". [21]