La versatilidad de la reacción en cadena de la polimerasa (PCR) ha dado lugar a modificaciones del protocolo básico que se utiliza en un gran número de técnicas variantes diseñadas para diversos fines. En este artículo se resumen muchas de las variantes más comunes que se utilizan actualmente o que se utilizaron en el pasado en los laboratorios de biología molecular ; es necesario estar familiarizado con la premisa fundamental por la que funciona la PCR y los términos y conceptos correspondientes para comprender estas técnicas variantes.
A menudo, solo es necesario realizar una pequeña modificación en el protocolo de PCR estándar para lograr el objetivo deseado:
La PCR multiplex utiliza varios pares de cebadores que se unen a diferentes secuencias diana. Esto permite el análisis simultáneo de múltiples dianas en una sola muestra. Por ejemplo, en la prueba de mutaciones genéticas, se pueden combinar seis o más amplificaciones. En el protocolo estándar para la identificación de ADN , las dianas analizadas a menudo se amplifican en grupos de 3 o 4. La amplificación de sonda dependiente de ligación multiplex ( MLPA ) permite amplificar múltiples dianas utilizando solo un par de cebadores, evitando las limitaciones de resolución de la PCR multiplex. La PCR multiplex también se ha utilizado para el análisis de microsatélites y SNP . [1]

La PCR de número variable de repeticiones en tándem (VNTR) se centra en las áreas repetitivas del genoma que presentan variaciones de longitud . El análisis de los genotipos en las muestras generalmente implica la determinación del tamaño de los productos de amplificación mediante electroforesis en gel . El análisis de segmentos VNTR más pequeños, conocidos como repeticiones cortas en tándem (o STR), es la base de las bases de datos de huellas dactilares de ADN como CODIS .
La PCR asimétrica amplifica preferentemente una cadena de un objetivo de ADN bicatenario. Se utiliza en algunos métodos de secuenciación y en el sondeo de hibridación para generar una cadena de ADN como producto. El termociclado se lleva a cabo exactamente como en la PCR convencional, pero con una cantidad limitante o dejando fuera uno de los cebadores. Cuando el cebador limitante se agota, la replicación aumenta aritméticamente en lugar de exponencialmente a través de la extensión del cebador en exceso. [ 2 ] Una modificación de este proceso, denominada PCR lineal - exponencial (o LATE-PCR ), utiliza un cebador limitante con una temperatura de fusión (Tm ) más alta que el cebador en exceso para mantener la eficiencia de la reacción a medida que la concentración del cebador limitante disminuye a mitad de la reacción. [3] Véase también PCR de superposición-extensión .
Se necesitan algunas modificaciones para realizar una PCR larga . El proceso PCR original basado en Klenow no generaba productos que tuvieran más de 400 pb. Sin embargo, la polimerasa Taq puede amplificar dianas de hasta varios miles de pb de longitud. [4] Desde entonces, los protocolos modificados con la enzima Taq han permitido amplificar dianas de más de 50 kb. [5]
La PCR anidada se utiliza para aumentar la especificidad de la amplificación del ADN. Se utilizan dos conjuntos de cebadores en dos reacciones sucesivas. En la primera PCR, se utiliza un par de cebadores para generar productos de ADN, que pueden contener productos amplificados de áreas no diana. Los productos de la primera PCR se utilizan luego como plantilla en una segunda PCR, utilizando uno ("hemi-anidación") o dos cebadores diferentes cuyos sitios de unión se encuentran (anidan) dentro del primer conjunto, lo que aumenta la especificidad. La PCR anidada suele ser más exitosa en la amplificación específica de productos de ADN largos que la PCR convencional, pero requiere un conocimiento más detallado de la secuencia de la diana.
La PCR cuantitativa ( qPCR ) se utiliza para medir la cantidad específica de ADN (o ARN) objetivo en una muestra. Al medir la amplificación solo dentro de la fase de aumento exponencial real, la cantidad de producto medido refleja con mayor precisión la cantidad inicial de objetivo. Se utilizan termocicladores especiales que controlan la cantidad de producto durante la amplificación.
La PCR cuantitativa en tiempo real ( QRT-PCR ), a veces llamada simplemente PCR en tiempo real ( RT-PCR ), se refiere a una colección de métodos que utilizan colorantes fluorescentes, como Sybr Green, o sondas de ADN que contienen fluoróforos , como TaqMan , para medir la cantidad de producto amplificado en tiempo real a medida que avanza la amplificación.
La PCR de inicio en caliente es una técnica que se realiza manualmente calentando los componentes de la reacción a la temperatura de fusión del ADN (por ejemplo, 95 °C) antes de agregar la polimerasa. De esta manera, se evita la amplificación no específica a temperaturas más bajas. [6] Alternativamente, los reactivos especializados inhiben la actividad de la polimerasa a temperatura ambiente, ya sea mediante la unión de un anticuerpo o por la presencia de inhibidores unidos covalentemente que solo se disocian después de un paso de activación a alta temperatura. La PCR de "inicio en caliente/finalización en frío" se logra con nuevas polimerasas híbridas que son inactivas a temperatura ambiente y solo se activan a temperaturas elevadas.
En la PCR de aproximación , la temperatura de hibridación se reduce gradualmente en los ciclos posteriores. La temperatura de hibridación en los primeros ciclos suele ser de 3 a 5 °C superior a la Tm estándar de los cebadores utilizados, mientras que en los ciclos posteriores es una cantidad similar inferior a la Tm . La temperatura de hibridación inicial más alta conduce a una mayor especificidad para la unión de los cebadores, mientras que las temperaturas más bajas permiten una amplificación más eficiente al final de la reacción. [7]
La PCR de ensamblaje (también conocida como ensamblaje cíclico de la polimerasa o PCA ) es la síntesis de estructuras largas de ADN mediante la realización de PCR en un grupo de oligonucleótidos largos con segmentos cortos superpuestos, para ensamblar dos o más fragmentos de ADN en una sola pieza. Implica una PCR inicial con cebadores que tienen una superposición y una segunda PCR que utiliza los productos como plantilla que genera el producto final de longitud completa. Esta técnica puede sustituir al ensamblaje basado en ligadura . [8]
En la PCR de colonias , las colonias bacterianas se examinan directamente mediante PCR, por ejemplo, la detección de construcciones de vectores de ADN correctas . Las colonias se muestrean con una punta de pipeta estéril y una pequeña cantidad de células se transfieren a una mezcla de PCR. Para liberar el ADN de las células, la PCR se inicia con un tiempo extendido a 95 °C (cuando se utiliza la polimerasa estándar), o con un paso de desnaturalización acortado a 100 °C y una polimerasa de ADN quimérica especial. [9]
La reacción en cadena de la polimerasa digital amplifica simultáneamente miles de muestras, cada una en una gota separada dentro de una emulsión o partición dentro de un micropocillo.
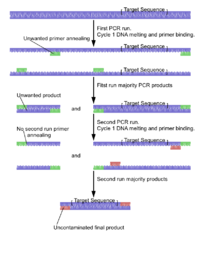
La PCR suicida se utiliza normalmente en paleogenética u otros estudios en los que evitar los falsos positivos y garantizar la especificidad del fragmento amplificado es la máxima prioridad. Se describió originalmente en un estudio para verificar la presencia del microbio Yersinia pestis en muestras dentales obtenidas de tumbas del siglo XIV de personas supuestamente asesinadas por la peste durante la epidemia medieval de la Muerte Negra . [10] El método prescribe el uso de cualquier combinación de cebadores solo una vez en una PCR (de ahí el término "suicidio"), que nunca debería haberse utilizado en ninguna reacción de PCR de control positivo, y los cebadores siempre deben apuntar a una región genómica nunca amplificada antes en el laboratorio utilizando este o cualquier otro conjunto de cebadores. Esto garantiza que no haya ADN contaminante de reacciones de PCR anteriores en el laboratorio, que de lo contrario podría generar falsos positivos.
COLD-PCR ( coamplificación a baja temperatura de desnaturalización -PCR) es un protocolo modificado que enriquece alelos variantes a partir de una mezcla de muestras de ADN de tipo salvaje y que contienen mutaciones.
El proceso básico de PCR a veces puede preceder o seguir a otra técnica.
La RT-PCR (o PCR con transcripción inversa ) se utiliza para transcribir de forma inversa y amplificar el ARN en ADNc . La PCR está precedida por una reacción que utiliza la transcriptasa inversa , una enzima que convierte el ARN en ADNc. Las dos reacciones se pueden combinar en un tubo, y el paso de calentamiento inicial de la PCR se utiliza para inactivar la transcriptasa. [4] La polimerasa Tth (descrita a continuación) tiene actividad RT y puede llevar a cabo toda la reacción. La RT-PCR se utiliza ampliamente en la elaboración de perfiles de expresión , que detecta la expresión de un gen. También se puede utilizar para obtener la secuencia de una transcripción de ARN, lo que puede ayudar a la determinación de los sitios de inicio y terminación de la transcripción (por RACE-PCR ) y facilitar el mapeo de la ubicación de exones e intrones en una secuencia genética.
La PCR de dos colas utiliza un único cebador que se une a un objetivo de microARN con extremos 3' y 5', conocidos como hemisondas. [11] Ambos extremos deben ser complementarios para que se produzca la unión. Luego, el extremo 3' se extiende mediante la transcriptasa inversa formando un ADNc largo. Luego, el ADNc se amplifica utilizando dos cebadores de PCR específicos del objetivo. La combinación de dos hemisondas, ambos dirigidos al objetivo de microARN corto, hace que el ensayo de dos colas sea extremadamente sensible y específico.
La PCR mediada por ligación utiliza pequeños "enlazadores" (o adaptadores) de oligonucleótidos de ADN que primero se ligan a fragmentos del ADN objetivo. Luego, se utilizan cebadores de PCR que se unen a las secuencias de enlace para amplificar los fragmentos objetivo. Este método se utiliza para la secuenciación de ADN, el rastreo genómico y la huella de ADN . [12] Una técnica relacionada es el polimorfismo de longitud de fragmentos amplificados , que genera fragmentos de diagnóstico de un genoma.
La PCR específica de metilación ( MSP ) se utiliza para identificar patrones de metilación del ADN en islas de citosina-guanina (CpG) en el ADN genómico. [13] El ADN diana se trata primero con bisulfito de sodio , que convierte las bases de citosina no metiladas en uracilo , que es complementario a la adenosina en los cebadores de PCR. Luego se llevan a cabo dos amplificaciones en el ADN tratado con bisulfito: un conjunto de cebadores se une al ADN con citosinas (que corresponde a la citosina metilada) y el otro conjunto se une al ADN con uracilo (que corresponde a la citosina no metilada). La MSP utilizada en la PCR cuantitativa proporciona información cuantitativa sobre el estado de metilación de una isla CpG determinada. [14]
Los ajustes de los componentes en PCR se utilizan comúnmente para un rendimiento óptimo.
El ion magnesio divalente (Mg ++ ) es necesario para la actividad de la PCR polimerasa. Concentraciones más bajas de Mg ++ aumentarán la fidelidad de replicación, mientras que concentraciones más altas introducirán más mutaciones. [15]
Los desnaturalizantes (como el DMSO ) pueden aumentar la especificidad de la amplificación al desestabilizar la unión de cebadores no específicos. Otros productos químicos, como el glicerol , son estabilizadores de la actividad de la polimerasa durante la amplificación. Los detergentes (como el Triton X-100 ) pueden evitar que la polimerasa se adhiera a sí misma o a las paredes del tubo de reacción.
Las ADN polimerasas incorporan ocasionalmente bases no coincidentes en la cadena que se extiende. La PCR de alta fidelidad emplea enzimas con actividad exonucleasa 3'-5' que disminuye esta tasa de incorporación incorrecta. Entre los ejemplos de enzimas con actividad de corrección de errores se incluyen Pfu ; los ajustes de las concentraciones de Mg ++ y dNTP pueden ayudar a maximizar la cantidad de productos que coinciden exactamente con el ADN objetivo original. [ cita requerida ]
Los ajustes a los oligonucleótidos sintéticos utilizados como cebadores en PCR son una rica fuente de modificación:
Normalmente, los cebadores de PCR se eligen de una parte invariable del genoma y pueden utilizarse para amplificar un área polimórfica entre ellos. En la PCR específica de alelos se hace lo contrario. Al menos uno de los cebadores se elige de un área polimórfica, con las mutaciones ubicadas en (o cerca de) su extremo 3'. En condiciones estrictas, un cebador no coincidente no iniciará la replicación, mientras que un cebador coincidente sí lo hará. Por lo tanto, la aparición de un producto de amplificación indica el genotipo. (Para obtener más información, consulte Genotipificación de SNP ).
La PCR específica entre secuencias (o ISSR-PCR ) es un método para la identificación de huellas dactilares de ADN que utiliza cebadores seleccionados de segmentos repetidos a lo largo de un genoma para producir una huella dactilar única de longitudes de productos amplificados. [16] El uso de cebadores de un segmento comúnmente repetido se denomina Alu-PCR y puede ayudar a amplificar secuencias adyacentes (o entre) estas repeticiones.
Los cebadores también pueden diseñarse para que sean "degenerados", es decir, capaces de iniciar la replicación desde una gran cantidad de ubicaciones objetivo. La amplificación del genoma completo (o WGA ) es un grupo de procedimientos que permiten que la amplificación se produzca en muchas ubicaciones en un genoma desconocido, y que pueden estar disponibles solo en pequeñas cantidades. Otras técnicas utilizan cebadores degenerados que se sintetizan utilizando múltiples nucleótidos en posiciones particulares (la polimerasa "elige" los cebadores que coinciden correctamente). Además, los cebadores pueden sintetizarse con el análogo de nucleósido inosina , que se hibrida con tres de las cuatro bases normales. Una técnica similar puede obligar a la PCR a realizar mutagénesis dirigida al sitio . (Véase también Reacción en cadena de la polimerasa con extensión por superposición )
Normalmente, los cebadores que se utilizan en la PCR están diseñados para ser totalmente complementarios al objetivo. Sin embargo, la polimerasa es tolerante a los desajustes que se producen más allá del extremo 3'. Los cebadores con cola incluyen secuencias no complementarias en sus extremos 5'. Un procedimiento común es el uso de cebadores enlazadores , que finalmente colocan sitios de restricción en los extremos de los productos de PCR, lo que facilita su inserción posterior en vectores de clonación.
Una extensión del método de "PCR de colonias" (arriba) es el uso de cebadores de vector . Primero se insertan los fragmentos de ADN diana (o ADNc) en un vector de clonación y se diseña un único conjunto de cebadores para las áreas del vector que flanquean el sitio de inserción. La amplificación se produce para cualquier ADN que se haya insertado. [4]
La PCR se puede modificar fácilmente para producir un producto marcado para su posterior uso como sonda de hibridación . Se pueden utilizar uno o ambos cebadores en la PCR con un marcador radiactivo o fluorescente ya adherido, o se pueden añadir marcadores después de la amplificación. Estos métodos de marcado se pueden combinar con la "PCR asimétrica" (arriba) para producir sondas de hibridación eficaces.
La PCR dependiente de la ARNasa H (rhPCR) puede reducir la formación de dímeros de cebadores y aumentar la cantidad de ensayos en la PCR multiplex. El método utiliza cebadores con un bloque escindible en el extremo 3' que se elimina mediante la acción de una enzima ARNasa HII termoestable. [17]
Hay varias ADN polimerasas que se utilizan en PCR.
El fragmento Klenow , derivado de la ADN polimerasa I original de E. coli , fue la primera enzima utilizada en PCR. Debido a su falta de estabilidad a altas temperaturas, es necesario reponerlo durante cada ciclo y, por lo tanto, no se utiliza comúnmente en PCR.
La ADN polimerasa del bacteriófago T4 (familia A) también se utilizó inicialmente en PCR. Tiene una mayor fidelidad de replicación que el fragmento Klenow, pero también se destruye con el calor. La ADN polimerasa T7 (familia B) tiene propiedades y propósitos similares. Se ha aplicado a la mutagénesis dirigida [18] y a la secuenciación de Sanger [19] .
La polimerasa Taq , la ADN polimerasa I de Thermus aquaticus , fue la primera polimerasa termoestable utilizada en PCR y sigue siendo la más utilizada. La enzima se puede aislar de su fuente nativa o de su gen clonado expresado en E. coli . [4] Un fragmento de 61 kDa truncado por carecer de actividad exonucleasa 5'-3' se conoce como fragmento Stoffel y se expresa en E. coli . [20] La falta de actividad exonucleasa puede permitirle amplificar objetivos más largos que la enzima nativa. Se ha comercializado como AmpliTaq y Klentaq . [21] También se ha producido una variante diseñada para PCR de inicio en caliente llamada "polimerasa Faststart". Requiere una fuerte activación por calor, evitando así la amplificación no específica debido a la actividad de la polimerasa a baja temperatura.Se han creado muchas otras variantes . [22]
Otras polimerasas de Thermus , como la polimerasa I Tth ( P52028 ) de Thermus thermophilus , también se han utilizado. La Tth tiene actividad de transcriptasa inversa en presencia de iones Mn 2+ , lo que permite la amplificación por PCR a partir de dianas de ARN. [23]
El género arqueano Pyrococcus ha demostrado ser una rica fuente de polimerasas termoestables con actividad de corrección de pruebas. La ADN polimerasa Pfu , aislada de P. furiosus, muestra una disminución de 5 veces en la tasa de error de replicación en comparación con Taq. [24] Dado que los errores aumentan a medida que progresa la PCR, Pfu es la polimerasa preferida cuando los productos se deben clonar individualmente para secuenciación o expresión. Otras polimerasas menos utilizadas de este género incluyen Pwo ( P61876 ) de Pyrococcus woesei , Pfx de una especie sin nombre, polimerasa "Deep Vent" ( Q51334 ) de la cepa GB-D. [25]
La polimerasa Vent o Tli es una polimerasa de ADN extremadamente termoestable aislada de Thermococcus litoralis . La polimerasa de Thermococcus fumicolans ( Tfu ) también se ha comercializado. [25]
A veces incluso el mecanismo básico de la PCR puede modificarse.

A diferencia de la PCR normal, la PCR inversa permite la amplificación y secuenciación del ADN que rodea una secuencia conocida. Implica someter inicialmente el ADN objetivo a una serie de digestiones con enzimas de restricción y luego circularizar los fragmentos resultantes mediante autoligación . Los cebadores están diseñados para extenderse hacia afuera del segmento conocido, lo que da como resultado la amplificación del resto del círculo. Esto es especialmente útil para identificar secuencias a ambos lados de varios insertos genómicos. [26]
De manera similar, la PCR asimétrica entrelazada térmica (o TAIL-PCR ) se utiliza para aislar secuencias desconocidas que flanquean un área conocida del genoma. Dentro de la secuencia conocida, la TAIL-PCR utiliza un par anidado de cebadores con diferentes temperaturas de hibridación. Se utiliza un cebador "degenerado" para amplificar en la otra dirección desde la secuencia desconocida. [27]
Se han desarrollado algunos protocolos de amplificación de ADN que pueden utilizarse como alternativa a la PCR. Son isotérmicos, es decir, se realizan a una temperatura constante. [28]
La amplificación dependiente de helicasa (HDA) es similar a la PCR tradicional, pero utiliza una temperatura constante en lugar de pasar por etapas de desnaturalización y annealing/extensión. La helicasa de ADN , una enzima que desenrolla el ADN, se utiliza en lugar de la desnaturalización térmica. [29] La amplificación isotérmica mediada por bucle es una idea similar, pero se realiza con una polimerasa que desplaza la cadena. [30]
La reacción de amplificación de enzima de mella (NEAR) y su prima, la amplificación por desplazamiento de cadena (SDA), son isotérmicas y replican el ADN a una temperatura constante utilizando una polimerasa y una enzima de mella. [28]
La amplificación por polimerasa recombinasa (RPA) [31] utiliza una recombinasa para emparejar específicamente los cebadores con el ADN bicatenario en función de la homología, dirigiendo así la síntesis de ADN a partir de secuencias de ADN definidas presentes en la muestra. La presencia de la secuencia diana inicia la amplificación del ADN y no se requiere la fusión térmica o química del ADN. La reacción progresa rápidamente y da como resultado una amplificación específica del ADN a partir de solo unas pocas copias diana hasta niveles detectables, generalmente en 5 a 10 minutos. Todo el sistema de reacción es estable como una formulación seca y no necesita refrigeración. La RPA se puede utilizar para reemplazar la PCR en una variedad de aplicaciones de laboratorio y los usuarios pueden diseñar sus propios ensayos. [32]
Otros tipos de amplificación isotérmica incluyen la amplificación del genoma completo (WGA), la amplificación basada en secuencias de ácidos nucleicos (NASBA) y la amplificación mediada por transcripción (TMA). [28]
{{cite book}}: |journal=ignorado ( ayuda )