Necator americanus es una especie de anquilostoma (un tipo de helminto ) comúnmente conocido como anquilostoma del Nuevo Mundo. Al igual que otros anquilostomas, es un miembro del filo Nematoda . Es un nematodo parásito obligatorio que vive en el intestino delgado de los huéspedes humanos. [1] Necatoriasis —un tipo de helmintiasis— es el término para la condición de ser huésped de una infestación de una especie de Necator . Dado que N. americanus y Ancylostoma duodenale (también conocido como anquilostoma del Viejo Mundo) son las dos especies de anquilostomas que más comúnmente infestan a los humanos, generalmente se las trata bajo el título colectivo de " infección por anquilostomas ". Difieren más obviamente en la distribución geográfica, la estructura de las piezas bucales y el tamaño relativo. [2]
Necator americanus se ha propuesto como alternativa a Trichuris suis en la terapia helmíntica . [3]
Este parásito tiene dos placas cortantes dorsales y dos ventrales alrededor del margen anterior de la cápsula bucal . También tiene un par de dientes subdorsales y un par de dientes subventrales ubicados cerca de la parte posterior. Los machos suelen tener entre 7 y 9 mm de largo, mientras que las hembras miden entre 9 y 11 mm. La vida útil típica de estos parásitos es de 3 a 5 años. Pueden producir entre 5000 y 10 000 huevos por día. [4]
N. americanus se encuentra principalmente en áreas tropicales y templadas. Este parásito prospera en climas más cálidos porque para eclosionar, los huevos requieren un ambiente húmedo, cálido y sombreado. Las cáscaras delgadas y lisas de esta especie hacen que los huevos y los juveniles mueran en temperaturas gélidas o con la desecación del suelo. Por lo tanto, el tipo de suelo donde reside el parásito también es muy importante para sus condiciones ideales de vida. Las condiciones ideales del suelo tienden a darse en áreas donde el agua puede drenar a un ritmo estándar y el tamaño de las partículas del suelo no es ni demasiado grande ni demasiado pequeño. De esa manera, el grado de humedad, así como las aberturas en el suelo, permiten que los parásitos excaven hasta la superficie y se adhieran a la piel de su próximo huésped. Las altas tasas de transmisión parecen ser congruentes con las fuertes lluvias y las temperaturas cálidas que son características de los climas tropicales. Una anomalía de esta especie es que parece preferir huéspedes masculinos a huéspedes femeninos, probablemente debido a la división del trabajo en las regiones de su prevalencia. [5]
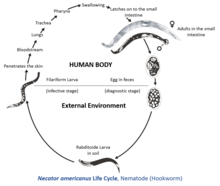
Este gusano comienza como un huevo no embrionado en el suelo. Después de 24 a 48 horas en condiciones favorables, los huevos se embrionan y eclosionan. Esta primera etapa juvenil 1 se conoce como "rabditiforme". Las larvas rabditiformes crecen y mudan en el suelo, transformándose en una etapa juvenil 2. La etapa juvenil 2 muda una vez más hasta alcanzar la etapa juvenil 3, que también se llama "filariforme"; esta es también la forma infecciosa. La transformación de rabditiforme a filariforme suele tardar entre 5 y 10 días. [6] Esta forma larvaria es capaz de penetrar la piel humana, viajar a través de los vasos sanguíneos y el corazón, y llegar a los pulmones. Una vez allí, excava a través de los alvéolos pulmonares y viaja hasta la tráquea , donde es tragada y transportada al intestino delgado. Allí, se adhiere a la pared intestinal, y madura hasta convertirse en un adulto y comienza la reproducción. Los adultos viven en el lumen de la pared intestinal, donde provocan la pérdida de sangre al huésped. Los huevos producidos por los adultos terminan en el suelo después de salir del cuerpo a través de las heces; las hembras de anquilostomas producen hasta 30.000 huevos por día. [7] [8] En promedio, la mayoría de los gusanos adultos se eliminan en 1-2 años. El ciclo de vida de N. americanus solo difiere ligeramente del de A. duodenale . N. americanus no tiene detención del desarrollo en huéspedes inmunes y debe migrar a través de los pulmones.
La patología de N. americanus se divide en dos etapas: larvas y adultos. Las larvas penetran la piel no infectada y viajan a través de varios órganos, incluido el tracto respiratorio y los ganglios linfáticos . Una vez en los ganglios linfáticos, las larvas comienzan a ingresar a la sangre, los pulmones y los intestinos . Algunas larvas no pueden ingresar fácilmente a la dermis y quedan atrapadas en la piel, lo que causa irritación de la piel y larva migratoria cutánea. Otros síntomas incluyen tos excesiva y disnea (falta de aire) durante la migración larvaria. Una vez adherido a la pared intestinal, N. americanus reside y madura hasta convertirse en adultos, penetra en los vasos sanguíneos y succiona sangre. El proceso de incubación de las larvas comienza una vez que ingresan al intestino delgado; por lo tanto, los síntomas pueden no aparecer hasta 40 días después, pero esto varía de persona a persona. [9] La pérdida de sangre de los sitios de unión intestinal puede causar anemia por deficiencia de hierro y pérdida de proteínas. [8] Un individuo de N. americanus puede causar 30 μl de pérdida de sangre por día. [10] La anemia ferropénica puede causar discapacidad intelectual e insuficiencia de crecimiento en los niños. Además, los pacientes infectados sufren dolor abdominal (que se agrava con las comidas) con diarrea, distensión abdominal y náuseas. [11]
En los Estados Unidos, el 95% de los casos de anquilostomas humanos son causados por N. americanus , principalmente en niños en edad escolar en áreas rurales económicamente desfavorecidas. Históricamente, ha habido altas tasas de infección entre los niños en el sur de Estados Unidos. [12] Los juveniles no pueden sobrevivir a temperaturas gélidas, por lo que la prevalencia más alta ocurre en áreas con temperaturas más cálidas y mayor pluviosidad. La mayor incidencia de infecciones ocurre en Asia y África subsahariana, especialmente en áreas afectadas por la pobreza con saneamiento deficiente. [8] Las infecciones por A. duodenale ocurren a una tasa menor y se observan principalmente en Europa y el Mediterráneo. [13]
Se ha secuenciado y analizado un borrador del genoma de Necator americanus . [14] Comprende 244 Mbp con 19.151 genes codificadores de proteínas predichos; estos incluyen genes cuyos productos median la invasión del huésped humano por parte del anquilostoma, genes involucrados en la alimentación sanguínea y el desarrollo, genes que codifican proteínas que representan nuevos objetivos farmacológicos potenciales contra los anquilostomas y familias de genes expandidas que codifican probables proteínas inmunomoduladoras , cuyos productos pueden ser beneficiosos en el tratamiento de enfermedades inflamatorias y asma . [15]
El método más común para diagnosticar N. americanus es mediante la identificación de huevos en una muestra fecal utilizando un microscopio . Los huevos de N. americanus tienen una cáscara fina y forma ovalada, midiendo aproximadamente 56–74 por 36–40 μm. [16]
El tratamiento más común para la infección por N. americanus son los benzimidazoles, específicamente albendazol y mebendazol . Los benzimidazoles matan a los gusanos adultos al unirse a la β-tubulina del nematodo y posteriormente inhibir la polimerización de microtúbulos dentro del parásito. [17] La eficacia de los tratamientos de dosis única para las infecciones por anquilostomas fue: 72% para albendazol, 15% para mebendazol y 31% para pamoato de pirantel. [18] Una preocupación actual con este parásito es el aumento de la resistencia a los medicamentos, como los benzimidazoles y mebendazoles. [19]
Las mujeres embarazadas no deben recibir tratamiento durante el primer trimestre. [9]
Durante la década de 1940, el tratamiento de elección era el tetracloroetileno , [20] administrado en dosis de 3 a 4 cc en ayunas, seguido de 30 a 45 g de sulfato de sodio . Se informó que el tetracloroetileno tenía una tasa de curación del 80 por ciento para las infecciones por Necator, pero del 25 por ciento en las infecciones por Ancylostoma, y a menudo producía una intoxicación leve en el paciente.
La infección y la transmisión a otras personas se pueden prevenir evitando defecar al aire libre o utilizando heces humanas como fertilizante. [21] Este parásito no se transmite directamente de persona a persona. [9] Los cerdos pueden ser un huésped intermediario para N. americanus. [1]
N. americanus causa enfermedades causadas por anquilostomas, que se asocian con pérdida de sangre y anemia. Los pacientes que están infectados con alrededor de 25 a 100 gusanos experimentan síntomas como fatiga, pérdida de peso y dolores de cabeza leves. A medida que el número de infestación alcanza los 100 a 500 gusanos, el paciente experimenta fatiga extrema , deficiencia de hierro y dolor abdominal . Los síntomas empeoran y pueden provocar la muerte cuando la infestación supera los 500 anquilostomas. Los niños y las mujeres embarazadas afectados por N. americanus corren un mayor riesgo debido a la anemia y la mayor necesidad de hierro y proteínas en la dieta. Es alta la demanda de una mejora del saneamiento para reducir la contaminación fecal en regiones con alta prevalencia de infecciones por N. americanus . Las estrategias de control actuales incluyen una combinación de administración masiva de medicamentos para niños de 4 a 6 años de edad para prevenir o eliminar las infecciones por N. americanus . [22]
( N. americanus ) es el anquilostoma nativo de África al sur del Sahara y el único que se encuentra en partes de la India. Ancylostoma y Necator se encuentran juntos en otras partes de la India, en gran parte de China, en el sudeste de Asia, en las islas del sur y suroeste del Pacífico y en partes de Australia. ..., es probable que desaparezcan los límites geográficos entre los dos géneros de anquilostomas humanos.