
La cristalización de proteínas es el proceso de formación de una serie regular de moléculas de proteínas individuales estabilizadas por contactos cristalinos. Si el cristal está suficientemente ordenado, se difractará . Algunas proteínas forman naturalmente matrices cristalinas, como la acuaporina en el cristalino del ojo. [1] [2]
En el proceso de cristalización de proteínas, las proteínas se disuelven en un ambiente acuoso y en una solución de muestra hasta que alcanzan el estado sobresaturado . [3] Se utilizan diferentes métodos para alcanzar ese estado, como difusión de vapor, microbatch, microdiálisis y difusión de interfaz libre. El desarrollo de cristales de proteínas es un proceso difícil influenciado por muchos factores, incluido el pH, la temperatura, la fuerza iónica en la solución de cristalización e incluso la gravedad. [3] Una vez formados, estos cristales se pueden utilizar en biología estructural para estudiar la estructura molecular de la proteína, particularmente para diversos fines industriales o médicos. [4] [5]
Desde hace más de 150 años, científicos de todo el mundo conocen la cristalización de moléculas de proteínas. [6]
En 1840, Friedrich Ludwig Hünefeld descubrió accidentalmente la formación de material cristalino en muestras de sangre de lombriz mantenidas bajo dos portaobjetos de vidrio y ocasionalmente observó pequeños cristales en forma de placas en muestras de sangre humana o porcina desecadas. Estos cristales fueron denominados "hemoglobina" por Felix Hoppe-Seyler en 1864. Los descubrimientos fundamentales de Hünefeld inspiraron a muchos científicos en el futuro. [7]
En 1851, Otto Funke describió el proceso de producción de cristales de hemoglobina humana mediante la dilución de glóbulos rojos con disolventes, como agua pura, alcohol o éter, seguido de una lenta evaporación del disolvente de la solución proteica. En 1871, William T. Preyer, profesor de la Universidad de Jena, publicó un libro titulado Die Blutkrystalle (Los cristales de sangre), en el que revisaba las características de los cristales de hemoglobina de unas 50 especies de mamíferos, aves, reptiles y peces. [7]
En 1909, el fisiólogo Edward T. Reichert publicó junto con el mineralogista Amos P. Brown un tratado sobre la preparación, fisiología y caracterización geométrica de los cristales de hemoglobina de varios cientos de animales, incluidas especies extintas como el lobo de Tasmania. [7] Se encontraron cristales de proteínas en aumento.
En 1934, John Desmond Bernal y su alumna Dorothy Hodgkin descubrieron que los cristales de proteínas rodeados por su licor madre daban mejores patrones de difracción que los cristales secos. Utilizando pepsina , fueron los primeros en discernir el patrón de difracción de una proteína globular húmeda. Antes de Bernal y Hodgkin, la cristalografía de proteínas sólo se había realizado en condiciones secas con resultados inconsistentes y poco confiables. Este es el primer patrón de difracción de rayos X de un cristal de proteína. [8]
En 1958, John Kendrew informó por primera vez sobre la estructura de la mioglobina (una proteína roja que contiene hemo), determinada mediante cristalografía de rayos X. [9] Kendrew compartió el Premio Nobel de Química de 1962 con Max Perutz por este descubrimiento. [4]
Ahora, basándose en los cristales de proteínas, sus estructuras juegan un papel importante en la bioquímica y la medicina traslacional.

La cristalización de proteínas se rige por la misma física que rige la formación de cristales inorgánicos. Para que la cristalización se produzca de forma espontánea, el estado cristalino debe favorecerse termodinámicamente. Esto se describe mediante la energía libre de Gibb (∆G), definida como ∆G = ∆H-T∆S, que captura cómo la energía de un proceso, ∆H, se compensa con el correspondiente cambio de entropía, ∆S. [10] La entropía, a grandes rasgos, describe el desorden de un sistema. Los estados altamente ordenados, como los cristales de proteínas, están desfavorecidos termodinámicamente en comparación con los estados más desordenados, como las soluciones de proteínas en solventes, porque la transición a un estado más ordenado disminuiría la entropía total del sistema (∆S positivo). Para que los cristales se formen espontáneamente, el ∆G de formación de cristales debe ser negativo. En otras palabras, la penalización entrópica debe pagarse mediante una disminución correspondiente en la energía total del sistema (∆H). Los cristales inorgánicos familiares, como el cloruro de sodio, se forman espontáneamente en condiciones ambientales porque el estado del cristal disminuye la energía total del sistema. Sin embargo, la cristalización de algunas proteínas en condiciones ambientales disminuiría la entropía (∆S positivo) y aumentaría la energía total (∆H positivo) del sistema y, por lo tanto, no ocurre espontáneamente. Para lograr la cristalización de tales proteínas, las condiciones se modifican para hacer que la formación de cristales sea energéticamente favorable. Esto suele lograrse mediante la creación de una solución sobresaturada de la muestra. [3]
La formación de cristales requiere dos pasos: nucleación y crecimiento. [3] La nucleación es el paso de iniciación de la cristalización. [3] En la fase de nucleación, las moléculas de proteína en solución se unen como agregados para formar un núcleo sólido estable. [3] A medida que se forma el núcleo, el cristal crece cada vez más gracias a las moléculas que se unen a este núcleo estable. [3] El paso de nucleación es fundamental para la formación de cristales, ya que es la transición de fase de primer orden de las muestras que pasan de tener un alto grado de libertad a obtener un estado ordenado (de acuoso a sólido). [3] Para que el paso de nucleación tenga éxito, la manipulación de los parámetros de cristalización es esencial. El enfoque detrás de lograr que una proteína cristalice es producir una menor solubilidad de la proteína objetivo en solución. [3] Una vez que se excede el límite de solubilidad y hay cristales presentes, se logra la cristalización. [3]
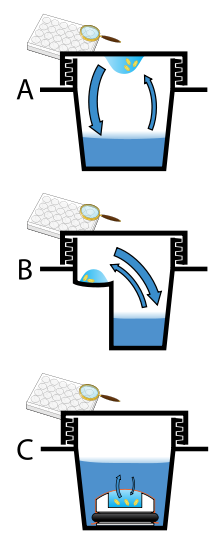
La difusión de vapor es el método más comúnmente empleado para la cristalización de proteínas. En este método, se permite que las gotas que contienen proteína purificada, tampón y precipitante se equilibren con un depósito más grande que contiene tampones y precipitantes similares en concentraciones más altas. Inicialmente, la gota de solución de proteína contiene concentraciones de precipitante y proteína comparativamente bajas, pero a medida que la gota y el depósito se equilibran, las concentraciones de precipitante y proteína aumentan en la gota. Si se utilizan las soluciones de cristalización adecuadas para una proteína determinada, el crecimiento de cristales se produce en la gota. [11] [12] Este método se utiliza porque permite cambios suaves y graduales en la concentración de proteínas y la concentración del precipitante, lo que ayuda al crecimiento de cristales grandes y bien ordenados.
La difusión de vapor se puede realizar en formato de gota colgante o de gota sentada. El aparato de gota colgante implica una gota de solución de proteína colocada sobre un cubreobjetos invertido, que luego se suspende sobre el depósito. El aparato de cristalización de gota sentada coloca la gota sobre un pedestal que está separado del depósito. Ambos métodos requieren sellar el entorno para que pueda producirse el equilibrio entre la gota y el depósito. [11] [13]
Un microlote normalmente implica sumergir un volumen muy pequeño de gotas de proteína en aceite (tan solo 1 µl). La razón por la que se requiere aceite es porque se utiliza un volumen tan bajo de solución de proteína y, por lo tanto, se debe inhibir la evaporación para llevar a cabo el experimento de forma acuosa. Aunque se pueden utilizar varios aceites, los dos agentes selladores más comunes son los aceites de parafina (descritos por Chayen et al.) y los aceites de silicona (descritos por D'Arcy). También existen otros métodos de microdosificación que no utilizan un agente sellador líquido y, en cambio, requieren que un científico coloque rápidamente una película o cinta adhesiva en una placa con pocillos después de colocar la gota en el pocillo.
Además de las cantidades muy limitadas de muestra necesarias, este método también tiene la ventaja adicional de que las muestras están protegidas de la contaminación del aire, ya que nunca quedan expuestas al aire durante el experimento.
La microdiálisis aprovecha una membrana semipermeable, a través de la cual pueden pasar pequeñas moléculas e iones, mientras que las proteínas y los polímeros grandes no pueden cruzar. Al establecer un gradiente de concentración de soluto a través de la membrana y permitir que el sistema progrese hacia el equilibrio, el sistema puede avanzar lentamente hacia la sobresaturación, momento en el cual se pueden formar cristales de proteínas.
La microdiálisis puede producir cristales mediante sal, empleando altas concentraciones de sal u otros compuestos pequeños permeables a la membrana que disminuyen la solubilidad de la proteína. Muy ocasionalmente, algunas proteínas pueden cristalizarse mediante sal por diálisis, dializándolas con agua pura, eliminando solutos, impulsando la autoasociación y la cristalización.
Esta técnica reúne proteínas y soluciones de precipitación sin premezclarlas, sino que las inyecta a través de ambos lados de un canal, permitiendo el equilibrio mediante difusión. Las dos soluciones entran en contacto en una cámara de reactivos, ambas en sus concentraciones máximas, iniciando la nucleación espontánea. A medida que el sistema llega al equilibrio, el nivel de sobresaturación disminuye, favoreciendo el crecimiento de los cristales. [14]
La fuerza impulsora básica para la cristalización de proteínas es optimizar la cantidad de enlaces que uno puede formar con otra proteína a través de interacciones intermoleculares. [3] Estas interacciones dependen de las densidades electrónicas de las moléculas y de las cadenas laterales de las proteínas que cambian en función del pH. [10] La estructura terciaria y cuaternaria de las proteínas está determinada por interacciones intermoleculares entre los grupos laterales de los aminoácidos, en las que los grupos hidrófilos generalmente miran hacia afuera, hacia la solución, para formar una capa de hidratación para el solvente (agua). [10] A medida que cambia el pH, la carga en estos grupos del lado polar también cambia con respecto al pH de la solución y el pKa de la proteína. De ahí que la elección del pH sea fundamental ya sea para favorecer la formación de cristales donde la unión entre las moléculas entre sí es más favorable que con las moléculas de agua. [10] El pH es una de las manipulaciones más poderosas que se pueden asignar para la condición óptima de cristalización.
La temperatura es otro parámetro interesante a discutir, ya que la solubilidad de las proteínas es función de la temperatura. [15] En la cristalización de proteínas, la manipulación de la temperatura para producir cristales exitosos es una estrategia común. A diferencia del pH, la temperatura de los diferentes componentes de los experimentos de cristalografía podría afectar los resultados finales, como la temperatura de la preparación del tampón, [16] la temperatura del experimento de cristalización real, etc.
Los aditivos químicos son pequeños compuestos químicos que se añaden al proceso de cristalización para aumentar el rendimiento de los cristales. [17] El papel de las moléculas pequeñas en la cristalización de proteínas no había sido bien pensado en los primeros días, ya que en la mayoría de los casos se pensaba que eran contaminantes. [17] Las moléculas más pequeñas cristalizan mejor que las macromoléculas como las proteínas, por lo que el uso de aditivos químicos había sido limitado antes del estudio de McPherson. Sin embargo, este es un aspecto poderoso de los parámetros experimentales para la cristalización que es importante que los bioquímicos y cristalógrafos investiguen y apliquen más a fondo. [17]
Existen métodos de alto rendimiento para ayudar a optimizar la gran cantidad de experimentos necesarios para explorar las diversas condiciones necesarias para el crecimiento exitoso de los cristales. Hay numerosos kits comerciales disponibles para ordenar que aplican ingredientes preensamblados en sistemas que garantizan una cristalización exitosa. Al utilizar un kit de este tipo, un científico evita la molestia de purificar una proteína y determinar las condiciones de cristalización adecuadas.
Los robots de manipulación de líquidos se pueden utilizar para configurar y automatizar una gran cantidad de experimentos de cristalización simultáneamente. Lo que de otro modo sería un proceso lento y potencialmente propenso a errores llevado a cabo por un ser humano, se puede lograr de manera eficiente y precisa con un sistema automatizado. Los sistemas de cristalización robóticos utilizan los mismos componentes descritos anteriormente, pero realizan cada paso del procedimiento de forma rápida y con una gran cantidad de réplicas. Cada experimento utiliza pequeñas cantidades de solución, y la ventaja del tamaño más pequeño es doble: los tamaños de muestra más pequeños no solo reducen el gasto de proteína purificada, sino que cantidades más pequeñas de solución conducen a cristalizaciones más rápidas. Cada experimento es monitoreado por una cámara que detecta el crecimiento de cristales. [12]
Las proteínas se pueden diseñar para mejorar las posibilidades de una cristalización exitosa de proteínas mediante el uso de técnicas como la reducción de entropía superficial [19] o la ingeniería en contactos cristalinos. [20] Con frecuencia, los residuos de cisteína problemáticos se pueden reemplazar por alanina para evitar la agregación mediada por disulfuro , y residuos como lisina, glutamato y glutamina se pueden cambiar a alanina para reducir la flexibilidad intrínseca de la proteína, lo que puede dificultar la cristalización.
Las estructuras macromoleculares se pueden determinar a partir de cristales de proteínas utilizando una variedad de métodos, incluida la difracción de rayos X / cristalografía de rayos X , la microscopía electrónica criogénica (CryoEM) (incluida la cristalografía electrónica y la difracción de electrones en microcristales (MicroED) ), la radiografía de ángulo pequeño. dispersión y difracción de neutrones . Véase también Biología estructural .
La cristalización de proteínas también puede ser útil en la formulación de proteínas con fines farmacéuticos. [21]