Las cianinas, también denominadas tetrametilindo(di)-carbocianinas [1] , son una familia de colorantes sintéticos que pertenecen al grupo de las polimetinas . Aunque el nombre deriva etimológicamente de términos para tonos de azul , la familia de las cianinas cubre el espectro electromagnético desde el infrarrojo cercano hasta el ultravioleta .
Químicamente, las cianinas son un sistema conjugado entre dos átomos de nitrógeno ; en cada estructura de resonancia , exactamente un átomo de nitrógeno se oxida a un iminio . Por lo general, forman parte de un sistema heterocíclico nitrogenado . [2]
La principal aplicación de los colorantes de cianina es el marcaje biológico . No obstante, existe una amplia literatura tanto sobre su síntesis como sobre sus usos, siendo las cianinas habituales en algunos soportes de CD y DVD .

Las cianinas se han clasificado de muchas maneras: [3]
Además se reconocen estas clases: [4]
donde dos nitrógenos cuaternarios están unidos por una cadena de polimetino . [5] Ambos nitrógenos pueden ser cada uno independientemente parte de una fracción heteroaromática , como pirrol , imidazol , tiazol , piridina , quinolina , indol , benzotiazol , etc.
Las cianinas se sintetizaron por primera vez hace más de un siglo. Originalmente se utilizaban, y todavía se utilizan, para aumentar el rango de sensibilidad de las emulsiones fotográficas , es decir, para aumentar el rango de longitudes de onda que formarán una imagen en la película, haciendo que la película sea pancromática . [4] Las cianinas también se utilizan en los medios CD-R y DVD-R . Los que se utilizan son en su mayoría de color verde o azul claro, y son químicamente inestables. Por esa razón, los discos de cianina no estabilizados no son adecuados para el uso de CD y DVD de archivo. Los discos de cianina recientes contienen estabilizadores, normalmente un átomo de metal unido a la molécula de cianina, [6] que ralentizan significativamente el deterioro. Estos discos suelen tener una vida útil de archivo de 75 años o más. Los otros colorantes utilizados en los CD-R son la ftalocianina y el azo .
Para aplicaciones en biotecnología, se sintetizan colorantes especiales de cianina a partir de estructuras de 2, 3, 5 o 7-metino con grupos reactivos en uno o ambos extremos de nitrógeno para que puedan unirse químicamente a ácidos nucleicos o moléculas de proteína . El etiquetado se realiza con fines de visualización y cuantificación. Las aplicaciones biológicas incluyen la hibridación genómica comparativa y los chips genéticos , que se utilizan en transcriptómica , y varios estudios en proteómica como la localización de ARN, [7] estudios de interacción molecular por transferencia de energía de resonancia de Förster (FRET) e inmunoensayos fluorescentes .
Los colorantes de cianina están disponibles con diferentes modificaciones, como sustituyentes metilo, etilo o butilo, grupos carboxilo, acetilmetoxi y sulfo que alteran su hidrofilicidad. [8]
Ex (nm): Longitud de onda de excitación en nanómetros
Em (nm): Longitud de onda de emisión en nanómetros
MW: Peso molecular
QY: Rendimiento cuántico
* Depende en gran medida de la viscosidad, la temperatura y las interacciones biomoleculares. [11]
Debido a que producen una fluorescencia más brillante y más estable, las cianinas pueden reemplazar ventajosamente a los colorantes convencionales como la fluoresceína y las rodaminas .
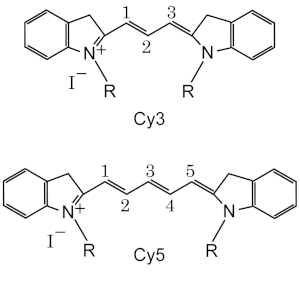
Cy3 fluoresce de color amarillo verdoso (excitación de ~550 nm , emisión de ~570 nm), mientras que Cy5 es fluorescente en la región del rojo lejano (excitación de ~650 nm, emisión de 670 nm). [12] Cy3 puede detectarse mediante varios fluorómetros, generadores de imágenes y microscopios con filtros estándar para tetrametilrodamina (TRITC). Debido a su alto coeficiente de extinción molar , este colorante también se detecta fácilmente a simple vista en geles de electroforesis y en solución. Cy5 se convirtió en un reemplazo popular para los colorantes fluorescentes de rojo lejano debido a su alto coeficiente de extinción (tan pequeño como 1 nanomol puede detectarse en la electroforesis en gel a simple vista) y su máxima emisión de fluoróforo en la región roja, donde muchos detectores CCD tienen máxima sensibilidad y los objetos biológicos dan baja interferencia de fondo.
Los escáneres [ ¿cuáles? ] utilizan en realidad distintas longitudes de onda de emisión láser (normalmente 532 nm y 635 nm ) y longitudes de onda de filtro (550-600 nm y 655-695 nm ) para evitar la contaminación de fondo. De este modo, pueden distinguir fácilmente los colores de Cy3 y Cy5, y también cuantificar la cantidad de marcado de Cy3 y Cy5 en una muestra (detección multiparamétrica). [ cita requerida ]
Cy3.5 puede reemplazar a la sulfoRodamina 101.
Cy5.5 es un colorante que emite fluorescencia en el infrarrojo cercano (IR) (excitación/emisión máxima 678/694 nm).
Cy7 es un fluoruro de infrarrojo cercano que es invisible a simple vista (excitación/emisión máxima 750/776 nm). Se utiliza en aplicaciones de imágenes in vivo , al igual que el colorante Cy7.5.
Los colorantes de sulfocianina tienen uno o dos grupos sulfo, lo que hace que el colorante Cy sea soluble en agua, pero existen formas tri- y cuadrisulfonadas para una solubilidad en agua aún mayor. [8] La PEGilación es otra modificación que confiere hidrofilicidad, no solo al colorante sino también al conjugado marcado.
La nomenclatura Cy3 y Cy5 fue propuesta por primera vez por Ernst, et al. [5] en 1989, y no es estándar ya que no da ninguna pista sobre sus estructuras químicas. En el artículo original, el número designaba el recuento de metinos (como se muestra), y las cadenas laterales no estaban especificadas. Debido a esta ambigüedad, varias estructuras se designan Cy3 y Cy5 en la literatura. Los grupos R no tienen que ser idénticos. En los colorantes que se utilizan, son cadenas alifáticas cortas, una o ambas de las cuales terminan en una fracción altamente reactiva como N-hidroxisuccinimida o maleimida .
Se desarrollaron muchos análogos de los colorantes estándar Cy 2/3/3.5/5/5.5/7/7.5, utilizando diversas modificaciones: colorantes Alexa Fluor , Dylight , colorantes FluoProbes , colorantes Sulfo Cy, [13] colorantes Seta, [14] colorantes IRIS de Cyanine Technologies [15] y otros se pueden usar indistintamente con los colorantes Cy en la mayoría de las aplicaciones bioquímicas, con supuestas mejoras en solubilidad, fluorescencia o fotoestabilidad. [16] [17]
Si bien la protección de patentes para la serie estándar de colorantes Cy ha caducado, la denominación registrada Cy sigue vigente. En consecuencia, ahora se venden colorantes idénticos a los colorantes Cy, pero con nombres diferentes.

Los colorantes de cianina se utilizan para marcar proteínas, anticuerpos, péptidos, sondas de ácidos nucleicos y cualquier otro tipo de biomoléculas que se utilizarán en una variedad de técnicas de detección de fluorescencia: citometría de flujo , microscopía (principalmente el rango visible, pero también UV e IR ), ensayos de microplacas, microarreglos , así como "sondas iluminadas" e imágenes in vivo. [18]
En los experimentos de microarray, el ADN o el ARN se marcan con Cy3 o Cy5, que se han sintetizado para que contengan un grupo reactivo de éster de N-hidroxisuccinimidilo ( éster de NHS ). Dado que los ésteres de NHS reaccionan fácilmente solo con grupos amino alifáticos , de los que carecen los ácidos nucleicos, los nucleótidos deben modificarse con grupos aminoalilo . Esto se hace mediante la incorporación de nucleótidos modificados con aminoalilo durante las reacciones de síntesis. Una buena proporción es una etiqueta cada 60 bases, de modo que las etiquetas no estén demasiado cerca una de otra, lo que daría lugar a efectos de extinción .
Para el etiquetado de proteínas, los colorantes Cy3 y Cy5 a veces llevan un grupo succinimidilo para reaccionar con aminas, o un grupo maleimida para reaccionar con un grupo sulfhidrilo de residuos de cisteína .
Cy5 es sensible a su entorno electrónico. Los cambios en la conformación de la proteína a la que está unida producirán un aumento o una disminución de la emisión. La velocidad de este cambio se puede medir para determinar los parámetros cinéticos de la enzima. Los colorantes se pueden utilizar para fines similares en experimentos FRET.
Cy3 y Cy5 se utilizan en experimentos de proteómica para que las muestras de dos fuentes se puedan mezclar y procesar juntas a través del proceso de separación. [19] [20] Esto elimina las variaciones debidas a las diferentes condiciones experimentales que son inevitables si las muestras se procesaran por separado. Estas variaciones hacen que sea extremadamente difícil, si no imposible, utilizar computadoras para automatizar la adquisición de los datos una vez que se completa la separación. El uso de estos colorantes hace que la automatización sea trivial.
La palabra cianina proviene del vocablo inglés "cyan", que convencionalmente significa un tono de azul verdoso (cercano al "aqua") y se deriva del griego κυάνεος / κυανοῦς kyaneos/kyanous que significa un color algo diferente: "azul oscuro".
{{cite book}}: |journal=ignorado ( ayuda )