En química orgánica , una cicloadición es una reacción química en la que "dos o más moléculas insaturadas (o partes de la misma molécula) se combinan con la formación de un aducto cíclico en el que hay una reducción neta de la multiplicidad del enlace ". La reacción resultante es una reacción de ciclación . Muchas, pero no todas, las cicloadiciones son concertadas y, por tanto, pericíclicas . [1] Las cicloadiciones no concertadas no son pericíclicas. [2] Como clase de reacción de adición , las cicloadiciones permiten la formación de enlaces carbono-carbono sin el uso de un nucleófilo o electrófilo .
Las cicloadiciones se pueden describir utilizando dos sistemas de notación. Una notación más antigua pero aún común se basa en el tamaño de las disposiciones lineales de los átomos en los reactivos. Utiliza paréntesis : ( i + j +…) donde las variables son los números de átomos lineales en cada reactivo. El producto es un ciclo de tamaño ( i + j +…) . En este sistema, la reacción estándar de Diels-Alder es una cicloadición (4 + 2), la cicloadición 1,3-dipolar es una cicloadición (3 + 2) y la ciclopropanación de un carbeno con un alqueno a (2 + 1). -cicloadición. [1]
Una notación más reciente, preferida por la IUPAC, introducida por primera vez por Woodward y Hoffmann , utiliza corchetes para indicar el número de electrones , en lugar de átomos de carbono, involucrados en la formación del producto. En la notación [ i + j + ...], la reacción estándar de Diels-Alder es una cicloadición [4 + 2], mientras que la cicloadición 1,3-dipolar también es una cicloadición [4 + 2]. [1]
Las cicloadiciones térmicas son aquellas cicloadiciones en las que los reactivos se encuentran en el estado electrónico fundamental. Suelen tener (4 n + 2) electrones π participando en el material de partida, para algún número entero n . Estas reacciones ocurren por razones de simetría orbital en un estado suprafacial -suprafacial ( syn / syn estereoquímica) en la mayoría de los casos. También se han informado muy pocos ejemplos de reacciones antarafaciales -antarafaciales ( anti / anti estereoquímica). Hay algunos ejemplos de cicloadición térmica que tienen 4 n electrones π (por ejemplo, la cicloadición [2 + 2]). Estos proceden en un sentido suprafacial-antarafacial ( sin / anti estereoquímica), como las reacciones de cicloadición de derivados de cetena y aleno , en las que el conjunto ortogonal de orbitales p permite que la reacción se desarrolle a través de un estado de transición cruzado , aunque el análisis de estos reacciones como [ π 2 s + π 2 a ] es controvertida. También se ha informado que los alquenos tensos, como los derivados de trans -ciclohepteno, reaccionan de manera antarafacial en reacciones de cicloadición [2 + 2].
Doering (en una comunicación personal con Woodward ) descubrió que el heptafulvaleno y el tetracianoetileno pueden reaccionar en una cicloadición [14 + 2] suprafacial-antarafacial. Este resultado fue posteriormente confirmado y ampliado por Erden y Kaufmann, quienes informaron sobre la cicloadición suprafacial-antarafacial de heptafulvaleno con N -feniltriazolinediona. [3]

Las cicloadiciones en las que participan 4n electrones π también pueden ocurrir mediante activación fotoquímica . Aquí, un componente tiene un electrón promovido del HOMO (enlace π) al LUMO ( antienlace π* ). La simetría orbital es entonces tal que la reacción puede desarrollarse de manera suprafacial-suprafacial. Un ejemplo es la reacción de DeMayo . Otro ejemplo se muestra a continuación, la dimerización fotoquímica del ácido cinámico . [4] Los dos trans alquenos reaccionan de cabeza a cola y los isómeros aislados se denominan ácidos truxílicos .
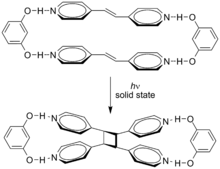
Los efectos supramoleculares pueden influir en estas cicloadiciones. La cicloadición de trans -1,2-bis(4-piridil)eteno está dirigida por resorcinol en estado sólido con un rendimiento del 100% . [5]
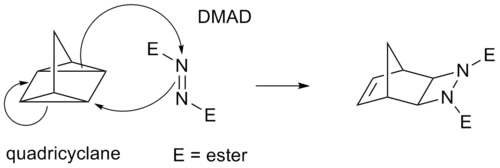
Algunas cicloadiciones en lugar de enlaces π operan a través de anillos de ciclopropano tensos , ya que tienen un carácter π significativo. Por ejemplo, un análogo de la reacción de Diels-Alder es la reacción cuadriciclano - DMAD :
En la notación de cicloadición (i+j+...), i y j se refieren al número de átomos involucrados en la cicloadición. En esta notación, una reacción de Diels-Alder es una cicloadición (4+2) y una adición 1,3-dipolar, como el primer paso en la ozonólisis, es una cicloadición (3+2). Sin embargo, la notación preferida de la IUPAC , con [i+j+...], tiene en cuenta los electrones y no los átomos. En esta notación, la reacción DA y la reacción dipolar se convierten ambas en una cicloadición [4+2]. La reacción entre norbornadieno y un alquino activado es una cicloadición [2+2+2].
La reacción de Diels-Alder es quizás la reacción de cicloadición más importante y comúnmente enseñada. Formalmente es una reacción de cicloadición [4+2] y existe en una amplia gama de formas, incluida la reacción inversa de Diels-Alder con demanda de electrones , la reacción de hexadehidro Diels-Alder y la trimerización de alquinos relacionada . La reacción también se puede realizar a la inversa en la reacción retro-Diels-Alder .
Se conocen reacciones que involucran heteroátomos; incluidas las reacciones aza-Diels-Alder e Imine Diels-Alder .
La reacción de cicloadición de Huisgen es una cicloadición (2+3).
La cicloadición de nitrona-olefina es una cicloadición (3+2).
Las reacciones queletrópicas son una subclase de cicloadiciones. La característica distintiva clave de las reacciones queletrópicas es que en uno de los reactivos, ambos enlaces nuevos se forman con el mismo átomo. El ejemplo clásico es la reacción del dióxido de azufre con un dieno .
Existen otras reacciones de cicloadición: [4+3]cicloadiciones , [6+4]cicloadiciones , [2+2]fotocicloadiciones , cicloadición centrada en metales y [4+4]fotocicloadiciones.
Las cicloadiciones a menudo tienen análogos radicales catalizados por metales y escalonados ; sin embargo, estas no son reacciones pericíclicas estrictamente hablando. Cuando en una cicloadición están involucrados intermedios cargados o radicales o cuando el resultado de la cicloadición se obtiene en una serie de pasos de reacción, a veces se les llama cicloadiciones formales para hacer la distinción con las verdaderas cicloadiciones pericíclicas.
Un ejemplo de una cicloadición formal [3+3] entre una enona cíclica y una enamina catalizada por n -butillitio es una reacción en cascada de enamina Stork / adición 1,2 : [6]
![Una cicloadición formal intermolecular [3+3] entre un cloruro de iminio cíclico y ciclopentenona.](http://upload.wikimedia.org/wikipedia/commons/thumb/5/53/3%2B3_cycloaddition_-_cyclic_iminium_to_cyclic_enone.svg/500px-3%2B3_cycloaddition_-_cyclic_iminium_to_cyclic_enone.svg.png)
Los catalizadores de diiminopiridina de hierro contienen un ligando activo redox en el que el átomo de hierro central puede coordinarse con dos dobles enlaces de olefina simples no funcionalizados. El catalizador se puede escribir como una resonancia entre una estructura que contiene electrones desapareados con el átomo de hierro central en el estado de oxidación II y una en la que el hierro se encuentra en el estado de oxidación 0. Esto le da la flexibilidad para unirse a los dobles enlaces a medida que se someten a una reacción de ciclación, generando una estructura de ciclobutano mediante eliminación reductora de CC; alternativamente, se puede producir una estructura de ciclobuteno mediante eliminación de beta-hidrógeno. La eficiencia de la reacción varía sustancialmente dependiendo de los alquenos utilizados, pero el diseño racional del ligando puede permitir la expansión de la gama de reacciones que pueden catalizarse. [7] [8]