Una ecuación química es la representación simbólica de una reacción química en forma de símbolos y fórmulas químicas . Las entidades reactivas se dan en el lado izquierdo y las entidades producto están en el lado derecho con un signo más entre las entidades tanto en los reactivos como en los productos, y una flecha que apunta hacia los productos para mostrar la dirección de la reacción. [1] Las fórmulas químicas pueden ser simbólicas, estructurales (diagramas pictóricos) o entremezcladas. Los coeficientes junto a los símbolos y fórmulas de entidades son los valores absolutos de los números estequiométricos. La primera ecuación química fue diagramada por Jean Beguin en 1615. [2]
Una ecuación química (ver un ejemplo a continuación) consta de una lista de reactivos (las sustancias iniciales) en el lado izquierdo, un símbolo de flecha y una lista de productos (sustancias formadas en la reacción química) en el lado derecho. . Cada sustancia se especifica por su fórmula química , precedida opcionalmente por un número llamado coeficiente estequiométrico . [a] El coeficiente especifica cuántas entidades (por ejemplo, moléculas ) de esa sustancia están involucradas en la reacción a nivel molecular. Si no se escribe explícitamente, el coeficiente es igual a 1. Varias sustancias en cualquier lado de la ecuación están separadas entre sí por un signo más .
Como ejemplo, la ecuación para la reacción del ácido clorhídrico con sodio se puede denotar:
Dado que las fórmulas son bastante simples, esta ecuación podría leerse como "dos HCL más dos NA producen [b] dos NACL y H dos". Alternativamente, y en general para ecuaciones que involucran sustancias químicas complejas, las fórmulas químicas se leen usando la nomenclatura IUPAC , que podría verbalizar esta ecuación como "dos moléculas de ácido clorhídrico y dos átomos de sodio reaccionan para formar dos unidades fórmula de cloruro de sodio y una molécula de gas hidrógeno ". "
Se utilizan diferentes variantes del símbolo de la flecha para indicar el tipo de reacción: [1]
Para indicar el estado físico de una sustancia química, se puede agregar un símbolo entre paréntesis a su fórmula: (s) para un sólido, (l) para un líquido, (g) para un gas y (aq) para una solución acuosa . Esto se hace especialmente cuando se desea enfatizar los estados o cambios de los mismos. Por ejemplo, la reacción del ácido clorhídrico acuoso con sodio sólido (metálico) para formar cloruro de sodio acuoso y gas hidrógeno se escribiría así:
Esa reacción tendría propiedades termodinámicas y cinéticas diferentes si el cloruro de hidrógeno gaseoso reemplazara al ácido clorhídrico como reactivo:
Alternativamente, en algunos casos se utiliza una flecha sin paréntesis para indicar la formación de un gas ↑ o precipitado ↓. Esto es especialmente útil si sólo se forma una de esas especies. A continuación se muestra un ejemplo que indica que se forma gas hidrógeno:
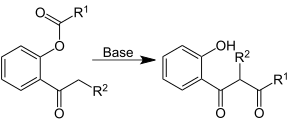
Si la reacción requiere energía, se indica encima de la flecha. Se coloca una letra griega mayúscula delta (Δ) o un triángulo (△) [e] en la flecha de reacción para mostrar que se agrega energía en forma de calor a la reacción. La expresión hν [f] se utiliza como símbolo de la adición de energía en forma de luz. Se utilizan otros símbolos para otros tipos específicos de energía o radiación.
De manera similar, si una reacción requiere un medio determinado con ciertas características específicas, entonces el nombre del ácido o base que se utiliza como medio se puede colocar encima de la flecha. Si no se requiere ningún ácido o base específico, otra forma de indicar el uso de un medio ácido o básico es escribir H + u OH − (o incluso "ácido" o "base") encima de la flecha. Del mismo modo podrán indicarse las condiciones específicas de temperatura y presión, así como la presencia de catalizadores.

La notación estándar para ecuaciones químicas solo permite que todos los reactivos estén en un lado, todos los productos en el otro y todos los coeficientes estequiométricos sean positivos. Por ejemplo, la forma habitual de la ecuación para la deshidratación de metanol a dimetiléter es:
A veces se utiliza una extensión, donde algunas sustancias con sus coeficientes estequiométricos se mueven por encima o por debajo de la flecha, precedidas por un signo más o nada para un reactivo, y por un signo menos para un producto. Entonces la misma ecuación puede verse así:
Esta notación sirve para ocultar sustancias menos importantes de los lados de la ecuación, hacer más obvio el tipo de reacción en cuestión y facilitar el encadenamiento de ecuaciones químicas. Esto es muy útil para ilustrar mecanismos de reacción de varios pasos . Tenga en cuenta que las sustancias encima o debajo de las flechas no son catalizadores en este caso, porque se consumen o se producen en la reacción como reactivos o productos ordinarios.
Otra extensión utilizada en los mecanismos de reacción mueve algunas sustancias a las ramas de la flecha. Ambas extensiones se utilizan en la ilustración de ejemplo de un mecanismo.
El uso de coeficientes estequiométricos negativos en ambos lados de la ecuación (como en el ejemplo siguiente) no se adopta ampliamente y, a menudo, se desaconseja. [5] [ se necesita una mejor fuente ]
Debido a que en una reacción química no tienen lugar reacciones nucleares , los elementos químicos pasan a través de la reacción sin cambios. Así, cada lado de la ecuación química debe representar el mismo número de átomos de cualquier elemento concreto (o nucleido , si se tienen en cuenta diferentes isótopos ). Lo mismo ocurre con la carga eléctrica total , tal como lo establece la ley de conservación de la carga . Una ecuación que cumple estos requisitos se dice que está equilibrada .
Una ecuación química se equilibra asignando valores adecuados a los coeficientes estequiométricos. Las ecuaciones simples se pueden equilibrar mediante inspección, es decir, mediante prueba y error. Otra técnica consiste en resolver un sistema de ecuaciones lineales .
Las ecuaciones balanceadas generalmente se escriben con los coeficientes de números naturales más pequeños . Sin embargo, a veces puede resultar ventajoso aceptar un coeficiente fraccionario, si simplifica los demás coeficientes. Por tanto, el ejemplo introductorio puede reescribirse como
En algunas circunstancias, los coeficientes fraccionarios son incluso inevitables. Por ejemplo, la reacción correspondiente a la entalpía estándar de formación debe escribirse de manera que se forme una molécula de un solo producto. Esto a menudo requerirá que algunos coeficientes de los reactivos sean fraccionarios, como es el caso de la formación de fluoruro de litio :

El método de inspección se puede resumir en establecer el coeficiente estequiométrico de la sustancia más compleja en 1 y asignar valores a otros coeficientes paso a paso, de modo que ambos lados de la ecuación terminen con el mismo número de átomos para cada elemento. Si surge algún coeficiente fraccionario durante este proceso, la presencia de fracciones puede eliminarse (en cualquier momento) multiplicando todos los coeficientes por su mínimo común denominador .
Balanceo de la ecuación química para la combustión completa del metano.
se logra de la siguiente manera:
Para cada elemento químico (o nucleido o resto o carga inalterada) i , su requisito de conservación se puede expresar mediante la ecuación matemática
dónde
Esto da como resultado un sistema homogéneo de ecuaciones lineales , que se resuelven fácilmente mediante métodos matemáticos. Dicho sistema siempre tiene la solución trivial de todos ceros , que no nos interesa, pero si hay soluciones adicionales, habrá un número infinito de ellas. Cualquier solución no trivial equilibrará la ecuación química. Una solución "preferida" es aquella con coeficientes estequiométricos s j de números enteros , en su mayoría positivos [g], con el máximo común divisor igual a uno.
Asignemos variables a los coeficientes estequiométricos de la ecuación química del apartado anterior y escribamos las ecuaciones lineales correspondientes:
Todas las soluciones de este sistema de ecuaciones lineales son de la siguiente forma, donde r es cualquier número real :
La elección de r = 1 produce la solución preferida,
que corresponde a la ecuación química balanceada:
El sistema de ecuaciones lineales presentado en la sección anterior también se puede escribir utilizando un formalismo matricial eficiente . Primero, para unificar los coeficientes estequiométricos del reactivo y del producto s j , introduzcamos la cantidad
llamado número estequiométrico , [h] que simplifica las ecuaciones lineales a
donde J es el número total de sustancias reaccionantes y producto (fórmulas) en la ecuación química.
Ubicación de los valores a ij en la fila i y la columna j de la matriz de composición
y disposición de los números estequiométricos en el vector estequiométrico
permite expresar el sistema de ecuaciones como una única ecuación matricial :
Como anteriormente, cualquier vector estequiométrico distinto de cero ν , que resuelva la ecuación matricial, equilibrará la ecuación química.
El conjunto de soluciones de la ecuación matricial es un espacio lineal llamado núcleo de la matriz A. Para que este espacio contenga vectores distintos de cero ν , es decir, que tenga una dimensión positiva J N , las columnas de la matriz de composición A no deben ser linealmente independientes . El problema de equilibrar una ecuación química se convierte entonces en el problema de determinar el núcleo J N -dimensional de la matriz de composición. Es importante señalar que sólo para J N = 1 habrá una única solución preferida al problema de equilibrio. Para J N > 1 habrá un número infinito de soluciones preferidas, siendo J N de ellas linealmente independientes. Si J N = 0, sólo existirá la solución trivial inutilizable, el vector cero.
Se han desarrollado técnicas [6] [7] para calcular rápidamente un conjunto de J N soluciones independientes al problema de equilibrio, que son superiores al método algebraico y de inspección [ cita necesaria ] porque son determinantes y producen todas las soluciones al equilibrio. problema.
Usando nuevamente la misma ecuación química, escriba la ecuación matricial correspondiente:
Sus soluciones son de la siguiente forma, donde r es cualquier número real:
La elección de r = 1 y un cambio de signo de las dos primeras filas produce la solución preferida al problema de equilibrio:
Una ecuación iónica es una ecuación química en la que los electrolitos se escriben como iones disociados . Las ecuaciones iónicas se utilizan para reacciones de desplazamiento simple y doble que ocurren en soluciones acuosas .
Por ejemplo, en la siguiente reacción de precipitación:
la ecuación iónica completa es:
o, con todos los estados físicos incluidos:
En esta reacción, los iones Ca 2+ y NO 3 − permanecen en solución y no son parte de la reacción. Es decir, estos iones son idénticos tanto en el lado reactivo como en el lado producto de la ecuación química. Como estos iones no participan en la reacción, se denominan iones espectadores . Una ecuación iónica neta es la ecuación iónica completa de la cual se han eliminado los iones espectadores. [8] La ecuación iónica neta de las reacciones anteriores es:
o, en forma equilibrada reducida ,
En una neutralización o reacción ácido / base , la ecuación iónica neta normalmente será:
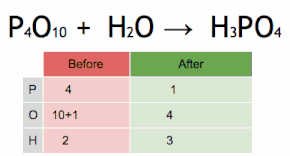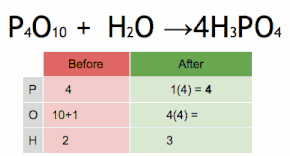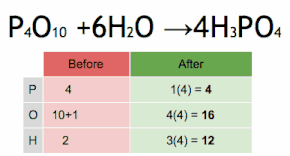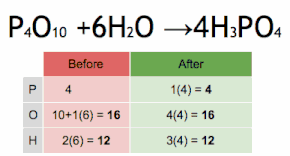
Hay algunas reacciones ácido/base que producen un precipitado además de la molécula de agua que se muestra arriba. Un ejemplo es la reacción del hidróxido de bario con ácido fosfórico , que produce no solo agua sino también la sal insoluble de fosfato de bario. En esta reacción, no hay iones espectadores, por lo que la ecuación iónica neta es la misma que la ecuación iónica completa.
Las reacciones de doble desplazamiento en las que un carbonato reacciona con un ácido tienen la ecuación iónica neta:
Si cada ion es un "ion espectador", entonces no hubo reacción y la ecuación iónica neta es nula.
Generalmente, si z j es el múltiplo de la carga elemental en la j-ésima molécula, la neutralidad de la carga se puede escribir como:
donde los ν j son los coeficientes estequiométricos descritos anteriormente. El z j puede incorporarse [6] [7] como una fila adicional en la matriz a ij descrita anteriormente, y una ecuación iónica adecuadamente equilibrada también obedecerá:
Ahora el Sr. Pfaundler ha unido estos dos fenómenos en un solo concepto al considerar el límite observado como el resultado de dos reacciones opuestas, conduciendo la del ejemplo citado a la formación de sal marina [es decir, NaCl] y ácido nítrico, [y ] el otro al ácido clorhídrico y al nitrato de sodio. Esta consideración, que la experiencia valida, justifica la expresión "equilibrio químico", que se utiliza para caracterizar el estado final de reacciones limitadas. Propondría traducir esta expresión por el siguiente símbolo:
- HCl + NO 3 Na ⇄ NO 3 H + Cl Na.
Por lo tanto, reemplazo, en este caso, el signo = en la ecuación química por el signo ⇄, que en realidad no expresa sólo igualdad sino que también muestra la dirección de la reacción. Esto expresa claramente que una acción química ocurre simultáneamente en dos direcciones opuestas.
O M. Pfaundler a relié ces deux phénomênes... s'accomplit en même temps dans deux sens opposés.