El carburo de boro (fórmula química aproximadamente B 4 C) es una cerámica de boro - carbono extremadamente dura , un material covalente utilizado en armaduras de tanques , chalecos antibalas , pólvoras de sabotaje de motores, [2] así como en numerosas aplicaciones industriales. Con una dureza Vickers de >30 GPa, es uno de los materiales más duros conocidos, detrás del nitruro de boro cúbico y el diamante . [3]
El carburo de boro se descubrió en el siglo XIX como subproducto de reacciones que involucraban boruros metálicos, pero se desconocía su fórmula química . No fue hasta la década de 1930 que la composición química se estimó en B 4 C. [4] Permaneció la controversia sobre si el material tenía o no esta estequiometría exacta de 4:1 , ya que, en la práctica, el material siempre tiene una ligera deficiencia de carbono con Respecto a esta fórmula, la cristalografía de rayos X muestra que su estructura es muy compleja, con una mezcla de cadenas CBC e icosaedros B 12 .
Estas características iban en contra de una fórmula empírica B 4 C exacta y muy simple. [5] Debido a la unidad estructural B 12 , la fórmula química del carburo de boro "ideal" a menudo no se escribe como B 4 C, sino como B 12 C 3 , y la deficiencia de carbono del carburo de boro se describe en términos de una combinación de las unidades B 12 C 3 y B 12 CBC.
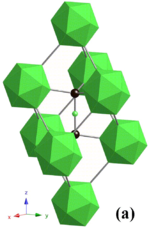

El carburo de boro tiene una estructura cristalina compleja típica de los boruros a base de icosaedros . Allí, los icosaedros B 12 forman una unidad de red romboédrica (grupo espacial: R 3 m (No. 166), constantes de red: a = 0,56 nm y c = 1,212 nm) que rodea una cadena CBC que reside en el centro de la celda unitaria . y ambos átomos de carbono forman un puente entre los tres icosaedros vecinos. Esta estructura está en capas: los icosaedros B 12 y los carbonos puente forman un plano de red que se extiende paralelo al plano c y se apila a lo largo del eje c . La red tiene dos unidades estructurales básicas: el icosaedro B 12 y el octaedro B 6 . Debido al pequeño tamaño de los octaedros B 6 , no pueden interconectarse. En cambio, se unen al icosaedro B 12 en la capa vecina, y esto disminuye la fuerza de unión en el plano c . [6]
Debido a la unidad estructural B 12 , la fórmula química del carburo de boro "ideal" a menudo no se escribe como B 4 C, sino como B 12 C 3 , y la deficiencia de carbono del carburo de boro se describe en términos de una combinación de B 12 C 3 y B 12 C 2 unidades. [5] [7] Algunos estudios indican la posibilidad de incorporación de uno o más átomos de carbono al icosaedro de boro, dando lugar a fórmulas como (B 11 C)CBC = B 4 C en el extremo de la estequiometría con mayor contenido de carbono, pero fórmulas como B 12 (CBB) = B 14 C en el extremo rico en boro. Por tanto, el "carburo de boro" no es un compuesto único, sino una familia de compuestos de diferentes composiciones. Un intermedio común, que se aproxima a una proporción de elementos comúnmente encontrada, es B 12 (CBC) = B 6,5 C. [8] Los cálculos de la mecánica cuántica han demostrado que el desorden configuracional entre los átomos de boro y de carbono en las diferentes posiciones del cristal determina varios de las propiedades de los materiales, en particular, la simetría cristalina de la composición B 4 C [9] y el carácter eléctrico no metálico de la composición B 13 C 2 . [10]
El carburo de boro se conoce como un material robusto que tiene una dureza extremadamente alta (entre 9,5 y 9,75 en la escala de dureza de Mohs ), una sección transversal alta para la absorción de neutrones (es decir, buenas propiedades de protección contra neutrones), estabilidad a la radiación ionizante y a la mayoría de los productos químicos. [11] Su dureza Vickers (38 GPa), módulo elástico (460 GPa) [12] y tenacidad a la fractura (3,5 MPa·m 1/2 ) se aproximan a los valores correspondientes al diamante (1150 GPa y 5,3 MPa·m 1/2 ). . [13]
En 2015 [actualizar], el carburo de boro es la tercera sustancia más dura conocida, después del diamante y el nitruro de boro cúbico , lo que le valió el sobrenombre de "diamante negro". [14] [15]
El carburo de boro es un semiconductor , con propiedades electrónicas dominadas por el transporte de tipo salto. [8] La banda prohibida de energía depende de la composición y del grado de orden. La banda prohibida se estima en 2,09 eV, con múltiples estados de banda prohibida media que complican el espectro de fotoluminiscencia . [8] El material suele ser de tipo p.
El carburo de boro fue sintetizado por primera vez por Henri Moissan en 1899, [7] mediante la reducción de trióxido de boro con carbono o magnesio en presencia de carbono en un horno de arco eléctrico . En el caso del carbono, la reacción se produce a temperaturas superiores al punto de fusión de B 4 C y va acompañada de la liberación de una gran cantidad de monóxido de carbono : [16]
Si se utiliza magnesio, la reacción se puede llevar a cabo en un crisol de grafito y los subproductos de magnesio se eliminan mediante tratamiento con ácido. [17]


Por su dureza:
Para otras propiedades:
La capacidad del carburo de boro para absorber neutrones sin formar radionucleidos de larga duración lo hace atractivo como absorbente de la radiación de neutrones que surge en las centrales nucleares [18] y en las bombas de neutrones antipersonal . Las aplicaciones nucleares del carburo de boro incluyen el blindaje. [11]
... el carburo de boro es el tercer material más duro del planeta.