El carburo de boro (fórmula química aproximada B 4 C) es una cerámica de boro - carbono extremadamente dura , un material covalente utilizado en blindaje de tanques , chalecos antibalas , polvos antisabotaje de motores , [2] así como en numerosas aplicaciones industriales. Con una dureza Vickers de >30 GPa, es uno de los materiales más duros conocidos, detrás del nitruro de boro cúbico y el diamante . [3]
El carburo de boro fue descubierto en el siglo XIX como un subproducto de reacciones que involucraban boruros metálicos, pero su fórmula química era desconocida. No fue hasta la década de 1930 que la composición química se estimó como B 4 C. [4] La controversia permaneció en cuanto a si el material tenía o no esta estequiometría exacta de 4:1 , ya que, en la práctica, el material siempre es ligeramente deficiente en carbono con respecto a esta fórmula, y la cristalografía de rayos X muestra que su estructura es altamente compleja, con una mezcla de cadenas CBC e icosaedros B 12 .
Estas características contradecían una fórmula empírica B 4 C muy simple y exacta. [5] Debido a la unidad estructural B 12 , la fórmula química del carburo de boro "ideal" a menudo no se escribe como B 4 C, sino como B 12 C 3 , y la deficiencia de carbono del carburo de boro se describe en términos de una combinación de las unidades B 12 C 3 y B 12 CBC.
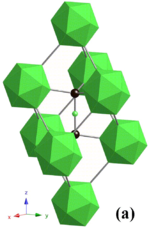

El carburo de boro tiene una estructura cristalina compleja típica de los boruros basados en icosaedros . Allí, los icosaedros B 12 forman una unidad reticular romboédrica (grupo espacial: R 3 m (n.º 166), constantes reticulares: a = 0,56 nm y c = 1,212 nm) que rodea una cadena CBC que reside en el centro de la celda unitaria , y ambos átomos de carbono forman un puente entre los tres icosaedros vecinos. Esta estructura está en capas: los icosaedros B 12 y los carbonos puente forman un plano de red que se extiende paralelo al plano c y se apila a lo largo del eje c . La red tiene dos unidades estructurales básicas: el icosaedro B 12 y el octaedro B 6. Debido al pequeño tamaño de los octaedros B 6 , no pueden interconectarse. En cambio, se unen a los icosaedros B 12 en la capa vecina, y esto disminuye la fuerza de enlace en el plano c . [6]
Debido a la unidad estructural B 12 , la fórmula química del carburo de boro "ideal" a menudo no se escribe como B 4 C, sino como B 12 C 3 , y la deficiencia de carbono del carburo de boro se describe en términos de una combinación de las unidades B 12 C 3 y B 12 C 2 . [5] [7] Algunos estudios indican la posibilidad de incorporación de uno o más átomos de carbono en los icosaedros de boro, dando lugar a fórmulas como (B 11 C)CBC = B 4 C en el extremo pesado en carbono de la estequiometría, pero fórmulas como B 12 (CBB) = B 14 C en el extremo rico en boro. El "carburo de boro" no es, por tanto, un compuesto único, sino una familia de compuestos de diferentes composiciones. Un intermedio común, que se aproxima a una proporción de elementos comúnmente encontrada, es B 12 (CBC) = B 6.5 C. [8] Los cálculos mecánicos cuánticos han demostrado que el desorden configuracional entre los átomos de boro y carbono en las diferentes posiciones en el cristal determina varias de las propiedades de los materiales, en particular, la simetría cristalina de la composición B 4 C [9] y el carácter eléctrico no metálico de la composición B 13 C 2. [10]
El carburo de boro es conocido como un material robusto que tiene una dureza extremadamente alta (aproximadamente 9,5 hasta 9,75 en la escala de dureza de Mohs ), una sección transversal alta para la absorción de neutrones (es decir, buenas propiedades de protección contra neutrones), estabilidad a la radiación ionizante y la mayoría de los productos químicos. [11] Su dureza Vickers (38 GPa), módulo elástico (460 GPa) [12] y tenacidad a la fractura (3,5 MPa·m 1/2 ) se aproximan a los valores correspondientes al diamante (1150 GPa y 5,3 MPa·m 1/2 ). [13]
A partir de 2015 [actualizar], el carburo de boro es la tercera sustancia más dura conocida, después del diamante y el nitruro de boro cúbico , lo que le valió el apodo de "diamante negro". [14] [15]
El carburo de boro es un semiconductor con propiedades electrónicas dominadas por el transporte de tipo salto. [8] La brecha de banda de energía depende de la composición, así como del grado de orden. La brecha de banda se estima en 2,09 eV, con múltiples estados de brecha de banda media que complican el espectro de fotoluminiscencia . [8] El material es típicamente de tipo p.
El carburo de boro fue sintetizado por primera vez por Henri Moissan en 1899, [7] mediante la reducción de trióxido de boro con carbono o magnesio en presencia de carbono en un horno de arco eléctrico . En el caso del carbono, la reacción se produce a temperaturas superiores al punto de fusión de B 4 C y va acompañada de la liberación de una gran cantidad de monóxido de carbono : [16]
Si se utiliza magnesio, la reacción se puede llevar a cabo en un crisol de grafito y los subproductos de magnesio se eliminan mediante tratamiento con ácido. [17]


La excepcional dureza del boro se puede utilizar para las siguientes aplicaciones:
Otras propiedades del carburo de boro también lo hacen adecuado para:
La capacidad del carburo de boro para absorber neutrones sin formar radionucleidos de larga duración lo hace atractivo como absorbente de la radiación neutrónica que surge en las centrales nucleares [18] y de las bombas de neutrones antipersonal . Las aplicaciones nucleares del carburo de boro incluyen el blindaje. [11]
Los filamentos de carburo de boro presentan perspectivas auspiciosas como elementos de refuerzo en compuestos de resina y metal, atribuidos a su excepcional resistencia, módulo elástico y características de baja densidad. [19] Además, los filamentos de carburo de boro no se ven afectados por la radiación debido a su capacidad para absorber neutrones. [20] Es menos dañino que los filamentos hechos de otros materiales, como el cadmio. [21]
... el carburo de boro es el tercer material más duro de la Tierra.