El carbazol es un compuesto orgánico heterocíclico aromático . Tiene una estructura tricíclica, que consta de dos anillos de benceno de seis miembros fusionados a cada lado de un anillo de cinco miembros que contiene nitrógeno . La estructura del compuesto se basa en la estructura del indol , pero en la que un segundo anillo de benceno está fusionado al anillo de cinco miembros en la posición 2-3 del indol (equivalente al doble enlace 9a-4a en el carbazol, respectivamente).
El carbazol es un componente del humo del tabaco . [3]
Carl Graebe y Carl Glaser aislaron por primera vez el compuesto del alquitrán de hulla en 1872. [4]
Pocos métodos de producción de carbazol son económicamente viables debido a la demanda limitada. Durante la destilación del alquitrán de hulla, el carbazol se concentra en el destilado de antraceno y debe eliminarse antes de la producción de antraquinona ; ese producto de desecho es la principal fuente industrial de carbazol. [4] [5] Los compuestos polares (por ejemplo, las cetonas) lo precipitan selectivamente del antraceno; una técnica más moderna es simplemente la cristalización selectiva a partir de alquitrán de hulla fundido a alta temperatura [4] o baja presión (70 mmHg). [6]
Una síntesis orgánica clásica de laboratorio para el carbazol es la ciclización de Borsche-Drechsel . [7] [8]

En el primer paso, la fenilhidrazina se condensa con ciclohexanona para formar la imina correspondiente . El segundo paso es una reacción de reordenamiento catalizada por ácido clorhídrico y una reacción de cierre de anillo para formar tetrahidrocarbazol. En una modificación, ambos pasos se combinan en uno al llevar a cabo la reacción en ácido acético . [9] En el tercer paso, este compuesto se oxida con plomo rojo para formar el propio carbazol.
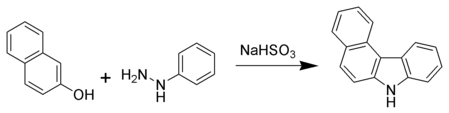
Otro clásico es la síntesis de carbazol de Bucherer , que utiliza un naftol y una arilhidrazina. [10]
Un tercer método para la síntesis de carbazol es la reacción de Graebe-Ullmann.

En el primer paso, un N -fenil-1,2-diaminobenceno ( N -fenil- o -fenilendiamina ) se convierte en una sal de diazonio que instantáneamente forma un 1,2,3-triazol . El triazol es inestable y a temperaturas elevadas, se libera nitrógeno y se forma el carbazol. [11] [12]

Los derivados de difenilamina , al ser ricos en electrones , se oxidan naturalmente a carbazoles cuando se calientan en el aire. [13] Una reacción similar es la reacción de Mallory :

Los carbazoles sustituidos se sintetizan más fácilmente con reacciones de acoplamiento de metales de transición . Para aplicaciones que las impurezas de metales de transición en el producto final podrían inhibir, una alternativa es la sustitución aromática nucleofílica en dióxido de dibenzotiofeno . [14]
Los carbazoles se encuentran de forma natural en los alcaloides de carbazol. Los alcaloides de carbazol con anillos de benceno no sustituidos aparecen raramente. Se ha encontrado olivacina en la corteza de Aspidosperma olivaceum y elipticina en Ochrosia elliptica . [15] Algunos alcaloides de carbazol, especialmente la glibomina B, se han aislado de Glycosmis pentaphylla . [16]
Como los carbazoles tienen un espectro de luz ultravioleta-visible relativamente rico , se utilizan como pigmentos [4] y fotocatalizadores . [17] El carbazol original se utiliza en la producción de Hydron Blue [4] y el aminoetilcarbazol se utiliza en la producción de pigmento violeta 23. [18]

Los carbazoles estabilizan los emisores de tripletes en ciertos diodos emisores de luz ; [4] en general, son fotodonadores de electrones (aceptores de huecos). [19]
El carbazol se oxida electroquímicamente y se convierte en un polímero conductor , que no ha alcanzado un uso industrial sustancial. [20] El polivinilcarbazol es útil en las industrias eléctrica y electrónica, y ciertas novolacas de carbazol son extremadamente resistentes al calor. [4]
En química orgánica, el carbazol propiamente dicho también es un ingrediente de varias moléculas bioactivas . El insecticida Nirosan, [4] el antídoto contra la sobredosis de cocaína Rimcazol y el AINE veterinario Carprofeno están hechos a partir de carbazol. El inhibidor de la topoisomerasa II elipticina fusiona el carbazol a un anillo de piridina .
{{cite encyclopedia}}: CS1 maint: varios nombres: lista de autores ( enlace )Afue invocada pero nunca definida (ver la página de ayuda ).