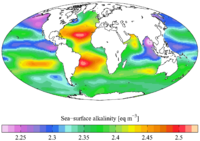
La alcalinidad (del árabe : القلوية , romanizado : al-qaly , literalmente 'cenizas de salina ') [1] es la capacidad del agua para resistir la acidificación . [2] No debe confundirse con la basicidad , que es una medida absoluta en la escala de pH . La alcalinidad es la fuerza de una solución tampón compuesta de ácidos débiles y sus bases conjugadas . Se mide valorando la solución con un ácido como HCl hasta que su pH cambia abruptamente o alcanza un punto final conocido donde eso sucede. La alcalinidad se expresa en unidades de concentración, como meq/L ( miliequivalentes por litro ), μeq/kg (microequivalentes por kilogramo) o mg/L CaCO 3 (miligramos por litro de carbonato de calcio ). [3] Cada una de estas mediciones corresponde a una cantidad de ácido agregado como titulante .
En el agua dulce , particularmente en terrenos no calizos , las alcalinidades son bajas e involucran muchos iones. En el océano, por el contrario, la alcalinidad está completamente dominada por el carbonato y el bicarbonato, además de una pequeña contribución del borato . [4]
Aunque alcalinidad es un término utilizado principalmente por limnólogos [5] y oceanógrafos , [3] también lo utilizan los hidrólogos para describir la dureza temporal . Además, medir la alcalinidad es importante para determinar la capacidad de un arroyo para neutralizar la contaminación ácida proveniente de la lluvia o las aguas residuales . Es una de las mejores medidas de la sensibilidad de la corriente a los aportes de ácido. [6] Puede haber cambios a largo plazo en la alcalinidad de arroyos y ríos en respuesta a perturbaciones humanas como la lluvia ácida generada por las emisiones de SO x y NO x . [7]
En 1884, el profesor Wilhelm (William) Dittmar del Anderson College, ahora Universidad de Strathclyde , analizó 77 muestras de agua de mar prístina de todo el mundo traídas por la expedición Challenger . Encontró que en el agua de mar los iones principales estaban en una proporción fija, confirmando la hipótesis de Johan Georg Forchhammer , que ahora se conoce como el Principio de Proporciones Constantes. Sin embargo, hubo una excepción. Dittmar descubrió que la concentración de calcio era ligeramente mayor en las profundidades del océano y llamó a este aumento alcalinidad. [ cita necesaria ]
También en 1884, Svante Arrhenius presentó su tesis doctoral en la que defendía la existencia de iones en solución y definía los ácidos como donadores de iones hidronio y las bases como donadores de iones hidróxido . Por ese trabajo, recibió el Premio Nobel de Química en 1903. [ cita necesaria ] Véase también Svante Arrhenius#Disociación iónica .
La alcalinidad se refiere aproximadamente a la cantidad molar de bases en una solución que un ácido fuerte puede convertir en especies no cargadas. Por ejemplo, 1 mol de HCO−
3en solución representa 1 equivalente molar, mientras que 1 mol de CO2-3
es 2 equivalentes molares porque serían necesarios el doble de iones H + para equilibrar la carga. La carga total de una solución siempre es igual a cero. [8] Esto conduce a una definición paralela de alcalinidad que se basa en el equilibrio de carga de los iones en una solución.
Ciertos iones, incluidos Na + , K + , Ca 2+ , Mg 2+ , Cl − , SO2-4
y NO−
3son " conservadores " de modo que no se ven afectados por cambios de temperatura, presión o pH. [8] Otros como HCO−
3Se ven afectados por cambios de pH, temperatura y presión. Al aislar los iones conservadores en un lado de esta ecuación de equilibrio de carga, los iones no conservativos que aceptan o donan protones y, por lo tanto, definen la alcalinidad, se agrupan en el otro lado de la ecuación.
Este equilibrio de carga combinado y el equilibrio de protones se denomina alcalinidad total . [9] La alcalinidad total no se ve (muy) afectada por la temperatura, la presión o el pH y, por lo tanto, es en sí misma una medida conservadora, lo que aumenta su utilidad en los sistemas acuáticos. Todos los aniones excepto HCO−
3y CO2-3
Tienen bajas concentraciones en el agua superficial de la Tierra (arroyos, ríos y lagos). Por tanto, la alcalinidad del carbonato , que es igual a [ HCO−
3] + 2[ CO2-3
] también es aproximadamente igual a la alcalinidad total del agua superficial. [8]
La alcalinidad mide la capacidad de una solución para neutralizar ácidos hasta el punto de equivalencia de carbonato o bicarbonato, definido como pH 4,5 para muchos estudios oceanográficos/limnológicos. [10] La alcalinidad es igual a la suma estequiométrica de las bases en solución. En la mayoría de las aguas superficiales de la Tierra, la alcalinidad carbonatada tiende a constituir la mayor parte de la alcalinidad total debido a la aparición y disolución común de rocas carbonatadas y otros procesos de meteorización geológica que producen aniones carbonato. Otros componentes naturales comunes que pueden contribuir a la alcalinidad incluyen borato , hidróxido , fosfato , silicato , amoníaco disuelto y las bases conjugadas de ácidos orgánicos (p. ej., acetato ). Las soluciones producidas en un laboratorio pueden contener un número prácticamente ilimitado de especies que contribuyen a la alcalinidad. La alcalinidad se expresa frecuentemente como equivalentes molares por litro de solución o por kilogramo de disolvente. En contextos comerciales (por ejemplo, la industria de las piscinas) y regulatorios, la alcalinidad también podría darse en partes por millón de carbonato de calcio equivalente (ppm CaCO 3 ) [ cita requerida ] . La alcalinidad a veces se utiliza incorrectamente como sinónimo de basicidad . Por ejemplo, la adición de CO 2 reduce el pH de una solución, reduciendo así la basicidad mientras que la alcalinidad permanece sin cambios (ver ejemplo a continuación).
Se especifican una variedad de valorantes , puntos finales e indicadores para diversos métodos de medición de alcalinidad. Los ácidos clorhídrico y sulfúrico son valorantes ácidos comunes, mientras que la fenolftaleína , el rojo de metilo y el verde de bromocresol son indicadores comunes. [11]
En agua subterránea o agua de mar típica , la alcalinidad total medida se establece en:
(El subíndice T indica la concentración total de las especies en la solución medida. Esto se opone a la concentración libre, que tiene en cuenta la cantidad significativa de interacciones de pares iónicos que ocurren en el agua de mar).
La alcalinidad se puede medir titulando una muestra con un ácido fuerte hasta que se consuma toda la capacidad tampón de los iones antes mencionados por encima del pH del bicarbonato o carbonato. Este punto está funcionalmente fijado en pH 4,5. En este punto, todas las bases de interés han sido protonadas a la especie de nivel cero, por lo que ya no causan alcalinidad. En el sistema carbonato los iones bicarbonato [ HCO−
3] y los iones carbonato [ CO2-3
] se han convertido en ácido carbónico [H 2 CO 3 ] a este pH. Este pH también se denomina punto de equivalencia de CO 2, donde el componente principal del agua es el CO 2 disuelto que se convierte en H 2 CO 3 en una solución acuosa. En este punto no hay ácidos ni bases fuertes. Por tanto, la alcalinidad se modela y cuantifica con respecto al punto de equivalencia de CO 2 . Debido a que la alcalinidad se mide con respecto al punto de equivalencia del CO 2 , la disolución del CO 2 , aunque agrega ácido y carbono inorgánico disuelto, no cambia la alcalinidad. En condiciones naturales, la disolución de rocas básicas y la adición de amoníaco [NH 3 ] o aminas orgánicas conduce a la adición de base a las aguas naturales en el punto de equivalencia de CO 2 . La base disuelta en agua aumenta el pH y titula una cantidad equivalente de CO 2 a ion bicarbonato y ion carbonato. En equilibrio, el agua contiene una cierta cantidad de alcalinidad aportada por la concentración de aniones ácidos débiles. Por el contrario, la adición de ácido convierte los aniones ácidos débiles en CO 2 y la adición continua de ácidos fuertes puede hacer que la alcalinidad sea inferior a cero. [12] Por ejemplo, las siguientes reacciones tienen lugar durante la adición de ácido a una solución típica de agua de mar:
Se puede ver en las reacciones de protonación anteriores que la mayoría de las bases consumen un protón (H + ) para convertirse en una especie neutra, aumentando así la alcalinidad en uno por equivalente. CO2-3
sin embargo, consumirá dos protones antes de convertirse en una especie de nivel cero (CO 2 ), por lo que aumenta la alcalinidad en dos por mol de CO.2-3
. [H + ] y [ HSO−
4] disminuyen la alcalinidad, ya que actúan como fuentes de protones. A menudo se representan colectivamente como [H + ] T.
La alcalinidad normalmente se informa como mg/L como CaCO 3 . (La conjunción "como" es apropiada en este caso porque la alcalinidad resulta de una mezcla de iones, pero se informa "como si" todo esto se debiera al CaCO 3 ). Esto se puede convertir en miliequivalentes por litro (meq/L). dividiendo por 50 (el MW aproximado de CaCO 3 dividido por 2).
La adición (o eliminación) de CO 2 a una solución no cambia su alcalinidad, ya que la reacción neta produce el mismo número de equivalentes de especies que contribuyen positivamente (H + ) que de especies que contribuyen negativamente ( HCO) .−
3y/o CO2-3
). Agregar CO 2 a la solución reduce su pH, pero no afecta la alcalinidad.
En todos los valores de pH:
Sólo con valores de pH altos (básicos):
La adición de CO 2 a una solución en contacto con un sólido puede (con el tiempo) afectar la alcalinidad, especialmente para los minerales carbonatados en contacto con agua subterránea o agua de mar. La disolución (o precipitación) de la roca carbonatada tiene una fuerte influencia sobre la alcalinidad. Esto se debe a que la roca carbonatada está compuesta de CaCO 3 y su disociación agregará Ca 2+ y CO.2-3
en solución. Ca 2+ no influirá en la alcalinidad, pero sí el CO2-3
aumentará la alcalinidad en 2 unidades. La mayor disolución de la roca carbonatada por la acidificación de la lluvia ácida y la minería ha contribuido al aumento de las concentraciones de alcalinidad en algunos ríos importantes en todo el este de EE. UU. [7] La siguiente reacción muestra cómo la lluvia ácida, que contiene ácido sulfúrico, puede tener el efecto de aumentar la alcalinidad del río al aumentando la cantidad de ion bicarbonato:
Otra forma de escribir esto es:
Cuanto menor sea el pH, mayor será la concentración de bicarbonato. Esto muestra cómo un pH más bajo puede conducir a una mayor alcalinidad si la cantidad de bicarbonato producido es mayor que la cantidad de H + que queda después de la reacción. Esto es así porque la cantidad de ácido en el agua de lluvia es baja. Si estas aguas subterráneas alcalinas entran posteriormente en contacto con la atmósfera, pueden perder CO 2 , precipitar carbonatos y, por tanto, volverse menos alcalinas. Cuando los minerales carbonatados, el agua y la atmósfera están en equilibrio, la reacción reversible
muestra que el pH estará relacionado con la concentración de iones de calcio, con un pH más bajo asociado a una concentración de iones de calcio más alta. En este caso, cuanto mayor sea el pH, más bicarbonato y iones carbonato habrá, a diferencia de la situación paradójica descrita anteriormente, donde no se tiene equilibrio con la atmósfera.
En el océano, la alcalinidad está completamente dominada por el carbonato y el bicarbonato, además de una pequeña contribución del borato . [4]
Así, la ecuación química para la alcalinidad del agua de mar es:
Existen muchos métodos de generación de alcalinidad en el océano . Quizás la más conocida es la disolución del carbonato de calcio para formar Ca 2+ y CO.2-3
(carbonato). El ion carbonato tiene el potencial de absorber dos iones de hidrógeno. Por tanto, provoca un aumento neto de la alcalinidad del océano. La disolución del carbonato de calcio se produce en regiones del océano que están infrasaturadas con respecto al carbonato de calcio.
El aumento del nivel de dióxido de carbono en la atmósfera , debido a las emisiones de dióxido de carbono , da como resultado una mayor absorción de CO 2 de la atmósfera hacia los océanos. [13] Esto no afecta la alcalinidad del océano [14] : 2252 pero sí resulta en una reducción en el valor del pH (llamada acidificación del océano ). [15] Se ha propuesto mejorar la alcalinidad del océano como una opción para agregar alcalinidad al océano y, por lo tanto, amortiguar los cambios de pH. [16] : 181
Los procesos biológicos tienen un impacto mucho mayor sobre la alcalinidad oceánica en escalas de tiempo cortas (de minutos a siglos). [17] La respiración aeróbica de la materia orgánica puede disminuir la alcalinidad mediante la liberación de protones. [17] La desnitrificación y la reducción de sulfatos ocurren en ambientes con oxígeno limitado. Ambos procesos consumen iones de hidrógeno (aumentando así la alcalinidad) y liberan gases (N 2 o H 2 S), que eventualmente escapan a la atmósfera. Tanto la nitrificación como la oxidación de sulfuros disminuyen la alcalinidad al liberar protones como subproducto de las reacciones de oxidación. [18]
La alcalinidad del océano varía con el tiempo, de manera más significativa a lo largo de escalas de tiempo geológicas (milenios). Los cambios en el equilibrio entre la erosión terrestre y la sedimentación de minerales carbonatados (por ejemplo, en función de la acidificación de los océanos) son los principales impulsores a largo plazo de la alcalinidad en los océanos. [19] En escalas de tiempo humanas, la alcalinidad media del océano es relativamente estable. [20] La variabilidad estacional y anual de la alcalinidad media del océano es muy baja. [21]
La alcalinidad varía según la ubicación dependiendo de la evaporación/precipitación, la advección de agua, los procesos biológicos y los procesos geoquímicos. [4]
La mezcla dominada por los ríos también ocurre cerca de la costa; es más fuerte cerca de la desembocadura de un río grande. Aquí, los ríos pueden actuar como fuente o sumidero de alcalinidad. A T sigue la salida del río y tiene una relación lineal con la salinidad. [21]
La alcalinidad oceánica también sigue tendencias generales basadas en la latitud y la profundidad. Se ha demostrado que la A T es a menudo inversamente proporcional a la temperatura de la superficie del mar (SST). Por lo tanto, generalmente aumenta con latitudes y profundidades altas. Como resultado, las áreas de surgencia (donde el agua de las profundidades del océano es empujada hacia la superficie) también tienen valores de alcalinidad más altos. [22]
Existen muchos programas para medir, registrar y estudiar la alcalinidad oceánica, junto con muchas de las otras características del agua de mar, como la temperatura y la salinidad. Estos incluyen: GEOSECS (Estudio de secciones geoquímicas del océano), [23] TTO/NAS (Estudio de trazadores transitorios en el océano/Atlántico norte), JGOFS (Estudio conjunto sobre el flujo oceánico global), [24] WOCE (Experimento de circulación oceánica mundial), [ 25] CARINA (Dióxido de carbono en el Océano Atlántico). [26]
{{citation}}: Mantenimiento CS1: DOI inactivo a partir de enero de 2024 ( enlace )Los siguientes paquetes calculan el estado del sistema de carbonatos en el agua de mar (incluido el pH):