
La química de organocobre es el estudio de las propiedades físicas, reacciones y síntesis de compuestos de organocobre , que son compuestos organometálicos que contienen un enlace químico de carbono a cobre . [1] [2] [3] Son reactivos en química orgánica .
El primer compuesto organocobre, el explosivo acetiluro de cobre (I) Cu 2 C 2 ( Cu−C≡C−Cu ), fue sintetizado por Rudolf Christian Böttger en 1859 al pasar gas acetileno a través de una solución de cloruro de cobre (I) : [4]
Los compuestos de organocobre son diversos en estructura y reactividad, pero casi todos se basan en cobre con un estado de oxidación de +1, a veces denominado Cu(I) o Cu + . Con 10 electrones en su capa de valencia , el comportamiento de enlace del Cu(I) es similar al del Ni(0), pero debido a su mayor estado de oxidación, participa en menos enlaces posteriores pi . Los derivados orgánicos de los estados de oxidación más altos del cobre +2 y +3 se encuentran a veces como intermediarios de reacción , pero rara vez se aíslan o incluso se observan.
Los compuestos organocobre forman complejos con una variedad de ligandos blandos como alquilfosfinas ( R 3 P ), tioéteres ( R 2 S ) y cianuro ( CN − ).
Debido a la capa electrónica esférica de Cu + , los complejos de cobre(I) tienen estructuras simétricas (lineales, trigonales planas o tetraédricas ) , dependiendo del número de ligandos.
Desde hace mucho tiempo se sabe que las sales de cobre (I) se unen al CO, aunque de forma débil. Un complejo representativo es el CuCl(CO), que es polimérico. A diferencia de los carbonilos metálicos clásicos, la unión posterior de pi no es fuerte en estos compuestos. [5]

Los alquenos se unen al cobre (I), aunque nuevamente de manera débil. La unión del etileno al Cu en las proteínas tiene una gran importancia en la biología vegetal, hasta el punto de que el etileno se clasifica como una hormona vegetal . Su presencia, detectada por la proteína Cu, afecta la maduración y muchos otros procesos. [6]
Aunque el cobre no forma un metaloceno , se pueden producir complejos de semisándwich. Uno de estos derivados es el π-ciclopentadienil(trietilfosfina)cobre(I). [7]
Los haluros de cobre reaccionan con reactivos de organolitio para dar compuestos de organocobre. El área fue iniciada por Henry Gilman , quien informó sobre el metilcobre en 1936. Por lo tanto, el fenilcobre se prepara por reacción del fenillitio con bromuro de cobre (I) en éter dietílico . Los reactivos de Grignard se pueden utilizar en lugar de compuestos de organolitio. Gilman también investigó los dialquilcupratos. Estos se obtienen combinando dos equivalentes de RLi con sales de Cu (I). Alternativamente, estos cupratos se preparan a partir de compuestos de organocobre neutros oligoméricos mediante el tratamiento con un equivalente de reactivo de organolitio.
Los compuestos del tipo [CuR n ] ( n −1)− son reactivos con el oxígeno y el agua, formando óxido de cobre(I) . También tienden a ser térmicamente inestables, lo que puede ser útil en ciertas reacciones de acoplamiento. A pesar de o debido a estas dificultades, los reactivos de organocobre se generan y consumen con frecuencia in situ sin intentar aislarlos. Se utilizan en síntesis orgánica como reactivos alquilantes porque exhiben una mayor tolerancia de grupo funcional que los reactivos de Grignard y organolitio correspondientes. La electronegatividad del cobre es mucho mayor que la de su vecino de al lado en los elementos del grupo 12 , el zinc , lo que sugiere una nucleofilia disminuida para sus ligandos de carbono.
Las sales de cobre reaccionan con los alquinos terminales para formar los acetiluros .
Los haluros de alquilo reaccionan con compuestos de organocobre con inversión de configuración. Por otra parte, las reacciones de compuestos de organocobre con haluros de alquenilo se producen manteniendo la configuración del sustrato. [8]
Los compuestos organocobre se acoplan con haluros de arilo (ver condensación de Ullmann y reacción de Ullmann ):
Los complejos de alquilo y arilo de cobre se agregan tanto en forma cristalina como en solución. La agregación es especialmente evidente para los compuestos de organocobre de carga neutra, es decir, especies con la fórmula empírica (RCu), que adoptan estructuras cíclicas. Dado que cada centro de cobre requiere al menos dos ligandos, el grupo orgánico es un ligando puente . Este efecto se ilustra mediante la estructura del mesitilocobre, que es un pentámero. También se observa una estructura cíclica para CuCH 2 SiMe 3 , donde Me representa el grupo metilo CH 3 , el primer compuesto de organocobre 1:1 que se analizó mediante cristalografía de rayos X (1972 por Lappert). Este compuesto es relativamente estable porque los voluminosos grupos trimetilsililo proporcionan protección estérica. Es un tetrámero , que forma un anillo de 8 miembros con enlaces alternados Cu-C. Además, los cuatro átomos de cobre forman un anillo planar Cu 4 basado en enlaces de dos electrones de tres centros . La longitud del enlace cobre-cobre es de 242 pm , en comparación con las 256 pm del cobre en masa. En el pentafluorofenilcobre se forma un anillo de cobre de 5 miembros, similar al (2,4,6-trimetilfenil)oro, y el pentafluorofenilcobre es un tetrámero. [9]
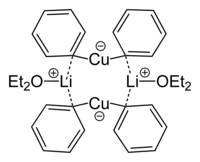
El dimetilcuprato de litio (I) es un dímero en éter dietílico , que forma un anillo de 8 miembros con dos átomos de litio que unen dos grupos metilo, (Li + [Cu(CH 3 ) 2 ] − ) 2 . De manera similar, el difenilcuprato de litio (I) forma un eterato dimérico, ([Li(O(CH 2 CH 3 ) 2 )] + [Cu Ph 2 ] − ) 2 , en estado sólido. [10]
La participación del estado de oxidación Cu(III), por lo demás raro, se ha demostrado en la adición conjugada del reactivo de Gilman a una enona : [11] En un experimento de RMN de inyección rápida a −100 °C, se introdujo el reactivo de Gilman Li + [Cu(CH 3 ) 2 ] − (estabilizado con yoduro de litio ) en ciclohexenona ( 1 ), lo que permitió detectar el complejo pi de cobre-alqueno 2 . Tras la adición posterior de cianuro de trimetilsililo, se forma la especie Cu(III) 3 (indefinidamente estable a esa temperatura) y, al aumentar la temperatura a −80 °C, el producto de adición conjugada 4 . Según un experimento in silico adjunto [12], el intermedio Cu(III) tiene una geometría molecular plana cuadrada con el grupo ciano en orientación cis con respecto al grupo ciclohexenil metino y antiparalelo al protón metino. Con otros ligandos distintos del grupo ciano, este estudio predice compuestos de Cu(III) estables a temperatura ambiente .
Antes del desarrollo de las reacciones de acoplamiento cruzado catalizadas por paladio , el cobre fue el catalizador preferido durante casi un siglo. El paladio ofrece una reacción más rápida y selectiva. Los reactivos y catalizadores de cobre siguen siendo objeto de innovación. En comparación con el paladio, el cobre es más barato, pero los números de recambio suelen ser menores con el cobre y las condiciones de reacción son más vigorosas. [13]
Las reacciones de Li + [CuR 2 ] − con haluros de alquilo R'−X dan el producto de acoplamiento:
El mecanismo de reacción implica la adición oxidativa (OA) del haluro de alquilo a Cu(I), formando un intermedio planar de Cu(III), seguido de eliminación reductora (RE). El ataque nucleofílico es el paso determinante de la velocidad. En la sustitución del yoduro , se propone un mecanismo de transferencia de un solo electrón (ver figura).
En esta reacción participan muchos electrófilos. El orden aproximado de reactividad, comenzando por los más reactivos, es el siguiente: cloruros de ácido [14] > aldehídos > tosilatos ~ epóxidos > yoduros > bromuros > cloruros > cetonas > ésteres > nitrilos >> alquenos
En general, el mecanismo de OA-RE es análogo al de las reacciones de acoplamiento cruzado catalizadas por paladio. Una diferencia entre el cobre y el paladio es que el cobre puede sufrir procesos de transferencia de un solo electrón. [8]
El acoplamiento oxidativo es el acoplamiento de acetiluros de cobre a alquinos conjugados en el acoplamiento de Glaser (por ejemplo en la síntesis de ciclooctadecanonaeno ) o a haluros de arilo en el acoplamiento de Castro-Stephens .
El acoplamiento reductivo es una reacción de acoplamiento de haluros de arilo con un equivalente estequiométrico de cobre metálico que ocurre en la reacción de Ullmann . Una reacción relacionada llamada acoplamiento cruzado descarboxilativo , un compañero de acoplamiento es un carboxilato. Cu(I) desplaza un carboxilo formando el intermedio de arilcobre (ArCu). Simultáneamente, un catalizador de paladio reacciona con un bromuro de arilo para dar un intermedio de organopaladio (Ar'PdB), que sufre transmetalación para dar ArPdAr', que a su vez elimina reductivamente el biarilo . [15] [16]
El acoplamiento neutro redox es el acoplamiento de alquinos terminales con haloalquinos con una sal de cobre (I) en el acoplamiento de Cadiot-Chodkiewicz . También es posible el acoplamiento térmico de dos compuestos organocobre.
La carbocupración es una adición nucleofílica de reactivos de organocobre ( R−Cu ) al acetileno o alquinos terminales que dan como resultado un compuesto de alquenilcobre ( R 2 C=C(R)−Cu ). [17] Es un caso especial de carbometalación y también se denomina reacción de Normant . [18] [19]
Los hidruros de cobre son agentes reductores especializados . El conocido hidruro de cobre es el reactivo de Stryker , con la fórmula [(PPh3 ) CuH] 6 . Reduce la porción alqueno de los compuestos carbonílicos α,β-insaturados . [21] Una reacción relacionada pero catalítica utiliza un complejo de cobre(I) NHC con equivalentes de hidruro proporcionados por un hidrosilano . [22] [23]
En general, la reacción de alquilación de reactivos de organocobre se lleva a cabo mediante alquilación gamma . El ataque gamma cis ocurre mejor en el carbamato de ciclohexilo debido a la estérica . Se informa que la reacción es favorable en solventes etéreos. Se demostró que este método es muy eficaz para el acoplamiento oxidativo de aminas y alquilo, incluidos los haluros de terc -butilo y arilo. [24]
Funcionalización vecinal mediante una secuencia de reacción aldólica de carbocupración/Mukaiyama: [25]
Muller y colaboradores informaron una funcionalización vecinal de ésteres α,β-acetilénicos utilizando una secuencia de reacción aldólica de carbocupración/Mukaiyama (como se muestra en la figura anterior); la carbocupración favorece la formación del Z-aldol.