
En química orgánica , el término catión 2-norbornilo (o catión 2-biciclo[2.2.1]heptilo ) describe un derivado iónico carbonio del norbornano . Se cristalizó una sal del catión 2-norbornilo y se caracterizó por cristalografía de rayos X, lo que confirmó la estructura no clásica. [1]

Los defensores de la naturaleza no clásica del catión 2-norbornilo estable suelen representar las especies utilizando estructuras de resonancia o una única estructura con enlaces parciales ( véase la Figura 2 ). Esta interacción hipovalente puede imaginarse como el efecto neto de i) un enlace sigma parcial entre los carbonos 1 y 6, ii) un enlace sigma parcial entre los carbonos 2 y 6, y iii) un enlace pi parcial entre los carbonos 1 y 2. [2] Cada enlace parcial se representa como un enlace completo en una de las tres estructuras de resonancia o como un enlace parcial discontinuo si el catión se representa a través de una única estructura.

Se ha debatido en qué medida la estructura de resonancia unida a pi contribuye realmente a la estructura electrónica deslocalizada. [4] Mediante espectroscopia de RMN de 1 H y 13 C , se ha confirmado que una carga positiva significativa se encuentra en el carbono 6 del metileno. [5] Esto es sorprendente, ya que los carbocationes primarios son mucho menos estables que los carbocationes secundarios. Sin embargo, el catión 2-norbornilo se puede formar a partir de derivados de β-(Δ 3 -ciclopentenil)-etano, lo que indica que la estructura de resonancia unida a pi es significativa. [6]
El catión 2-norbornilo fue uno de los primeros ejemplos de un ion no clásico . Los iones no clásicos se pueden definir como cationes orgánicos en los que la densidad electrónica de un orbital de enlace lleno se comparte entre tres o más centros y contiene algún carácter de enlace sigma. [7] El catión 2-norbornilo se considera el prototipo de los iones no clásicos. Otros cationes simples como el acetileno protonado (etinio, C
2yo+
3), etileno protonado (etenio, C
2yo+
5) y etano protonado (etanio, C
2yo+
7Se ha demostrado que ) se describen mejor como no clásicos a través de espectroscopia infrarroja. [8]
La representación orbital molecular propuesta con mayor frecuencia para el catión 2-norbornilo se muestra en la Figura 3. Dos orbitales de tipo p , uno en cada uno de los carbonos 1 y 2, interactúan con un orbital hibridado sp 3 en el carbono 6 para formar el enlace hipovalente. [3] [9] Los cálculos de la teoría de Hückel extendida para el catión 2-norbornilo sugieren que el orbital en el carbono 6 podría, en cambio, estar hibridado sp 2 , aunque esto solo afecta la geometría de los hidrógenos geminales . [10]

Según los defensores de un potencial de doble pozo clásico, el catión 2-norbornilo existe en equilibrio dinámico entre dos estructuras asimétricas enantioméricas . La especie deslocalizada central para el cuadro no clásico es simplemente un estado de transición entre las dos estructuras. Se invocan los reordenamientos de Wagner-Meerwein como el mecanismo que convierte entre los dos enantiómeros ( ver Figura 4 ).
Los intentos de aislar las especies asimétricas mediante espectroscopia suelen ser infructuosos. Se informa que la principal razón de este fracaso son las velocidades de reacción directa e inversa extremadamente rápidas , lo que indica una barrera potencial muy baja para la interconversión entre los dos enantiómeros. [2]
Algunos químicos también han considerado que el catión 2-norbornilo está mejor representado por el ion nortriciclonio, un nortriciclonio protonado simétrico en C 3 . Esta representación se invocó por primera vez para explicar parcialmente los resultados de un experimento de mezcla de isótopos de 14 C. [11] La representación orbital molecular de esta estructura implica una interacción en fase entre los orbitales hibridados sp 2 de los carbonos 1, 2 y 6 y el orbital atómico 1s en un átomo de hidrógeno compartido ( ver Figura 5 ). [12]

Los iones no clásicos difieren de los cationes tradicionales en su estructura electrónica : aunque los enlaces químicos se representan típicamente como el intercambio de electrones entre dos átomos, los iones no clásicos estables pueden contener tres o más átomos que comparten un solo par de electrones. [7] En 1939, Thomas Nevell y otros intentaron dilucidar el mecanismo para transformar el clorhidrato de canfeno en cloruro de isobornilo . En uno de los mecanismos de reacción propuestos que se describen en el artículo, la carga positiva de un catión intermedio no se asignó a un solo átomo sino a la estructura en su conjunto. [13] Esto fue citado más tarde por los oponentes de la descripción no clásica como la primera vez que se invocó un ion no clásico. [14] Sin embargo, el término "ion no clásico" no apareció explícitamente en la literatura química hasta más de una década después, cuando se utilizó para etiquetar el enlace deslocalizado en un catión butílico piramidal. [15]
El término ion sinartético también se utilizó para describir el enlace deslocalizado en carbocationes estables antes de que se generalizara el término ion no clásico . Los primeros usuarios de este término comentaron la sorprendente similitud entre el enlace en estos tipos de cationes y el enlace en los borohidruros . [16]
En 1949, Saul Winstein observó que el brosilato de 2- exo -norbornilo ( p -bromobencenosulfonato) y el tosilato de 2- endo -norbornilo ( p -toluenosulfonato) daban una mezcla racémica del mismo producto, acetato de 2- exo -norbornilo , tras acetólisis ( véase la Figura 6 ). Dado que los tosilatos y los brosilatos funcionan igualmente bien como grupos salientes , concluyó que tanto el norbornano sustituido en 2- endo como en 2- exo deben pasar por un intermedio catiónico común con una reactividad exo dominante . Informó que este intermedio era muy probablemente un catión 2-norbornilo deslocalizado y simétrico. [17] Más tarde se demostró mediante cromatografía en fase de vapor que la cantidad de epímero endo del producto producido era inferior al 0,02%, lo que demuestra la alta estereoselectividad de la reacción. [18]


Cuando un solo enantiómero de brosilato de 2- exo -norbornilo sufre acetólisis, no se observa actividad óptica en el acetato de 2- exo -norbornilo resultante ( ver Figura 7 ). [17] Según la descripción no clásica del catión 2-norbornilo, el plano de simetría presente (que recorre los carbonos 4, 5 y 6) permite un acceso igualitario a ambos enantiómeros del producto, lo que da como resultado la mezcla racémica observada .
También se observó que los norbornanos 2- exo -sustituidos reaccionaron 350 veces más rápido que los isómeros endo correspondientes . La ayuda anquimérica del enlace sigma entre los carbonos 1 y 6 se racionalizó como la explicación de este efecto cinético. [17] Es importante destacar que la ayuda anquimérica invocada llevó a muchos químicos a postular que la estabilidad energética del catión 2-norbornilo se debía directamente a la estructura simétrica y en puente invocada en la explicación no clásica. Sin embargo, algunos otros autores ofrecieron explicaciones alternativas para la alta estabilidad sin invocar una estructura no clásica. [19]
En 1951, se sugirió por primera vez que el catión 2-norbornilo podría describirse mejor si se lo considera como un ion nortriciclonio. [11] Se ha demostrado que el principal producto formado a partir de una reacción de eliminación del catión 2-norbornilo es el nortriciclono (no el norborneno), pero se ha afirmado que esto respalda ambos postulados de iones no clásicos. [18]
Herbert C. Brown propuso que no era necesario invocar un nuevo tipo de enlace en intermediarios estables para explicar la reactividad del catión 2-norbornilo. Criticando a muchos químicos por ignorar las explicaciones anteriores de la reactividad, Brown argumentó que toda la información antes mencionada sobre el catión 2-norbornilo podría explicarse utilizando efectos estéricos simples presentes en el sistema norbornilo. [2] Dado que una explicación alternativa que utilizaba un par de iones que se equilibraban rápidamente para describir el catión 2-norbornilo era válida, no vio la necesidad de invocar una descripción estable y no clásica del enlace. [20] Invocar iones estables no clásicos se estaba volviendo algo común; Brown sintió que esto no solo era injustificado sino también contraproducente para el campo de la química en su conjunto. De hecho, muchos artículos que informaban sobre iones estables no clásicos fueron posteriormente retractados por ser poco realistas o incorrectos. [21] Después de publicar esta controvertida visión en 1962, Brown comenzó una búsqueda para encontrar evidencia experimental incompatible con la imagen deslocalizada del enlace en el catión 2-norbornilo. [22]
Brown también trabajó para demostrar la inestabilidad de una estructura electrónica deslocalizada para el catión 2-norbornilo. Si se pudiera demostrar que el ion no clásico tiene mayor energía que el par de iones clásicos correspondiente, el ion no clásico solo se consideraría un estado de transición entre los dos cationes asimétricos. [21] [23] Aunque no descartó la posibilidad de un estado de transición deslocalizado, Brown continuó rechazando la simetría reflexiva propuesta del catión 2-norbornilo, incluso al final de su carrera. [24]
La introducción del enlace deslocalizado de dos electrones con tres centros invocado en la imagen no clásica del catión 2-norbornilo permitió a los químicos explorar un reino completamente nuevo de enlaces químicos. Los químicos estaban ansiosos por aplicar las características de los estados electrónicos hipovalentes a sistemas nuevos y viejos por igual (aunque varios se dejaron llevar demasiado). [4] Uno de los conceptos más importantes que emergieron de la intensa investigación centrada en los iones no clásicos fue la idea de que los electrones ya involucrados en enlaces sigma podrían estar involucrados con la reactividad. Aunque se sabía que los orbitales pi llenos eran donantes de electrones , los químicos habían dudado de que los orbitales sigma pudieran funcionar en la misma capacidad. La descripción no clásica del catión 2-norbornilo puede verse como la donación de un par de electrones de un enlace sigma carbono-carbono a un orbital p vacío de carbono 2. Por lo tanto, este carbocatión mostró que la donación de electrones de enlace sigma es tan plausible como la donación de electrones de enlace pi. [25] [26]
El intenso debate que siguió al desafío de Brown a los defensores de los iones no clásicos también tuvo un gran impacto en el campo de la química. Para probar o refutar la naturaleza no clásica del catión 2-norbornilo, los químicos de ambos lados del debate buscaron celosamente nuevas técnicas para la caracterización química e interpretaciones más innovadoras de los datos existentes. [27] Una técnica espectroscópica que se desarrolló aún más para investigar el catión 2-norbornilo fue la espectroscopia de resonancia magnética nuclear de compuestos en medios altamente ácidos. [19] A menudo se hacían comparaciones del catión 2-norbornilo con estados de transición inestables con estados electrónicos deslocalizados cuando se intentaba dilucidar si el sistema norbornilo era estable o no. Estos esfuerzos motivaron investigaciones más detalladas de los estados de transición y aumentaron enormemente la comprensión de la comunidad científica sobre su estructura electrónica. [27] En resumen, la vigorosa competencia entre grupos científicos condujo a una investigación extensa y a una mejor comprensión de los conceptos químicos subyacentes.
El catión 2-norbornilo se puede obtener mediante una multitud de rutas sintéticas. Estas rutas se pueden agrupar en tres clases: formación σ , formación π y formación por reordenamiento . Cada una de ellas se analiza por separado a continuación.

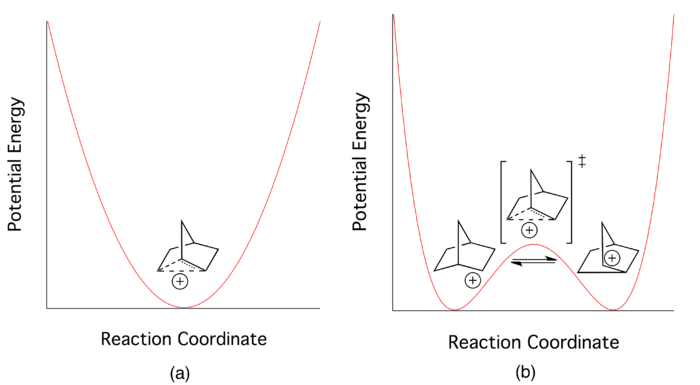
El material de partida para esta ruta es un derivado de norbornano con un buen grupo saliente en la posición 2. Si el grupo saliente está en la cara exo , la densidad electrónica del enlace σ entre los carbonos 1 y 6 se dona al antienlace σ* entre el carbono 2 y el grupo saliente ( ver Figura 8b ). [28]
Si el grupo saliente está en la cara endo , el grupo saliente primero sale por sí solo. Luego, la densidad electrónica del enlace σ entre los carbonos 1 y 6 se dona al orbital atómico vacío resultante en el carbono 2. Sin embargo, esta ruta de formación es mucho más lenta que la del isómero exo porque el enlace σ no puede proporcionar asistencia anquimérica para el primer paso, lo que hace que la energía de activación para el primer estado de transición sea mucho mayor. Además, si hay una alta concentración de electrófilos reactivos en la mezcla de reacción, la formación de un derivado de norbornano recién sustituido puede impedir la formación de iones no clásicos. [17] [29]
Un ejemplo de esta ruta de formación es la reacción que llevó a Winstein y Trifan a proponer la estructura deslocalizada del catión 2-norbornilo. Los tosilatos y brosilatos de 2-norbornilo forman el catión 2-norbornilo a través de esta ruta como un intermediario hacia la solvólisis . [17]
El material de partida para esta ruta es un derivado de β-(Δ 3 -ciclopentenil)-etano con un buen grupo saliente en el carbono terminal del grupo etano. La densidad electrónica del enlace π de la fracción de alqueno se dona al antienlace σ* entre el carbono terminal y el grupo saliente ( ver Figura 8c ). [28] [29]
Por ejemplo, el producto principal de la acetólisis del nosilato de β-(Δ 3 -ciclopentenil)-etilo ( p -nitrobencenosulfonato) es el acetato de 2- exo -norbornilo. La falta de acetato de β-(Δ 3 -ciclopentenil)-etilo presente después de la reacción se explica por la mayor estabilidad del sistema norbornilo sobre el sistema ciclopentenilo decorado. [6]
Esta ruta sólo es eficaz si la olefina de ciclopentenilo se aísla de cualquier sistema de enlace π más grande. La velocidad de reacción disminuye significativamente si el doble enlace involucrado forma un anillo aromático de seis miembros, como ocurre en el nosilato de 2-indaniletilo. Se ha observado que las sustituciones de alquilo en las olefinas aumentan la velocidad de reacción al estabilizar el carbocatión resultante. [30]
El catión 2-norbornilo también se puede formar a través de reordenamientos de iones similares, como los cationes 1-norbornilo y 7-norbornilo, aunque estos no se comprenden tan bien en general. Los experimentos de marcado con isótopos radiactivos de carbono-14 han demostrado que la combinación compleja en los sistemas de cationes norbornilo permite que el 14 C esté presente en las siete posiciones del sistema norbornilo. [11] Al alternar entre temperaturas bajas y altas durante las hidrólisis de 1- y 7-cloronorbornanos, se observó una gran cantidad de 2-norbornanol además de los 1- y 7-norbornanoles esperados, respectivamente. Por lo tanto, los cationes 1- y 7-norbornilo tienen algún mecanismo por el cual pueden reordenarse al catión 2-norbornilo más estable en la escala de tiempo de las reacciones de solvólisis. [31]
Una prueba para comprobar si el catión 2-norbornilo es o no no clásico es investigar la simetría inherente del catión. Muchas herramientas espectroscópicas, como la espectroscopia de resonancia magnética nuclear (espectroscopia de RMN) y la espectroscopia Raman , dan pistas sobre la simetría reflexiva y rotacional presente en una molécula o ion. Cada una de las tres estructuras propuestas del catión 2-norbornilo ilustra una simetría molecular distinta. La forma no clásica contiene un plano de reflexión a través de los carbonos 4, 5, 6 y el punto medio de los carbonos 1 y 2. La forma clásica no contiene simetría reflexiva ni rotacional. La estructura protonada del nortricicleno contiene un eje de rotación simétrico en C 3 a través del carbono 4.
Cada pico de un espectro de RMN corresponde a un conjunto de átomos de un elemento particular que se encuentran en entornos químicos similares. El espectro de RMN de la sal de cloropentafluoruro de antimonio del catión 2-norbornilo no es útil a temperatura ambiente porque los desplazamientos de hidruro ocurren más rápido que la escala de tiempo de un experimento de RMN; la mayoría de los hidrógenos se consideran, por lo tanto, equivalentes y se tienen en cuenta en el mismo pico de absorción. Al reducir la temperatura del experimento de RMN a -60 °C, los desplazamientos de hidruro se "congelan" y se puede obtener más información estructural del espectro. Los investigadores descubrieron que a estas bajas temperaturas, el espectro de RMN de 1 H coincidía con lo que se esperaría para la estructura no clásica del ion. [31] [32]
Los estudios de RMN de 1H y 13C pudieron confirmar que cualquier reordenamiento de Wagner-Meerwein propuesto ocurrió más rápido que la escala de tiempo del experimento de RMN, incluso a bajas temperaturas. [33] Para moléculas en equilibrio estático con respecto a los reordenamientos, la RMN revela cuántos conjuntos de núcleos relacionados con la simetría hay en la molécula y cuántos núcleos representa cada uno de estos conjuntos a través de la integración del espectro. Para moléculas en equilibrio dinámico, como el catión 2-norbornilo, los núcleos dentro de cada conjunto también pueden transformarse entre sí a través de reordenamientos con velocidades de reacción rápidas. [34] Dado que el equilibrio dinámico propuesto por los defensores del ion clásico tenía velocidades de reordenamiento muy rápidas, los primeros estudios de RMN no favorecieron ni invalidaron ninguna de las tres estructuras propuestas. [5] Pero al usar el análisis de RMN de estado sólido , se puede reducir la temperatura del experimento de RMN a 5 kelvins (−268 °C) y, por lo tanto, ralentizar significativamente cualquier fenómeno de reordenamiento. Los espectros de RMN de 13 C en estado sólido del catión 2-norbornilo muestran que los carbonos 1 y 2 están en entornos químicos idénticos, lo que es consistente solo con la imagen no clásica del catión 2-norbornilo. [35]
Los espectros Raman del catión 2-norbornilo muestran una especie más simétrica de lo que cabría esperar para un par de iones clásicos que se equilibran rápidamente. Dado que las velocidades de reacción propuestas para los reordenamientos de iones clásicos son más lentas que la escala de tiempo Raman, cabría esperar que los espectros Raman indicaran una especie menos simétrica si la imagen clásica fuera correcta. [4]
Algunos estudios de RMN de 13 C en particular favorecieron la interpretación a través de la estructura del nortricicleno protonado. [36] Además, los espectros Raman del catión 2-norbornilo en algunos solventes ácidos muestran una banda de absorción a 3110 cm -1 indicativa de un anillo de ciclopropano empobrecido en electrones. Dado que esa banda de absorción sería esperable en el nortricicleno protonado C 3 -simétrico, algunos científicos afirmaron que esto era evidencia convincente para esta interpretación. [37] Otros químicos han postulado que las propiedades del catión 2-norbornilo dependen mucho del entorno del solvente. Aunque la alta acidez y baja nucleofilicidad de los solventes utilizados en los experimentos mencionados anteriormente pueden hacer que la geometría del nortricilconio protonado sea la más estable, esta geometría no necesita ser la más favorable energéticamente en otros solventes. [4]
Se han realizado muchos cálculos sobre las estructuras clásicas y no clásicas. [38] [10] [39]
Comparando el reordenamiento entre el catión 3-metil-2-norbornilo y el catión 2-metil-2-norbornilo con el que se produce entre los carbocationes isopentano terciario y secundario , se observa que el cambio de entalpía es aproximadamente 6 kcal/mol menor para el sistema norbornilo. Dado que la principal diferencia entre estos dos reordenamientos reversibles es la cantidad de deslocalización posible en el estado electrónico fundamental, se puede atribuir la estabilización del catión 3-metil-2-norbornilo a su naturaleza no clásica. [40] Sin embargo, algunos estudios experimentales no lograron observar esta estabilización en las reacciones de solvólisis. [21]
Otros estudios sobre la estabilidad del catión 2-norbornilo han demostrado que las sustituciones alquílicas en el carbono 1 o 2 obligan al sistema a ser decididamente clásico. Los carbocationes terciarios son mucho más estables que sus homólogos secundarios y, por lo tanto, no necesitan adoptar enlaces deslocalizados para alcanzar la energía potencial más baja posible. [41] [42]
Para apoyar su sugerencia de la naturaleza no clásica del catión 2-norbornilo, Winstein y Trifan utilizaron primero evidencia cinética de la mayor velocidad de reacción para la formación del catión 2- exo -norbornilo sobre el catión 2- endo -norbornilo. [17] Otros investigadores investigaron la velocidad de reacción de compuestos que podrían presentar asistencia anquimérica pero que no podrían sufrir reordenamientos, ya que el sistema norbornilo podría mostrar tendencias similares en la mejora de la velocidad. Algunos han afirmado que esto es evidencia definitiva de la imagen no clásica. [43] Pero no todos están de acuerdo. Otros investigadores encontraron que los derivados de ciclopentano que eran estructuralmente similares al sistema norbornilo aún presentaban velocidades de reacción mejoradas, lo que los llevó a afirmar que el catión norbornilo clásico describe el sistema mucho mejor. [44] [45]

Los experimentos de etiquetado de isótopos radiactivos proporcionan una herramienta poderosa para determinar la estructura de las moléculas orgánicas. Al descomponer sistemáticamente el catión 2-norbornilo y analizar la cantidad de isótopo radiactivo en cada producto de descomposición, los investigadores pudieron mostrar más evidencia de la imagen no clásica de enlace deslocalizado ( ver Figura 9 ). Los defensores de la imagen no clásica esperarían que el 50% del CO 2 generado en la descomposición en la Figura 9 contenga 14 C, mientras que los defensores de la imagen clásica esperarían que más del CO 2 generado sea radiactivo debido a la naturaleza de vida corta del catión. Se ha observado que el 40% del dióxido de carbono producido a través de la descomposición es radiactivo, lo que sugiere que la imagen no clásica es más correcta. [12]
Es posible distinguir aún más entre las estructuras clásicas y no clásicas del catión 2-norbornilo combinando experimentos de RMN con experimentos de marcaje isotópico. La sustitución isotópica de uno de los dos átomos de deuterio por un átomo de hidrógeno hace que el entorno de los átomos cercanos activos en RMN cambie drásticamente. El marcaje isotópico asimétrico de deuterio (sustitución) hará que un conjunto de carbonos que eran todos equivalentes en las especies de hidrógeno se dividan en dos o más conjuntos de carbonos equivalentes en las especies marcadas con deutero; esto se manifestará en el espectro de RMN como un pico en el espectro de las especies de hidrógeno que se convierte en al menos dos picos "divididos" en las especies marcadas con deutero. Si un sistema está experimentando un equilibrio rápido a una velocidad más rápida que la escala de tiempo de un experimento de RMN de 13 C, el pico relevante se dividirá drásticamente (del orden de 10-100 ppm). Si, en cambio, el sistema es estático, el pico se dividirá muy poco. [46] [47] El espectro de RMN de 13 C del catión 2-norbornilo a -150 °C muestra que los picos correspondientes a los carbonos 1 y 2 se dividen en menos de 10 ppm (partes por millón) cuando se lleva a cabo este experimento, lo que indica que el sistema no está experimentando un equilibrio rápido como en la imagen clásica. [48]