La reacción de Heck-Matsuda (HM) es una reacción orgánica y un tipo de arilación de olefinas catalizada por paladio que utiliza sales de arenodiazonio como alternativa a los haluros de arilo y triflatos . [1] [2] [3]
El uso de sales de arenediazonio presenta algunas ventajas sobre los electrófilos de haluros de arilo tradicionales , por ejemplo, no se requiere el uso de fosfinas como ligando y, por lo tanto, se elimina el requisito de condiciones anaeróbicas, lo que hace que la reacción sea más práctica y fácil de manejar. Además, la reacción se puede realizar con o sin una base y, a menudo, es más rápida que los protocolos Heck tradicionales . [4] [2] [3]

Los alcoholes alílicos , los alquenos conjugados , los heterociclos insaturados y los alquenos no activados se pueden arilar con sales de arenediazonio utilizando catalizadores simples como acetato de paladio (Pd(OAc) 2 ) o tris(dibencilidenoacetona)dipaladio(0) (Pd 2 dba 3 ) a temperatura ambiente en el aire y en solventes benignos y convencionales. [1]
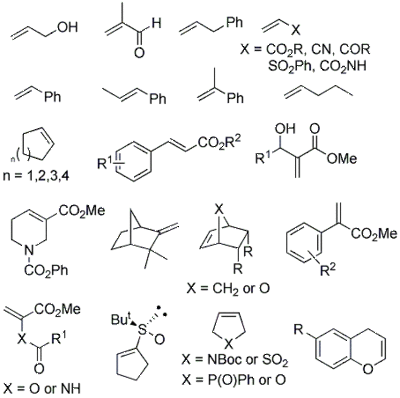
Además de la variante intermolecular de la reacción HM, también se han desarrollado procesos de ciclización intramolecular para la construcción de una gama de heterociclos de oxígeno y nitrógeno. [1]

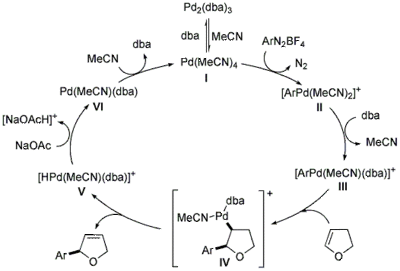
El ciclo catalítico de la reacción de arilación de Heck-Matsuda tiene cuatro pasos principales: adición oxidativa , inserción migratoria o carbopaladación, eliminación β de syn y eliminación reductora . El ciclo catalítico de Heck propuesto que involucra paladio catiónico con sales de diazonio fue reforzado por estudios con espectrometría de masas (ESI) por Correia y colaboradores. [1] Estos resultados también muestran las interacciones complejas que ocurren en la esfera de coordinación del paladio durante la reacción de Heck con la sal de arenodiazonio.
Una reacción relacionada es la arilación de Meerwein , que precede a la reacción de Heck. La arilación de Meerwein suele utilizar sales de cobre, pero en algunos casos puede realizarse sin un metal de transición.