La potencia celular es la capacidad de una célula para diferenciarse en otros tipos de células. [1] [2] Cuantos más tipos de células pueda diferenciarse una célula, mayor será su potencia. La potencia también se describe como el potencial de activación genética dentro de una célula, que como un continuo, comienza con la totipotencia para designar una célula con el mayor potencial de diferenciación, pluripotencia , multipotencia , oligopotencia y finalmente unipotencia .

La totipotencia (latín: totipotentia , literalmente 'capacidad para todas las [cosas]') es la capacidad de una sola célula para dividirse y producir todas las células diferenciadas de un organismo . Las esporas y los cigotos son ejemplos de células totipotentes. [3] En el espectro de potencia celular, la totipotencia representa la célula con mayor potencial de diferenciación , pudiendo diferenciarse en cualquier célula embrionaria , así como en cualquier célula de tejido extraembrionario . Por el contrario, las células pluripotentes sólo pueden diferenciarse en células embrionarias. [4] [5]
Una célula completamente diferenciada puede volver a un estado de totipotencia. [6] La conversión a totipotencia es compleja y no se comprende completamente. En 2011, una investigación reveló que las células pueden diferenciarse no en una célula completamente totipotente, sino en una "variación celular compleja" de totipotencia. [7] Las células madre que se asemejan a blastómeros totipotentes de embriones en etapa de 2 células pueden surgir espontáneamente en cultivos de células madre embrionarias de ratón [8] [9] y también pueden inducirse a surgir con mayor frecuencia in vitro mediante la regulación negativa de la actividad de ensamblaje de cromatina de CAF-1 . [10]
El modelo de desarrollo humano se puede utilizar para describir cómo surgen las células totipotentes. [11] El desarrollo humano comienza cuando un espermatozoide fertiliza un óvulo y el óvulo fertilizado resultante crea una única célula totipotente, un cigoto . [12] En las primeras horas después de la fertilización, este cigoto se divide en células totipotentes idénticas, que luego pueden desarrollarse en cualquiera de las tres capas germinales de un ser humano ( endodermo , mesodermo o ectodermo ), o en células de la placenta ( citotrofoblasto o sincitiotrofoblasto ). Después de alcanzar una etapa de 16 células, las células totipotentes de la mórula se diferencian en células que eventualmente se convertirán en la masa celular interna del blastocisto o en los trofoblastos externos . Aproximadamente cuatro días después de la fertilización y después de varios ciclos de división celular, estas células totipotentes comienzan a especializarse. La masa celular interna, fuente de células madre embrionarias , se vuelve pluripotente.
La investigación sobre Caenorhabditis elegans sugiere que múltiples mecanismos, incluida la regulación del ARN , pueden desempeñar un papel en el mantenimiento de la totipotencia en diferentes etapas de desarrollo en algunas especies. [13] El trabajo con peces cebra y mamíferos sugiere una mayor interacción entre los miARN y las proteínas de unión a ARN (RBP) para determinar las diferencias en el desarrollo. [14]
En las células germinales primordiales de ratón , la reprogramación de todo el genoma que conduce a la totipotencia implica el borrado de huellas epigenéticas . La reprogramación se ve facilitada por la desmetilación activa del ADN que involucra la vía enzimática de reparación por escisión de bases del ADN . [15] Esta vía implica la eliminación de la metilación de CpG (5mC) en células germinales primordiales mediante la conversión inicial de 5mC en 5-hidroximetilcitosina (5hmC), una reacción impulsada por altos niveles de las diez-once enzimas dioxigenasas TET-1 y TET-. 2 . [dieciséis]
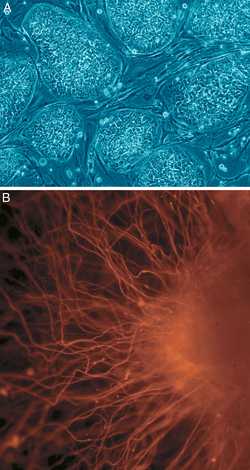
En biología celular, pluripotencia (latín: pluripotentia , literalmente 'capacidad para muchas [cosas]') [17] se refiere a una célula madre que tiene el potencial de diferenciarse en cualquiera de las tres capas germinales : endodermo (intestino, pulmones e hígado). ), mesodermo (músculo, esqueleto, sistema vascular sanguíneo, urogenital, dermis) o ectodermo (nervioso, sensorial, epidermis), pero no en tejidos extraembrionarios como la placenta o el saco vitelino. [18] Sin embargo, la pluripotencia celular es un continuo, que va desde la célula completamente pluripotente que puede formar cada célula del embrión propiamente dicha, por ejemplo, células madre embrionarias e iPSC, hasta la célula pluripotente parcial o incompleta que puede formar células de los tres embriones. capas, pero que pueden no exhibir todas las características de células completamente pluripotentes.
Las células madre pluripotentes inducidas, comúnmente abreviadas como células iPS o iPSC, son un tipo de células madre pluripotentes derivadas artificialmente de una célula no pluripotente, típicamente una célula somática adulta , mediante la inducción de una expresión "forzada" de ciertos genes y factores de transcripción . [19] Estos factores de transcripción desempeñan un papel clave en la determinación del estado de estas células y también resalta el hecho de que estas células somáticas conservan la misma información genética que las células embrionarias tempranas. [20] La capacidad de inducir células a un estado pluripotente fue iniciada inicialmente en 2006 utilizando fibroblastos de ratón y cuatro factores de transcripción, Oct4 , Sox2 , Klf4 y c- Myc ; [21] Esta técnica, llamada reprogramación , le valió más tarde a Shinya Yamanaka y John Gurdon el Premio Nobel de Fisiología o Medicina. [22] A esto le siguió en 2007 la inducción exitosa de iPSC humanas derivadas de fibroblastos dérmicos humanos utilizando métodos similares a los utilizados para la inducción de células de ratón. [23] Estas células inducidas exhiben rasgos similares a los de las células madre embrionarias (ESC), pero no requieren el uso de embriones. Algunas de las similitudes entre las ESC y las iPSC incluyen la pluripotencia, la morfología , la capacidad de autorrenovación, un rasgo que implica que pueden dividirse y replicarse indefinidamente, y la expresión genética . [24]
También se cree que los factores epigenéticos están involucrados en la reprogramación real de las células somáticas para inducir la pluripotencia. Se ha teorizado que ciertos factores epigenéticos podrían funcionar para eliminar las marcas epigenéticas somáticas originales con el fin de adquirir nuevas marcas epigenéticas que son parte del logro de un estado pluripotente. La cromatina también se reorganiza en las iPSC y se vuelve similar a la que se encuentra en las ESC en el sentido de que está menos condensada y, por lo tanto, más accesible. Las modificaciones de eucromatina también son comunes, lo que también es consistente con el estado de eucromatina que se encuentra en las ESC. [24]
Debido a su gran similitud con las ESC, las comunidades médica y de investigación están interesadas en las iPSC. Las iPSC podrían tener potencialmente las mismas implicaciones y aplicaciones terapéuticas que las CME, pero sin el controvertido uso de embriones en el proceso, un tema de gran debate bioético. La pluripotencia inducida de células somáticas en células iPS indiferenciadas fue aclamada originalmente como el fin del controvertido uso de células madre embrionarias . Sin embargo, se descubrió que las iPSC eran potencialmente tumorigénicas y, a pesar de los avances, [19] nunca fueron aprobadas para investigación en etapa clínica en los Estados Unidos hasta hace poco. Actualmente, las células progenitoras dopaminérgicas autólogas derivadas de iPSC se utilizan en ensayos para el tratamiento de la enfermedad de Parkinson. [25] También se han encontrado contratiempos como bajas tasas de replicación y senescencia temprana al fabricar iPSC, [26] lo que dificulta su uso como reemplazos de ESC.
La expresión somática de factores de transcripción combinados puede inducir directamente otros destinos celulares somáticos definidos ( transdiferenciación ); Los investigadores identificaron tres factores de transcripción específicos del linaje neuronal que podrían convertir directamente los fibroblastos (células del tejido conectivo) de ratón en neuronas completamente funcionales . [27] Este resultado desafía la naturaleza terminal de la diferenciación celular y la integridad del compromiso del linaje; e implica que con las herramientas adecuadas, todas las células son totipotentes y pueden formar todo tipo de tejidos.
Algunos de los posibles usos médicos y terapéuticos de las iPSC derivadas de pacientes incluyen su uso en trasplantes de células y tejidos sin el riesgo de rechazo que se encuentra comúnmente. Las iPSC pueden potencialmente reemplazar los modelos animales inadecuados, así como los modelos in vitro utilizados para la investigación de enfermedades. [28]

Los hallazgos con respecto a los epiblastos antes y después de la implantación han generado propuestas para clasificar la pluripotencia en dos estados: "ingenuo" y "preparado", que representan el epiblasto previo y posterior a la implantación, respectivamente. [29] El continuo de ingenuo a cebado se controla mediante la reducción de la dimerización de Sox2/Oct4 en los elementos de ADN de SoxOct que controlan la pluripotencia ingenua. [30] Las células madre pluripotentes preparadas de diferentes especies podrían restablecerse al estado ingenuo usando un cóctel que contiene Klf4 y Sox2 o "super-Sox", un factor de transcripción quimérico con capacidad mejorada para dimerizar con Oct4. [30]
Las células madre de referencia comúnmente utilizadas en la ciencia, denominadas células madre embrionarias (ESC), se derivan de un epiblasto previo a la implantación; dicho epiblasto puede generar el feto completo, y una célula de epiblasto puede contribuir a todos los linajes celulares si se inyecta en otro blastocisto. Por otro lado, se pueden observar varias diferencias marcadas entre los epiblastos previos y posteriores a la implantación, como su diferencia en la morfología, en la que el epiblasto después de la implantación cambia su morfología a una forma de copa llamada "cilindro de óvulo". así como la alteración cromosómica en la que uno de los cromosomas X se inactiva aleatoriamente en la etapa inicial del cilindro del óvulo, conocida como inactivación X. [31] Durante este desarrollo, las células del epiblasto del cilindro del óvulo son atacadas sistemáticamente por factores de crecimiento de fibroblastos , señalización Wnt y otros factores inductivos a través del saco vitelino circundante y el tejido del trofoblasto, [32] de modo que se vuelven instructivamente específicos de acuerdo con el espacio. organización. [33]
Otra diferencia importante es que las células madre del epiblasto postimplantación no pueden contribuir a las quimeras del blastocisto , [34] lo que las distingue de otras células madre pluripotentes conocidas. Las líneas celulares derivadas de dichos epiblastos posteriores a la implantación se denominan células madre derivadas de epiblastos , que se derivaron por primera vez en laboratorio en 2007. Tanto las ESC como las EpiSC se derivan de epiblastos, pero en diferentes fases de desarrollo. La pluripotencia aún está intacta en el epiblasto posterior a la implantación, como lo demuestra la expresión conservada de Nanog , Fut4 y Oct-4 en EpiSC, [35] hasta la somitogénesis y puede revertirse a mitad de camino de la expresión inducida de Oct-4 . [36]
_Ranunculus_asiaticus_-_example_of_Totipotency.jpg/440px-(MHNT)_Ranunculus_asiaticus_-_example_of_Totipotency.jpg)
Se ha observado pluripotencia no inducida en cultivos de tejidos de meristemas de raíces, especialmente por Kareem et al 2015, Kim et al 2018 y Rosspopoff et al 2017. Esta pluripotencia está regulada por varios reguladores, incluidos PLETHORA 1 y PLETHORA 2 ; y PLETORA 3 , PLETORA 5 y PLETORA 7 , cuya expresión, según Kareem, estaba provocada por auxinas . (Estos también se conocen como PLT1, PLT2, PLT3, PLT5, PLT7 y se expresan mediante genes del mismo nombre). A partir de 2019, [actualizar]se espera que esto abra futuras investigaciones sobre la pluripotencia en los tejidos de las raíces. [37]

La multipotencia se produce cuando las células progenitoras tienen el potencial de activación genética para diferenciarse en tipos de células discretas. Por ejemplo, una célula madre hematopoyética, y este tipo de célula puede diferenciarse en varios tipos de células sanguíneas como linfocitos , monocitos , neutrófilos , etc., pero todavía es ambiguo si las HSC poseen la capacidad de diferenciarse en células cerebrales , células óseas o otros tipos de células no sanguíneas. [ cita necesaria ]
La investigación relacionada con células multipotentes sugiere que las células multipotentes pueden ser capaces de convertirse en tipos de células no relacionadas. En otro caso, las células madre de la sangre del cordón umbilical humano se convirtieron en neuronas humanas. [38] También hay investigaciones sobre la conversión de células multipotentes en células pluripotentes. [39]
Las células multipotentes se encuentran en muchos tipos de células humanas, pero no en todos. Se han encontrado células multipotentes en la sangre del cordón umbilical , [40] tejido adiposo, [41] células cardíacas, [42] médula ósea y células madre mesenquimales (MSC) que se encuentran en el tercer molar . [43]
Las MSC pueden resultar una fuente valiosa de células madre de los molares entre los 8 y 10 años de edad, antes de la calcificación dental en adultos. Las MSC pueden diferenciarse en osteoblastos, condrocitos y adipocitos. [44]
En biología, la oligopotencia es la capacidad de las células progenitoras de diferenciarse en unos pocos tipos de células . Es un grado de potencia . Ejemplos de células madre oligopotentes son las células madre linfoides o mieloides. [2] Una célula linfoide específicamente puede dar origen a varias células sanguíneas, como las células B y T, pero no a un tipo de célula sanguínea diferente, como un glóbulo rojo. [45] Ejemplos de células progenitoras son las células madre vasculares que tienen la capacidad de convertirse en células endoteliales o de músculo liso.
En biología celular , una célula unipotente es el concepto de que una célula madre tiene la capacidad de diferenciarse en un solo tipo de célula. [46] Actualmente no está claro si existen verdaderas células madre unipotentes. Los hepatoblastos, que se diferencian en hepatocitos (que constituyen la mayor parte del hígado ) o colangiocitos (células epiteliales del conducto biliar), son bipotentes. [47] Un sinónimo cercano de célula unipotente es célula precursora .