
Un nucleótido cíclico (cNMP) es un nucleótido de fosfato simple con una disposición de enlace cíclico entre los grupos azúcar y fosfato. Al igual que otros nucleótidos, los nucleótidos cíclicos están compuestos por tres grupos funcionales: un azúcar, una base nitrogenada y un solo grupo fosfato. Como se puede ver en las imágenes del monofosfato de adenosina cíclico (cAMP) y el monofosfato de guanosina cíclico (cGMP), la parte "cíclica" consiste en dos enlaces entre el grupo fosfato y los grupos hidroxilo 3' y 5' del azúcar, muy a menudo una ribosa .
Su importancia biológica incluye una amplia gama de interacciones proteína - ligando . Se han identificado como mensajeros secundarios tanto en la señalización hormonal como en la señalización de canales iónicos en células eucariotas , así como compuestos efectores alostéricos de proteínas de unión al ADN en células procariotas . El AMPc y el GMPc son actualmente los nucleótidos cíclicos mejor documentados, sin embargo, hay evidencia de que el CMPc (con citosina ) también está involucrado en la mensajería celular eucariota. El papel del monofosfato de uridina cíclico (cUMP) es aún menos conocido.
El descubrimiento de los nucleótidos cíclicos ha contribuido en gran medida a la comprensión de los mecanismos de las quinasas y las fosfatasas , así como de la regulación de las proteínas en general. Aunque han pasado más de 50 años desde su descubrimiento inicial, el interés por los nucleótidos cíclicos y su importancia bioquímica y fisiológica continúa.
La comprensión del concepto de segundos mensajeros, y en particular el papel de los nucleótidos cíclicos y su capacidad para transmitir señales fisiológicas a una célula , tiene sus orígenes en la investigación del metabolismo del glucógeno por Carl y Gerty Cori , por la que fueron galardonados con un Premio Nobel de Fisiología o Medicina en 1947. [1] Una serie de descubrimientos incrementales pero importantes a lo largo de la década de 1950 se sumaron a su investigación, centrándose principalmente en la actividad de la glucógeno fosforilasa en el hígado del perro . La glucógeno fosforilasa cataliza el primer paso de la glucogenólisis , el proceso de descomposición del glucógeno en sus partes sustituyentes de glucosa . [2] Earl Sutherland investigó el efecto de las hormonas adrenalina y glucagón sobre la glucógeno fosforilasa, lo que le valió el Premio Nobel de Fisiología o Medicina en 1971. [1]
En 1956, Edwin Krebs y Edmond Fischer descubrieron que el trifosfato de adenosina (ATP) es necesario para la conversión de la glucógeno fosforilasa b en glucógeno fosforilasa a. Al año siguiente, mientras investigaban la acción de la adrenalina sobre la glucogenólisis , Sutherland y Walter Wosilait informaron que se libera fosfato inorgánico cuando se inactiva la enzima fosforilasa hepática; pero cuando se activa, incorpora un fosfato. [1] El “factor activo” que producían las hormonas [2] fue finalmente purificado en 1958, y luego se identificó que contenía una ribosa , un fosfato y una adenina en proporciones iguales. Además, se demostró que este factor se revertía a 5'-AMP cuando se inactivaba. [1]
Evgeny Fesenko, Stanislav Kolesnikov y Arkady Lyubarsky descubrieron en 1985 que el monofosfato de guanosina cíclico (cGMP) puede iniciar la fotorrespuesta en los bastones . Poco después, Tadashi Nakamura y Geoffrey Gold informaron sobre el papel del cNMP en los canales iónicos controlados de los cilios quimiosensibles de las neuronas sensoriales olfativas . En 1992, Lawrence Haynes y King-Wai Yau descubrieron el papel del cNMP en el canal controlado por nucleótidos cíclicos dependiente de la luz de los fotorreceptores de los conos . [3] A finales de la década, se comprendió la presencia de dos tipos de receptores intramembrana: Rs (que estimula la ciclasa ) y Ri (que inhibe la ciclasa). Wei-Jen Tang y James Hurley informaron en 1998 que la adenilil ciclasa, que sintetiza AMPc, está regulada no sólo por hormonas y neurotransmisores , sino también por la fosforilación , el calcio , la forskolina y las proteínas de unión al nucleótido de guanina ( proteínas G ). [2]
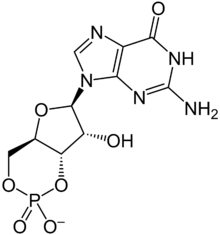
Los dos nucleótidos cíclicos mejor estudiados son el AMP cíclico (cAMP) y el GMP cíclico (cGMP), mientras que el CMP cíclico (cCMP) y el UMP cíclico (cUMP) son menos conocidos. El cAMP es el monofosfato de adenosina cíclico 3'5', el cGMP es el monofosfato de guanosina cíclico 3'5', el cCMP es el monofosfato de citidina 3',5' y el cUMP es el fosfato cíclico 3',5' de uridina. [4] [5]
Cada nucleótido cíclico tiene tres componentes. Contiene una base nitrogenada (es decir, contiene nitrógeno): por ejemplo, adenina en cAMP y guanina en cGMP. También contiene un azúcar, específicamente la ribosa de cinco carbonos . Y, por último, un nucleótido cíclico contiene un fosfato. Una purina de doble anillo es la base nitrogenada para cAMP y cGMP, mientras que la citosina, la timina y el uracilo tienen cada uno una base nitrogenada de un solo anillo ( pirimidina ).
Estos tres componentes están conectados de manera que la base nitrogenada está unida al primer carbono de la ribosa (carbono 1') y el grupo fosfato está unido al carbono 5' de la ribosa. Si bien todos los nucleótidos tienen esta estructura, el grupo fosfato hace una segunda conexión con el anillo de ribosa en el carbono 3' en los nucleótidos cíclicos. Debido a que el grupo fosfato tiene dos enlaces separados con el azúcar ribosa, forma un anillo cíclico. [6]
La convención de numeración de átomos se utiliza para identificar los carbonos y nitrógenos dentro de un nucleótido cíclico. En la pentosa, el carbono más cercano al grupo carbonilo está etiquetado como C-1. Cuando una pentosa está conectada a una base nitrogenada, la numeración de los átomos de carbono se distingue con una notación prima ('), que diferencia estos carbonos de la numeración de los átomos de la base nitrogenada. [7]
Por lo tanto, para el AMPc, el monofosfato de adenosina cíclico 3'5' indica que un solo grupo fosfato forma una estructura cíclica con el grupo ribosa en sus carbonos 3' y 5', mientras que el grupo ribosa también está unido a la adenosina (se entiende que este enlace está en la posición 1' de la ribosa).
Los nucleótidos cíclicos se encuentran tanto en células procariotas como eucariotas. El control de las concentraciones intracelulares se mantiene mediante una serie de reacciones enzimáticas en las que participan varias familias de proteínas. En los mamíferos de orden superior, los cNMP están presentes en muchos tipos de tejidos.

Los nucleótidos cíclicos se producen a partir de la reacción genérica NTP → cNMP + PP i , [8] donde N representa una base nitrogenada. La reacción es catalizada por nucleotidil ciclasas específicas, de modo que la producción de AMPc es catalizada por la adenilil ciclasa y la producción de GMPc es catalizada por la guanilil ciclasa . [2] La adenilil ciclasa se ha encontrado tanto en forma transmembrana como citosólica , representando distintas clases de proteínas y diferentes fuentes de AMPc. [9]

Tanto el AMPc como el GMPc se degradan por hidrólisis del enlace fosfodiéster 3' , lo que da como resultado un NMP 5'. La degradación se lleva a cabo principalmente por una clase de enzimas conocidas como fosfodiesterasas (PDE). En las células de mamíferos, existen 11 familias de PDE conocidas con diferentes isoformas de cada proteína expresadas en función de las necesidades regulatorias de la célula. Algunas fosfodiesterasas son específicas del NMPc, mientras que otras pueden hidrolizar de forma no específica. [10] Sin embargo, las vías de degradación del AMPc y el GMPc se comprenden mucho mejor que las del CMPc o el CUMPc. La identificación de PDE específicas para el CMPc y el CUMPc no se ha establecido tan a fondo. [11]
Los nucleótidos cíclicos se pueden encontrar en muchos tipos diferentes de células eucariotas, incluyendo bastones y conos fotorreceptores, células musculares lisas y células hepáticas . Las concentraciones celulares de nucleótidos cíclicos pueden ser muy bajas, en el rango de 10 −7 M , porque el metabolismo y la función a menudo se localizan en partes particulares de la célula. [1] Un dominio de unión a nucleótidos cíclicos (CNB) altamente conservado está presente en todas las proteínas que se unen a cNMP, independientemente de su función biológica. El dominio consiste en una arquitectura de sándwich beta, con el bolsillo de unión de nucleótidos cíclicos entre las láminas beta . La unión de cNMP causa un cambio conformacional que afecta la actividad de la proteína. [12] También hay datos que respaldan un efecto de unión sinérgico entre múltiples nucleótidos cíclicos, con cCMP reduciendo la concentración efectiva (EC 50 ) de cAMP para la activación de la proteína quinasa A (PKA). [13]
Los nucleótidos cíclicos son parte integral de un sistema de comunicación que actúa dentro de las células. [1] Actúan como "segundos mensajeros" al transmitir las señales de muchos primeros mensajeros, como hormonas y neurotransmisores, a sus destinos fisiológicos. Los nucleótidos cíclicos participan en muchas respuestas fisiológicas, [14] incluyendo el acoplamiento receptor-efector, la regulación negativa de la respuesta a fármacos, las cascadas de proteína-quinasa y la transducción de señales transmembrana. [1]
Los nucleótidos cíclicos actúan como segundos mensajeros cuando los primeros mensajeros, que no pueden entrar en la célula, se unen a receptores en la membrana celular. El receptor cambia de conformación y transmite una señal que activa una enzima en el interior de la membrana celular llamada adenilil ciclasa. Esto libera AMPc en el interior de la célula, donde estimula una proteína quinasa llamada proteína quinasa dependiente de AMP cíclico. Al fosforilar proteínas, la proteína quinasa dependiente de AMP cíclico altera la actividad de la proteína. El papel del AMPc en este proceso termina con la hidrólisis a AMP por la fosfodiesterasa. [2]
Los nucleótidos cíclicos son adecuados para actuar como segundos mensajeros por varias razones. Su síntesis es favorable desde el punto de vista energético y se derivan de componentes metabólicos comunes (ATP y GTP). Cuando se descomponen en AMP/GMP y fosfato inorgánico, estos componentes no son tóxicos. [14] Por último, los nucleótidos cíclicos se pueden distinguir de los nucleótidos no cíclicos porque son más pequeños y menos polares . [2]
La participación de los nucleótidos cíclicos en las funciones biológicas es variada, mientras que la comprensión de su papel continúa creciendo. Hay varios ejemplos de su influencia biológica. Están asociados con la memoria a largo y corto plazo. [20] También trabajan en el hígado para coordinar varias enzimas que controlan la glucosa en sangre y otros nutrientes . [21] En las bacterias , los nucleótidos cíclicos se unen a la proteína activadora del gen catabolito (CAP), que actúa para aumentar la actividad enzimática metabólica al aumentar la tasa de transcripción del ADN . [5] También facilitan la relajación de las células del músculo liso en el tejido vascular , [22] y activan los canales cíclicos de CNG en los fotorreceptores de la retina y las neuronas sensoriales olfativas . Además, activan potencialmente los canales cíclicos de CNG en: la sensibilidad a la luz de la glándula pineal , las neuronas sensoriales del órgano vomeronasal (que participa en la detección de feromonas ), las células receptoras del gusto , la señalización celular en los espermatozoides , las células epiteliales de las vías respiratorias , la línea celular neuronal secretora de la hormona liberadora de gonadotropina (GnRH) y el conducto colector medular interno renal . [3]
Entre los ejemplos de alteraciones de las vías de cNMP se incluyen: las mutaciones en los genes del canal CNG se asocian con la degeneración de la retina y con el daltonismo [3] y la sobreexpresión de la adenilil ciclasa citosólica o soluble (sAC) se ha relacionado con el carcinoma de próstata humano . Se ha demostrado que la inhibición de la sAC, o su inactivación mediante la transfección por interferencia de ARN (RNAi), previene la proliferación de las células del carcinoma de próstata. La vía reguladora parece ser parte de la vía EPAC y no de la vía PKA [9] .
Las fosfodiesterasas, reguladoras principales de la degradación de cNMP, suelen ser el objetivo de los tratamientos. La cafeína es un inhibidor conocido de la PDE, mientras que los fármacos utilizados para el tratamiento de la disfunción eréctil, como el sildenafil y el tadalafil, también actúan inhibiendo la actividad de las fosfodiesterasas. [10]
{{cite journal}}: CS1 maint: varios nombres: lista de autores ( enlace )