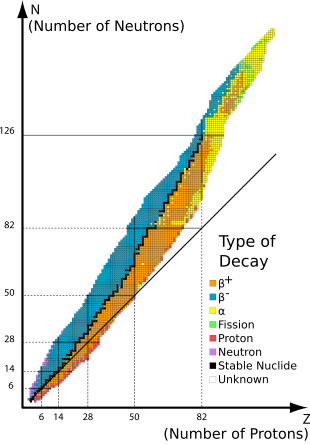
Los nucleidos estables son nucleidos que no son radiactivos y por lo tanto (a diferencia de los radionucleidos ) no sufren desintegración radiactiva espontáneamente . [1] Cuando se hace referencia a dichos nucleidos en relación con elementos específicos, generalmente se les denomina isótopos estables .
Los 80 elementos con uno o más isótopos estables comprenden un total de 251 nucleidos que no se sabe que se descompongan con los equipos actuales (consulte la lista al final de este artículo). De estos 80 elementos, 26 tienen un solo isótopo estable; por eso se les denomina monoisotópicos . El resto tiene más de un isótopo estable. El estaño tiene diez isótopos estables, el mayor número de isótopos estables conocido para un elemento.
La mayoría de los nucleidos naturales son estables (alrededor de 251; consulte la lista al final de este artículo), y se sabe que alrededor de 35 más (un total de 286) son radiactivos con vidas medias (también conocidas) lo suficientemente largas como para ocurrir primordialmente. Si la vida media de un nucleido es comparable o superior a la edad de la Tierra (4.500 millones de años), una cantidad significativa habrá sobrevivido desde la formación del Sistema Solar , y entonces se dice que es primordial . Entonces contribuirá de esa manera a la composición isotópica natural de un elemento químico. Los radioisótopos presentes primordialmente se detectan fácilmente con vidas medias tan cortas como 700 millones de años (p. ej., 235 U ). Este es el límite actual de detección, [ cita necesaria ] ya que los nucleidos de vida más corta aún no se han detectado de manera indiscutible en la naturaleza, excepto cuando se produjeron recientemente, como productos de desintegración o espalación de rayos cósmicos.
Muchos radioisótopos naturales (otros 53 aproximadamente, para un total de unos 339) exhiben vidas medias aún más cortas que 700 millones de años, pero se fabrican recientemente, como productos hijos de procesos de desintegración de nucleidos primordiales (por ejemplo, el radio del uranio). ) o de reacciones energéticas en curso, como los nucleidos cosmogénicos producidos por el actual bombardeo de la Tierra por rayos cósmicos (por ejemplo, 14 C elaborado a partir de nitrógeno).
Se predice que algunos isótopos clasificados como estables (es decir, no se ha observado radiactividad en ellos) tendrán vidas medias extremadamente largas (a veces hasta de 10 a 18 años o más). [2] Si la vida media prevista cae dentro de un rango experimentalmente accesible, dichos isótopos tienen la posibilidad de pasar de la lista de nucleidos estables a la categoría radiactiva, una vez que se observa su actividad. Por ejemplo, 209 Bi y 180 W se clasificaban anteriormente como estables, pero en 2003 se descubrió que eran alfa -activos. Sin embargo, estos nucleidos no cambian su estatus de primordiales cuando se determina que son radiactivos.
Se cree que la mayoría de los isótopos estables de la Tierra se formaron en procesos de nucleosíntesis , ya sea en el Big Bang , o en generaciones de estrellas que precedieron a la formación del Sistema Solar . Sin embargo, algunos isótopos estables también muestran variaciones de abundancia en la Tierra como resultado de la desintegración de nucleidos radiactivos de larga vida. Estos productos de desintegración se denominan isótopos radiogénicos para distinguirlos del grupo mucho más amplio de isótopos "no radiogénicos".
De los elementos químicos conocidos, 80 elementos tienen al menos un nucleido estable. Estos comprenden los primeros 82 elementos, desde el hidrógeno hasta el plomo , con las dos excepciones, el tecnecio (elemento 43) y el prometio (elemento 61), que no tienen ningún nucleido estable. En 2023, había un total de 251 nucleidos "estables" conocidos. En esta definición, "estable" significa un nucleido del que nunca se ha observado que se desintegre en condiciones naturales. Por lo tanto, estos elementos tienen vidas medias demasiado largas para poder medirlas por cualquier medio, directo o indirecto.
Isótopos estables:
Estos últimos 26 se denominan así elementos monoisotópicos . [3] El número medio de isótopos estables para elementos que tienen al menos un isótopo estable es 251/80 = 3,1375.
La estabilidad de los isótopos se ve influenciada por la proporción entre protones y neutrones, así como por la presencia de ciertos números mágicos de neutrones o protones que representan capas cuánticas cerradas y llenas. Estas capas cuánticas corresponden a un conjunto de niveles de energía dentro del modelo de capa del núcleo; Las capas llenas, como la capa llena de 50 protones del estaño, confieren una estabilidad inusual al nucleido. Como en el caso del estaño, un número mágico para Z , el número atómico, tiende a aumentar el número de isótopos estables del elemento.
Al igual que en el caso de los electrones, que tienen el estado de energía más bajo cuando se encuentran en pares en un orbital determinado, los nucleones (tanto protones como neutrones) exhiben un estado de energía más bajo cuando su número es par, en lugar de impar. Esta estabilidad tiende a evitar la desintegración beta (en dos pasos) de muchos nucleidos pares-pares en otro nucleido par-par del mismo número másico pero de menor energía (y por supuesto con dos protones más y dos neutrones menos), porque la desintegración que ocurre uno paso a paso tendría que pasar a través de un nucleido impar de mayor energía. Por lo tanto, dichos núcleos sufren una doble desintegración beta (o se teoriza que lo hacen) con vidas medias varios órdenes de magnitud mayores que la edad del universo . Esto genera un mayor número de nucleidos pares estables, que representan 150 del total de 251. Los nucleidos pares estables suman hasta tres isobaras para algunos números másicos y hasta siete isótopos para algunos números atómicos.
Por el contrario, de los 251 nucleidos estables conocidos, sólo cinco tienen un número impar de protones y un número impar de neutrones: hidrógeno-2 ( deuterio ), litio-6 , boro-10 , nitrógeno-14 y tantalio-180m . Además, sólo cuatro nucleidos radiactivos extraños e impares de origen natural tienen una vida media de más de mil millones de años: potasio-40 , vanadio-50 , lantano-138 y lutecio-176 . Los nucleidos primordiales impares son raros porque la mayoría de los núcleos impares son inestables con respecto a la desintegración beta , porque los productos de la desintegración son pares-pares y, por lo tanto, están más fuertemente unidos debido a los efectos del apareamiento nuclear . [4]
Otro efecto más de la inestabilidad de un número impar de cualquier tipo de nucleones es que los elementos impares tienden a tener menos isótopos estables. De los 26 elementos monoisotópicos (aquellos que tienen un solo isótopo estable), todos menos uno tienen un número atómico impar y todos menos uno tienen un número par de neutrones; la única excepción a ambas reglas es el berilio.
El fin de los elementos estables de la tabla periódica se produce después del plomo , en gran parte debido a que los núcleos con 128 neutrones (dos neutrones por encima del número mágico 126) son extraordinariamente inestables y casi de inmediato desprenden partículas alfa. [5] Esto también contribuye a las vidas medias muy cortas del astato , el radón y el francio en relación con elementos más pesados. Un fenómeno similar ocurre, en mucha menor medida, con 84 neutrones (dos neutrones por encima del número mágico 82), donde varios isótopos de elementos de la serie de los lantánidos exhiben desintegración alfa.
El recuento de 251 nucleidos estables conocidos incluye el tantalio-180m, ya que aunque su desintegración e inestabilidad está automáticamente implicada por su notación de "metaestable", esto aún no se ha observado. Todos los isótopos "estables" (estables por observación, no por teoría) son los estados fundamentales de los núcleos, con la excepción del tantalio-180m, que es un isómero nuclear o estado excitado. El estado fundamental de este núcleo en particular, tantalio-180, es radiactivo con una vida media comparativamente corta de 8 horas; por el contrario, la desintegración del isómero nuclear excitado está extremadamente prohibida por las reglas de selección de paridad de espín. Se ha informado experimentalmente mediante observación directa que la vida media de 180m Ta hasta la desintegración gamma debe ser de más de 10 a 15 años. Tampoco se han observado nunca otros modos posibles de desintegración de 180 m Ta (desintegración beta, captura de electrones y desintegración alfa).
Se espera que una mejora continua de la sensibilidad experimental permita descubrir una radiactividad muy leve (inestabilidad) de algunos isótopos que hoy se consideran estables. Por ejemplo, en 2003 se informó que el bismuto-209 (el único isótopo primordial del bismuto) es muy levemente radiactivo, con un tiempo de vida media de (1,9 ± 0,2) × 10 19 años, [6] [7], lo que confirma Predicciones teóricas [8] de la física nuclear de que el bismuto-209 se desintegraría muy lentamente por emisión alfa .
Los isótopos que teóricamente se cree que son inestables pero que no se ha observado que se desintegren se denominan observacionalmente estables . Actualmente existen 105 isótopos "estables" teóricamente inestables, de los cuales 40 han sido observados en detalle sin signos de desintegración, siendo el más ligero el 36 Ar. Muchos nucleidos "estables" son " metaestables ", ya que liberarían energía si ocurriera una desintegración radiactiva [9] y, de hecho, se espera que experimenten tipos muy raros de desintegración radiactiva , incluida la emisión doble beta .
146 nucleidos de 62 elementos con números atómicos del 1 ( hidrógeno ) al 66 ( disprosio ), excepto 43 ( tecnecio ), 61 ( prometio ), 62 ( samario ) y 63 ( europio ), son teóricamente estables ante cualquier tipo de desintegración nuclear, excepto para la posibilidad teórica de la desintegración de protones , que nunca se ha observado a pesar de extensas búsquedas, y la fisión espontánea , que es teóricamente posible para los nucleidos con números de masa atómica ≥ 93. [10]
Para procesos distintos de la fisión espontánea, otras rutas teóricas de desintegración para elementos más pesados incluyen: [10]
Estos incluyen todos los nucleidos de masa 165 y mayor. Argón-36 es actualmente el nucleido "estable" más ligero conocido y, en teoría, inestable. [10]
La positividad de la liberación de energía en estos procesos significa que se permiten cinemáticamente (no violan la conservación de la energía) y, por lo tanto, en principio, pueden ocurrir. [10] No se observan debido a una supresión fuerte pero no absoluta, por reglas de selección de paridad de espín (para desintegraciones beta y transiciones isoméricas) o por el espesor de la barrera de potencial (para desintegraciones alfa y de cúmulos y fisión espontánea).
Esta es una tabla resumen de la Lista de nucleidos . Tenga en cuenta que las cifras no son exactas y pueden cambiar ligeramente en el futuro, a medida que se observe que los nucleidos son radiactivos o se determinen nuevas vidas medias con cierta precisión.
Los radionucleidos primordiales se han incluido a modo de comparación; están en cursiva y apartados de la lista de nucleidos estables propiamente dicha.
Abreviaturas de deterioro no observado previsto: [12] [2] [11]
A para desintegración alfa, B para desintegración beta, 2B para desintegración beta doble, E para captura de electrones, 2E para captura de electrones doble, IT para transición isomérica, SF para fisión espontánea, * para los nucleidos cuyas vidas medias tienen un límite inferior. La desintegración beta doble solo se ha incluido cuando la desintegración beta tampoco es posible.
^ El tantalio-180m es un "isótopo metaestable", lo que significa que es un isómero nuclear excitado del tantalio-180. Véase isótopos de tantalio . Sin embargo, la vida media de este isómero nuclear es tan larga que nunca se ha observado que se desintegre y, por lo tanto, se presenta como un nucleido primordial "observacionalmente no radiactivo" , como un isótopo menor de tantalio. Este es el único caso de un isómero nuclear que tiene una vida media tan larga que nunca se ha observado que se desintegre. Por tanto, está incluido en esta lista.
^^ Durante mucho tiempo se creyó que el bismuto-209 era estable, debido a su vida media de 2,01 · 10 19 años, que es más de mil millones de veces la edad del universo.
§ El europio-151 y el samario-147 son nucleidos primordiales con vidas medias muy largas de 4,62 · 10 18 años y 1,066 · 10 11 años, respectivamente.