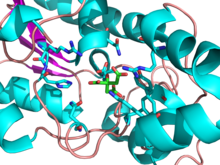
La fosfoglicerato mutasa (PGM) es cualquier enzima que cataliza el paso 8 de la glucólisis : la transferencia interna de un grupo fosfato de C-3 a C-2 que da como resultado la conversión de 3-fosfoglicerato (3PG) en 2-fosfoglicerato (2PG) a través de un intermedio de 2,3-bisfosfoglicerato. Estas enzimas se clasifican en dos clases distintas: dependientes de cofactor (dPGM) o independientes de cofactor (iPGM). [1] La enzima dPGM ( EC 5.4.2.11) está compuesta de aproximadamente 250 aminoácidos y se encuentra en todos los vertebrados, así como en algunos invertebrados, hongos y bacterias. La clase iPGM ( EC 5.4.2.12) se encuentra en todas las plantas y algas, así como en algunos invertebrados, hongos y bacterias grampositivas. [2] Esta clase de enzima PGM comparte la misma superfamilia que la fosfatasa alcalina . [3]
PGM es una enzima isomerasa que transfiere efectivamente un grupo fosfato (PO 4 3− ) desde el carbono C-3 del 3-fosfoglicerato al carbono C-2 formando el 2-fosfoglicerato . Hay un total de tres reacciones que dPGM puede catalizar: una reacción de mutasa que resulta en la conversión de 3PG a 2PG y viceversa, [4] [5] una reacción de fosfatasa que crea fosfoglicerato a partir de 2,3-bisfosfoglicerato, [6] [7] y una reacción de sintasa que produce 2,3-bisfosfoglicerato a partir de 1,3-bisfosfoglicerato similar a la enzima bifosfoglicerato mutasa [ cita requerida ] . Los estudios cinéticos y estructurales han proporcionado evidencia que indica que la dPGM y la bifosfoglicerato mutasa son estructuras parálogas . [6] Ambas enzimas están contenidas en la superfamilia que también contiene la porción fosfatasa de la fosfofructoquinasa 2 y la fosfatasa ácida prostática . [8]
La reacción de mutasa catalizada implica dos grupos fosforilo separados y el fosfato final en el carbono 2 no es el mismo fosfato eliminado del carbono 3. En el estado inicial de la enzima
dependiente de cofactor , el sitio activo contiene un complejo de fosfohistidina formado por la fosforilación de un residuo de histidina específico . [9] Cuando el 3-fosfoglicerato ingresa al sitio activo , el complejo de fosfohistidina se coloca para facilitar la transferencia de fosfato de la enzima al sustrato C-2, creando un intermedio de 2,3-bisfosfoglicerato . La desfosforilación de la enzima histidina activa un cambio alostérico local en la configuración de la enzima que ahora alinea el grupo fosfato 3-C del sustrato con el sitio activo de la enzima histidina y facilita la transferencia de fosfato, devolviendo la enzima a su estado fosforilado inicial y liberando el producto 2-fosfoglicerato . Se requiere 2,3-bisfosfoglicerato como cofactor para dPGM. Por el contrario, la clase iPGM es independiente del 2,3-bisfosfoglicerato y cataliza la transferencia intramolecular del grupo fosfato en monofosfogliceratos utilizando un intermediario fosfoserina. [10]
3PG + P-Enzima → 2,3BPG + Enzima → 2PG + P-Enzima
3-fosfoglicerato intermedio 2-fosfoglicerato
ΔG° ′ =+1,1kcal/mol
La fosfoglicerato mutasa existe principalmente como un dímero de dos subunidades idénticas o estrechamente relacionadas de aproximadamente 32 kDa. La enzima se encuentra en organismos tan simples como la levadura a través del Homo sapiens y su estructura está altamente conservada en todas partes. (PGM de levadura ≈74 % conservado frente a la forma de mamífero).
En los mamíferos, las subunidades enzimáticas parecen ser una forma derivada del músculo (tipo m) o de otro tejido (tipo b para el cerebro donde se aisló originalmente la isoenzima b). Al existir como un dímero, la enzima tiene 3 isoenzimas dependiendo de qué subunidad forma la molécula completa (mm, bb o mb). El tipo mm se encuentra principalmente en el músculo liso casi exclusivamente. La isoenzima mb se encuentra en el músculo cardíaco y esquelético y la tipo bb se encuentra en el resto de tejidos. [11] Si bien las tres isoenzimas se pueden encontrar en cualquier tejido, las distribuciones anteriores se basan en la prevalencia en cada una.
Haga clic en genes, proteínas y metabolitos a continuación para vincular a los artículos respectivos. [§ 1]
La fosfoglicerato mutasa tiene una pequeña energía libre de Gibbs positiva y esta reacción se desarrolla fácilmente en ambas direcciones. Dado que es una reacción reversible, no es el sitio de mecanismos o esquemas de regulación importantes para la vía glucolítica.
Moléculas aniónicas como vanadato , [12] acetato , ion cloruro , fosfato , 2-fosfoglicolato y N-[tris(hidroximetil)metil-2-amino]etanosulfonato son inhibidores conocidos de la actividad mutasa de dPGM. Los estudios han demostrado que dPGM es sensible a los cambios en la concentración iónica, donde concentraciones crecientes de sales dan como resultado la activación de la actividad fosfatasa de la enzima al tiempo que inhiben su actividad mutasa. Se sabe que ciertas sales, como el KCl, son inhibidores competitivos con respecto a la actividad del 2-fosfoglicerato y de la mutasa. [13] Tanto el fosfato como el 2-fosfoglicolato son inhibidores competitivos de la actividad mutasa con respecto a los sustratos 2-fosfoglicerato y 2,3-bisfosfoglicerato. [14]
En los seres humanos, el gen PGAM2 que codifica esta enzima se encuentra en el brazo corto del cromosoma 7.
La deficiencia de fosfoglicerato mutasa causa la enfermedad de almacenamiento de glucógeno tipo X , un raro trastorno genético autosómico recesivo con síntomas que varían de leves a moderados; No se cree que ponga en peligro la vida y se puede controlar con cambios en el estilo de vida. [ cita necesaria ] Esto se presenta como una miopatía metabólica y es una de las muchas formas de síndromes anteriormente conocidos como distrofia muscular. [ cita necesaria ] La deficiencia de PGAM1 afecta el hígado, mientras que la deficiencia de PGAM2 afecta el músculo.
El inicio generalmente se observa desde la niñez hasta la edad adulta temprana, aunque algunos que pueden verse levemente afectados por el trastorno pueden no saber que lo padecen. Los pacientes con deficiencia de PGAM suelen ser asintomáticos, excepto cuando realizan esfuerzos breves y extenuantes que pueden desencadenar mialgias, calambres, necrosis muscular y mioglobinuria. [15] Una característica patológica inusual de la deficiencia de PGAM es la asociación con agregados tubulares. Los síntomas son intolerancia al esfuerzo o actividad física, calambres y dolores musculares. La debilidad permanente es rara. La enfermedad no es progresiva y tiene un pronóstico excelente. [ cita necesaria ]
GBP ; PFKFB1 ; PFKFB2 ; PFKFB3 ; PFKFB4 ; PGAM1 ; PGAM2 ; PGAM4; PGAM5 ; STS1; UBASH3A ;