Una hexoquinasa es una enzima que fosforila de forma irreversible las hexosas ( azúcares de seis carbonos ) y forma hexosas fosfato. En la mayoría de los organismos, la glucosa es el sustrato más importante para las hexoquinasas, y la glucosa-6-fosfato es el producto más importante. La hexoquinasa posee la capacidad de transferir un grupo fosfato inorgánico del ATP a un sustrato.
Las hexoquinasas no deben confundirse con la glucoquinasa , que es una hexoquinasa específica que se encuentra en el hígado. Todas las hexoquinasas son capaces de fosforilar varias hexosas, pero la hexoquinasa IV(D) suele denominarse de forma engañosa glucoquinasa, aunque no es más específica para la glucosa que las otras isoenzimas de los mamíferos. [3]
Se han descubierto genes que codifican la hexoquinasa en todos los dominios de la vida y existen en una variedad de especies que van desde bacterias , levaduras y plantas hasta humanos y otros vertebrados . Las enzimas de levaduras, plantas y vertebrados muestran evidencia clara de homología de secuencia, pero las de bacterias pueden no estar relacionadas. [4]
Se clasifican como proteínas plegadas de actina , que comparten un núcleo de sitio de unión de ATP común que está rodeado de secuencias más variables que determinan las afinidades del sustrato y otras propiedades.
En una sola especie pueden existir varias isoenzimas de hexoquinasa que desempeñan diferentes funciones .
Las reacciones intracelulares mediadas por hexoquinasas se pueden caracterizar como:
donde hexosa-CH 2 OH representa cualquiera de varias hexosas (como la glucosa) que contienen una fracción -CH 2 OH accesible.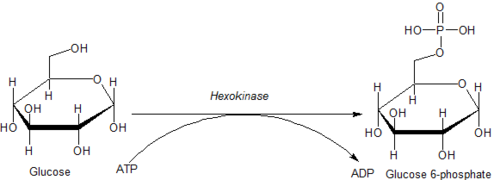
La fosforilación de una hexosa como la glucosa suele limitarla a una serie de procesos metabólicos intracelulares, como la glucólisis o la síntesis de glucógeno . Esto se debe a que las hexosas fosforiladas están cargadas y, por lo tanto, son más difíciles de transportar fuera de la célula.
En pacientes con fructosuria esencial , el metabolismo de la fructosa por la hexoquinasa a fructosa-6-fosfato es el método principal de metabolización de la fructosa dietética; esta vía no es significativa en individuos normales.
La mayoría de las hexoquinasas bacterianas tienen un tamaño de aproximadamente 50 kDa. Los organismos multicelulares, incluidas las plantas y los animales, a menudo tienen más de una isoforma de hexoquinasa. La mayoría tienen un tamaño de aproximadamente 100 kDa y constan de dos mitades (terminal N y C), que comparten mucha homología de secuencia. Esto sugiere un origen evolutivo por duplicación y fusión de una hexoquinasa ancestral de 50 kDa similar a las de las bacterias.
Existen cuatro isoenzimas hexoquinasas importantes en mamíferos ( EC 2.7.1.1) que varían en ubicaciones subcelulares y cinéticas con respecto a diferentes sustratos y condiciones, y función fisiológica. Se las designó hexoquinasas A, B, C y D sobre la base de su movilidad electroforética. [5] Los nombres alternativos hexoquinasas I, II, III y IV (respectivamente) [6] propuestos posteriormente son ampliamente utilizados.
Las hexoquinasas I, II y III se denominan isoenzimas de baja K m debido a una alta afinidad por la glucosa (por debajo de 1 mM). Las hexoquinasas I y II siguen la cinética de Michaelis-Menten a concentraciones fisiológicas de sustratos. [ cita requerida ] Las tres son fuertemente inhibidas por su producto, glucosa-6-fosfato . Las masas moleculares son de alrededor de 100 kDa. Cada una consta de dos mitades similares de 50 kDa, pero solo en la hexoquinasa II ambas mitades tienen sitios activos funcionales.
La hexoquinasa IV de mamíferos, también conocida como glucoquinasa , se diferencia de otras hexoquinasas en su cinética y funciones.
La fosforilación se produce a nivel subcelular cuando la glucoquinasa se traslada entre el citoplasma y el núcleo de las células hepáticas . La glucoquinasa sólo puede fosforilar la glucosa si la concentración de este sustrato es suficientemente alta; no sigue la cinética de Henri-Michaelis-Menten y no tiene K m ; está semisaturada a concentraciones de glucosa 100 veces superiores a las de las hexoquinasas I, II y III.
La hexoquinasa IV es monomérica, de aproximadamente 50 kDa, muestra cooperatividad positiva con la glucosa y no es inhibida alostéricamente por su producto, la glucosa-6-fosfato. [4]
La hexoquinasa IV está presente en el hígado , el páncreas , el hipotálamo , el intestino delgado y quizás en otras células neuroendocrinas , y desempeña un papel regulador importante en el metabolismo de los carbohidratos . En las células β de los islotes pancreáticos , actúa como un sensor de glucosa para controlar la liberación de insulina y, de manera similar, controla la liberación de glucagón en las células α . En los hepatocitos del hígado, la glucoquinasa responde a los cambios en los niveles ambientales de glucosa aumentando o reduciendo la síntesis de glucógeno.
La glucosa es única porque todas las células pueden utilizarla para producir ATP tanto en presencia como en ausencia de oxígeno molecular (O2 ) . El primer paso de la glucólisis es la fosforilación de la glucosa por la hexoquinasa.
Compuesto C00031 en la base de datos de rutas KEGG . Enzima 2.7.1.1 en la base de datos de rutas KEGG . Compuesto C00668 en la base de datos de rutas KEGG . Reacción R01786 en la base de datos de rutas KEGG .
Al catalizar la fosforilación de la glucosa para producir glucosa 6-fosfato, las hexoquinasas mantienen el gradiente de concentración descendente que favorece el transporte facilitado de la glucosa al interior de las células. Esta reacción también inicia todas las vías fisiológicamente relevantes de utilización de la glucosa, incluidas la glucólisis y la vía de las pentosas fosfato . [9] La adición de un grupo fosfato cargado en la posición 6 de las hexosas también asegura el "atrapamiento" de la glucosa y los análogos de la glucosa 2-desoxihexosa (por ejemplo, 2-desoxiglucosa y 2-fluoro-2-desoxiglucosa) dentro de las células, ya que las hexosas fosfato cargadas no pueden atravesar fácilmente la membrana celular.
Las hexoquinasas I y II pueden asociarse físicamente a la superficie externa de la membrana externa de las mitocondrias mediante la unión específica a una porina, o canal aniónico dependiente de voltaje. Esta asociación confiere a la hexoquinasa acceso directo al ATP generado por las mitocondrias, que es uno de los dos sustratos de la hexoquinasa. La hexoquinasa mitocondrial está muy elevada en las células tumorales malignas de rápido crecimiento, con niveles hasta 200 veces superiores a los de los tejidos normales. Se ha demostrado que la hexoquinasa unida a las mitocondrias es la fuerza impulsora [10] de las tasas glucolíticas extremadamente altas que tienen lugar aeróbicamente en las células tumorales (el llamado efecto Warburg descrito por Otto Heinrich Warburg en 1930).
La deficiencia de hexoquinasa es una enfermedad genética autosómica recesiva que causa anemia hemolítica crónica. La anemia hemolítica crónica es causada por una mutación en el gen que codifica la hexoquinasa. La mutación causa una reducción de la actividad de la hexoquinasa y, por lo tanto, una deficiencia de la misma. [11]