Las ginkgólidos son lactonas terpénicas biológicamente activas presentes en el Ginkgo biloba . Son diterpenoides con esqueletos de 20 carbonos, que se biosintetizan a partir de pirofosfato de geranilgeranilo . [1]
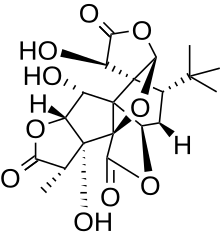
Ginkgolide B, específicamente, es una trilactona diterpenoide con seis anillos de cinco miembros. Contiene un anillo carbocíclico espiro[4,4]-nonano, un anillo de tetrahidrofurano y un grupo terc-butilo muy específico en uno de los anillos (Figura 1). La clase de ginkgólidos se aisló por primera vez del árbol Ginkgo biloba en 1932. [2] La elucidación estructural se logró en 1967 por Maruyama et al . [3]
Se extrae de la corteza de la raíz y las hojas del árbol Ginkgo biloba ( ginkyo que significa "albaricoque plateado") que se encuentra en China. Se comercializa en otros países que incluyen Corea, Francia, Estados Unidos, etc. por las propiedades farmacológicas y clínicas de los extractos. En el árbol está presente menos del 0,1 al 0,25% de ginkgólido B, siendo el más abundante el ginkgólido A. [4]
Esta clase de moléculas se ha estudiado por su potencial para actuar como antagonista del receptor del factor activador de plaquetas . [2] [5]
Se ha investigado el potencial de la ginkgolida B para reducir la frecuencia de las migrañas. [6]
Ginkgolide B también se utiliza en el tratamiento de la enfermedad cerebrovascular . Las investigaciones también han demostrado que la ginkgolida B también puede tratar las migrañas en edades tempranas. [2] [4] [6] La literatura indica que la ginkgolida B funciona como un antagonista selectivo de los receptores de glicina basado en la inhibición no competitiva para el sistema neurológico que realiza este compuesto. [5]
Las ginkolides A - C se aislaron a partir de una extracción metanólica a gran escala seguida de particiones líquido-líquido, cromatografía en columna y cristalizaciones repetidas. Las fórmulas moleculares se determinaron mediante espectrometría de masas de alta resolución y las estructuras generales mediante análisis espectroscópicos de IR y RMN y extensas técnicas de derivatización.

Si bien los investigadores han publicado vías químicas para producir esta molécula, la mayoría de las síntesis diseñadas eran demasiado complejas y producían poco del material real para realizar análisis completos. [2] Por lo tanto, es preferible estudiar la biosíntesis de la molécula.
La mayoría de los terpenoides de productos naturales comienzan con difosfato de isopentenilo sintetizado por la vía MEP . Esta vía también genera dimetilalil difosfato , a partir de piruvato y D-gliercaldehído 3-fosfato (GAP). Cuando se acoplan, forman una molécula de geranilgeranil difosfato con geranilgeranil difosfato sintasa.
Una molécula de GGPP genera ( 1 )(+)-copalilo en presencia de levopimaradieno sintasa . ( a ) Luego ( 1 ) pierde su grupo OPP catalizado por esta misma sintasa, realizando una ciclación alílica intramolecular con los dos alquenos , para formar ( 2 ) el catión sandaracopimarenilo. ( b ) Este catión luego sufre una ciclación interna para estabilizar el carbocatión en el anillo mediante transferencia de protones para formar ( 3 ) intermedio. ( c ) Al hacer esto, la molécula se prepara para una migración de metilo para estabilizar ese catión secundario y generar ese carbocatión terciario en ( 4 ). ( d ) Esto induce una pérdida de protones para obtener ( 5 ) levopimaradieno. ( e ) Con la oxidación, la pérdida de un protón para formar un anillo aromático genera ( 6 ) abietatrieno . ( g ) Este abietatrieno recién formado sufre un cambio de 1,2-alquilo para romper el anillo de 6 miembros en ( 7 ) con un anillo de cinco miembros (más favorable). ( h ) Se produce otro cambio de 1,2-alquilo al mismo tiempo que se produce una escisión del anillo para generar ( 8 ). ( i ) La oxidación en todas las posiciones con alquenos genera ( 9 ) intermedio que luego sufre cierres de anillo con un hemiacetal y las tres lactonas para obtener ginkgólido B en ( 10 ). [4]