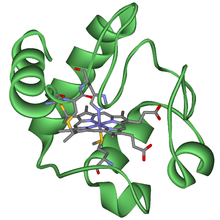
Los citocromos son proteínas con actividad redox que contienen un hemo , con un átomo central de hierro (Fe) en su núcleo, como cofactor . Están involucrados en la cadena de transporte de electrones y en la catálisis redox . Se clasifican según el tipo de hemo y su modo de unión . Cuatro variedades son reconocidas por la Unión Internacional de Bioquímica y Biología Molecular (IUBMB), los citocromos a, los citocromos b , los citocromos c y el citocromo d . [1]
La función del citocromo está relacionada con el cambio redox reversible del estado de oxidación ferroso (Fe (II)) al férrico (Fe (III)) del hierro que se encuentra en el núcleo hemo. [2] Además de la clasificación realizada por la IUBMB en cuatro clases de citocromos, en la literatura bioquímica se pueden encontrar varias clasificaciones adicionales, como el citocromo o [3] y el citocromo P450 .
Los citocromos fueron descritos inicialmente en 1884 por Charles Alexander MacMunn como pigmentos respiratorios (miohematina o histohematina). [4] En la década de 1920, Keilin redescubrió estos pigmentos respiratorios y los llamó citocromos o “pigmentos celulares”. [5] Clasificó estas proteínas hemo según la posición de su banda de absorción de energía más baja en su estado reducido, como citocromos a (605 nm), b (≈565 nm) yc ( 550 nm). Las firmas espectroscópicas de ultravioleta (UV) a visible de los hemo todavía se utilizan para identificar el tipo de hemo en el estado reducido ligado a bispiridina, es decir, el método del hemocromo de piridina. Dentro de cada clase, citocromo a , b o c , los citocromos tempranos se numeran consecutivamente, por ejemplo, cyt c , cyt c 1 y cyt c 2 , con ejemplos más recientes designados por su máximo de banda R de estado reducido, por ejemplo, cyt c 559 . [6]
El grupo hemo es un sistema de anillos altamente conjugado (lo que permite que sus electrones sean muy móviles) que rodea a un ion hierro. El hierro en los citocromos generalmente existe en un estado ferroso (Fe 2+ ) y férrico (Fe 3+ ) con un estado ferroxo (Fe 4+ ) que se encuentra en los intermedios catalíticos. [1] Los citocromos son, por tanto, capaces de realizar reacciones de transferencia de electrones y catálisis mediante reducción u oxidación de su hierro hemo. La ubicación celular de los citocromos depende de su función. Se pueden encontrar como proteínas globulares y proteínas de membrana .
En el proceso de fosforilación oxidativa , una proteína globular del citocromo cc participa en la transferencia de electrones desde el complejo III unido a la membrana al complejo IV . El propio complejo III está compuesto por varias subunidades, una de las cuales es un citocromo de tipo b mientras que otra es un citocromo de tipo c. Ambos dominios participan en la transferencia de electrones dentro del complejo. El complejo IV contiene un dominio del citocromo a/a3 que transfiere electrones y cataliza la reacción del oxígeno al agua. El fotosistema II, el primer complejo proteico en las reacciones dependientes de la luz de la fotosíntesis oxigenada , contiene una subunidad del citocromo b. La ciclooxigenasa 2 , una enzima implicada en la inflamación , es una proteína del citocromo b.
A principios de la década de 1960, Emanuel Margoliash [7] sugirió una evolución lineal de los citocromos que condujo a la hipótesis del reloj molecular . La tasa de evolución aparentemente constante de los citocromos puede ser una herramienta útil para tratar de determinar cuándo varios organismos pueden haberse separado de un ancestro común . [8]
Existen varios tipos de citocromo y pueden distinguirse mediante espectroscopia , estructura exacta del grupo hemo, sensibilidad a inhibidores y potencial de reducción. [9]
Se distinguen cuatro tipos de citocromos por sus grupos protésicos:
No existe un "citocromo e", pero el citocromo f , que se encuentra en el complejo citocromo b 6 f de las plantas, es un citocromo de tipo c. [12]
En las mitocondrias y los cloroplastos , estos citocromos a menudo se combinan en el transporte de electrones y vías metabólicas relacionadas: [13]
Una familia distinta de citocromos es la familia del citocromo P450 , llamada así por el característico pico de Soret formado por la absorbancia de luz en longitudes de onda cercanas a 450 nm cuando el hierro hemo se reduce (con ditionito de sodio ) y se compleja con monóxido de carbono . Estas enzimas participan principalmente en la esteroidogénesis y la desintoxicación . [14] [9]
{{cite book}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace )