El diseño de fármacos , a menudo denominado diseño racional de fármacos o simplemente diseño racional , es el proceso inventivo de encontrar nuevos medicamentos basándose en el conocimiento de un objetivo biológico . [1] El fármaco es más comúnmente una pequeña molécula orgánica que activa o inhibe la función de una biomolécula como una proteína , lo que a su vez produce un beneficio terapéutico para el paciente . En el sentido más básico, el diseño de fármacos implica el diseño de moléculas que sean complementarias en forma y carga al objetivo biomolecular con el que interactúan y, por lo tanto, se unirán a él. El diseño de fármacos con frecuencia, pero no necesariamente, se basa en técnicas de modelado por computadora . [2] Este tipo de modelado a veces se denomina diseño de fármacos asistido por computadora . Finalmente, el diseño de fármacos que se basa en el conocimiento de la estructura tridimensional del objetivo biomolecular se conoce como diseño de fármacos basado en la estructura . [2] Además de las moléculas pequeñas, los productos biofarmacéuticos que incluyen péptidos [3] [4] y especialmente anticuerpos terapéuticos son una clase cada vez más importante de medicamentos y también se han desarrollado métodos computacionales para mejorar la afinidad, selectividad y estabilidad de estas terapias basadas en proteínas. [5]
La frase "diseño de fármacos" es similar al diseño de ligandos (es decir, el diseño de una molécula que se unirá firmemente a su objetivo). [6] Aunque las técnicas de diseño para la predicción de la afinidad de unión son razonablemente exitosas, hay muchas otras propiedades, como la biodisponibilidad , la vida media metabólica y los efectos secundarios , que primero deben optimizarse antes de que un ligando pueda convertirse en un fármaco seguro y eficaz. Estas otras características a menudo son difíciles de predecir con técnicas de diseño racionales.
Debido a las altas tasas de deserción, especialmente durante las fases clínicas del desarrollo de fármacos , se está prestando más atención en las primeras etapas del proceso de diseño de fármacos a la selección de fármacos candidatos cuyas propiedades fisicoquímicas se prevé que resulten en menos complicaciones durante el desarrollo y, por lo tanto, tengan más probabilidades de conducir a un fármaco aprobado y comercializado. [7] Además, los experimentos in vitro complementados con métodos computacionales se utilizan cada vez más en el descubrimiento temprano de fármacos para seleccionar compuestos con perfiles ADME (absorción, distribución, metabolismo y excreción) y toxicológicos más favorables . [8]
Un objetivo biomolecular (más comúnmente una proteína o un ácido nucleico ) es una molécula clave involucrada en una vía metabólica o de señalización particular que está asociada con una condición o patología de enfermedad específica o con la infectividad o supervivencia de un patógeno microbiano . Los objetivos potenciales de los fármacos no son necesariamente causantes de enfermedades, pero por definición deben ser modificadores de la enfermedad. [9] En algunos casos, se diseñarán moléculas pequeñas para mejorar o inhibir la función del objetivo en la vía específica modificadora de la enfermedad. Se diseñarán moléculas pequeñas (por ejemplo, agonistas , antagonistas , agonistas inversos o moduladores de receptores ; activadores o inhibidores de enzimas; o abridores o bloqueadores de canales iónicos ) [10] que sean complementarias al sitio de unión del objetivo. [11] Las moléculas pequeñas (fármacos) se pueden diseñar de manera que no afecten a ninguna otra molécula importante "fuera del objetivo" (a menudo denominadas antiobjetivos ) ya que las interacciones de los fármacos con moléculas fuera del objetivo pueden provocar efectos secundarios indeseables . [12] Debido a las similitudes en los sitios de unión, los objetivos estrechamente relacionados identificados a través de la homología de secuencia tienen la mayor probabilidad de reactividad cruzada y, por lo tanto, el mayor potencial de efectos secundarios.
En la mayoría de los casos, los fármacos son pequeñas moléculas orgánicas producidas mediante síntesis química, pero los fármacos basados en biopolímeros (también conocidos como biofármacos ) producidos mediante procesos biológicos son cada vez más comunes. [13] Además, las tecnologías de silenciamiento de genes basadas en ARNm pueden tener aplicaciones terapéuticas. [14] Por ejemplo, las nanomedicinas basadas en ARNm pueden agilizar y acelerar el proceso de desarrollo de fármacos, lo que permite la expresión transitoria y localizada de moléculas inmunoestimulantes. [15] El ARNm transcrito in vitro (IVT) permite la administración a varios tipos de células accesibles a través de la sangre o vías alternativas. El uso de ARNm IVT sirve para transmitir información genética específica a las células de una persona, con el objetivo principal de prevenir o alterar una enfermedad en particular. [16]
El descubrimiento fenotípico de fármacos es un método tradicional de descubrimiento de fármacos, también conocido como farmacología avanzada o farmacología clásica. Utiliza el proceso de cribado fenotípico en colecciones de pequeñas moléculas sintéticas, productos naturales o extractos dentro de bibliotecas químicas para identificar sustancias que exhiben efectos terapéuticos beneficiosos. Este método consiste en descubrir primero la actividad funcional in vivo o in vitro de los fármacos (como los fármacos de extracto o los productos naturales) y luego realizar la identificación del objetivo. El descubrimiento fenotípico utiliza un enfoque práctico e independiente del objetivo para generar pistas iniciales, con el objetivo de descubrir compuestos farmacológicamente activos y terapias que operan a través de nuevos mecanismos farmacológicos. [17] Este método permite la exploración de fenotipos de enfermedades para encontrar tratamientos potenciales para afecciones con orígenes desconocidos, complejos o multifactoriales, donde la comprensión de los objetivos moleculares es insuficiente para una intervención eficaz. [18]
El diseño racional de fármacos (también llamado farmacología inversa ) comienza con la hipótesis de que la modulación de un objetivo biológico específico puede tener valor terapéutico. Para que una biomolécula sea seleccionada como objetivo de un fármaco, se requieren dos datos esenciales. El primero es la evidencia de que la modulación del objetivo modificará la enfermedad. Este conocimiento puede provenir, por ejemplo, de estudios de vinculación de enfermedades que muestran una asociación entre mutaciones en el objetivo biológico y ciertos estados patológicos. [19] El segundo es que el objetivo sea capaz de unirse a una molécula pequeña y que su actividad pueda ser modulada por la molécula pequeña. [20]
Una vez que se ha identificado un objetivo adecuado, normalmente se clona , se produce y se purifica . La proteína purificada se utiliza luego para establecer un ensayo de detección . Además, se puede determinar la estructura tridimensional del objetivo.
La búsqueda de pequeñas moléculas que se unan al objetivo se inicia con la selección de bibliotecas de compuestos farmacológicos potenciales. Esto se puede hacer utilizando el ensayo de selección ("pantalla húmeda"). Además, si se dispone de la estructura del objetivo, se puede realizar una selección virtual de los fármacos candidatos. Idealmente, los compuestos farmacológicos candidatos deberían ser " similares a los fármacos ", es decir, deberían poseer propiedades que se prevea que conduzcan a una biodisponibilidad oral , una estabilidad química y metabólica adecuada y efectos tóxicos mínimos. [21] Hay varios métodos disponibles para estimar la similitud con los fármacos, como la Regla de los Cinco de Lipinski y una variedad de métodos de puntuación, como la eficiencia lipofílica . [22] También se han propuesto varios métodos para predecir el metabolismo de los fármacos en la literatura científica. [23]
Debido a la gran cantidad de propiedades de los fármacos que deben optimizarse simultáneamente durante el proceso de diseño, a veces se emplean técnicas de optimización multiobjetivo . [24] Finalmente, debido a las limitaciones de los métodos actuales para la predicción de la actividad, el diseño de fármacos todavía depende en gran medida de la serendipia [25] y la racionalidad limitada . [26]
El objetivo más fundamental en el diseño de fármacos es predecir si una molécula dada se unirá a un objetivo y, de ser así, con qué fuerza. La mecánica molecular o la dinámica molecular se utilizan con mayor frecuencia para estimar la fuerza de la interacción intermolecular entre la molécula pequeña y su objetivo biológico. Estos métodos también se utilizan para predecir la conformación de la molécula pequeña y para modelar los cambios conformacionales en el objetivo que pueden ocurrir cuando la molécula pequeña se une a él. [3] [4] Los métodos semiempíricos , de química cuántica ab initio o la teoría funcional de la densidad se utilizan a menudo para proporcionar parámetros optimizados para los cálculos de mecánica molecular y también proporcionar una estimación de las propiedades electrónicas (potencial electrostático, polarizabilidad , etc.) del candidato a fármaco que influirán en la afinidad de unión. [27]
También se pueden utilizar métodos de mecánica molecular para proporcionar una predicción semicuantitativa de la afinidad de unión. Además, se puede utilizar una función de puntuación basada en el conocimiento para proporcionar estimaciones de la afinidad de unión. Estos métodos utilizan regresión lineal , aprendizaje automático , redes neuronales u otras técnicas estadísticas para derivar ecuaciones predictivas de afinidad de unión ajustando las afinidades experimentales a las energías de interacción derivadas computacionalmente entre la molécula pequeña y el objetivo. [28] [29]
Lo ideal sería que el método computacional pudiera predecir la afinidad antes de sintetizar un compuesto, por lo que en teoría solo se necesita sintetizar un compuesto, lo que ahorraría mucho tiempo y dinero. La realidad es que los métodos computacionales actuales son imperfectos y, en el mejor de los casos, solo brindan estimaciones cualitativamente precisas de la afinidad. En la práctica, se requieren varias iteraciones de diseño, síntesis y pruebas antes de descubrir un fármaco óptimo. Los métodos computacionales han acelerado el descubrimiento al reducir el número de iteraciones necesarias y, a menudo, han proporcionado estructuras novedosas. [30] [31]
El diseño de fármacos asistido por computadora se puede utilizar en cualquiera de las siguientes etapas del descubrimiento de fármacos:

Para superar la predicción insuficiente de la afinidad de unión calculada por las funciones de puntuación recientes, se utilizan para el análisis la interacción proteína-ligando y la información de la estructura 3D del compuesto. Para el diseño de fármacos basado en la estructura, se han desarrollado varios análisis posteriores a la selección centrados en la interacción proteína-ligando para mejorar el enriquecimiento y extraer de forma eficaz candidatos potenciales:
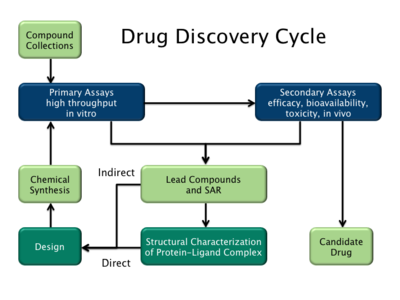
Existen dos tipos principales de diseño de fármacos. El primero se denomina diseño de fármacos basado en ligandos y el segundo, diseño de fármacos basado en la estructura. [2]
El diseño de fármacos basado en ligandos (o diseño indirecto de fármacos ) se basa en el conocimiento de otras moléculas que se unen al objetivo biológico de interés. Estas otras moléculas pueden utilizarse para derivar un modelo de farmacóforo que define las características estructurales mínimas necesarias que debe poseer una molécula para unirse al objetivo. [36] Se puede construir un modelo del objetivo biológico basándose en el conocimiento de lo que se une a él, y este modelo a su vez puede utilizarse para diseñar nuevas entidades moleculares que interactúen con el objetivo. Alternativamente, se puede derivar una relación cuantitativa estructura-actividad (QSAR), en la que se correlaciona entre las propiedades calculadas de las moléculas y su actividad biológica determinada experimentalmente . Estas relaciones QSAR a su vez pueden utilizarse para predecir la actividad de nuevos análogos. [37]
El diseño de fármacos basado en la estructura (o diseño directo de fármacos ) se basa en el conocimiento de la estructura tridimensional del objetivo biológico obtenido a través de métodos como la cristalografía de rayos X o la espectroscopia RMN . [38] Si no se dispone de una estructura experimental de un objetivo, puede ser posible crear un modelo de homología del objetivo basado en la estructura experimental de una proteína relacionada. Utilizando la estructura del objetivo biológico, se pueden diseñar fármacos candidatos que se predice que se unirán con alta afinidad y selectividad al objetivo utilizando gráficos interactivos y la intuición de un químico medicinal . Alternativamente, se pueden utilizar varios procedimientos computacionales automatizados para sugerir nuevos candidatos a fármacos. [39]
Los métodos actuales para el diseño de fármacos basados en la estructura se pueden dividir en tres categorías principales. [40] El primer método es la identificación de nuevos ligandos para un receptor determinado mediante la búsqueda en grandes bases de datos de estructuras 3D de moléculas pequeñas para encontrar aquellas que se ajusten al bolsillo de unión del receptor utilizando programas rápidos de acoplamiento aproximado . Este método se conoce como cribado virtual .
Una segunda categoría es el diseño de novo de nuevos ligandos. En este método, las moléculas de ligando se construyen dentro de las limitaciones de la cavidad de unión mediante el ensamblaje de pequeñas piezas de manera gradual. Estas piezas pueden ser átomos individuales o fragmentos moleculares. La principal ventaja de este método es que se pueden sugerir estructuras nuevas, que no están contenidas en ninguna base de datos. [41] [42] [43] Un tercer método es la optimización de ligandos conocidos mediante la evaluación de análogos propuestos dentro de la cavidad de unión. [40]
La identificación del sitio de unión es el primer paso en el diseño basado en la estructura. [20] [44] Si la estructura del objetivo o un homólogo suficientemente similar se determina en presencia de un ligando unido, entonces el ligando debería ser observable en la estructura, en cuyo caso la ubicación del sitio de unión es trivial. Sin embargo, puede haber sitios de unión alostéricos desocupados que puedan ser de interés. Además, puede ser que solo estén disponibles estructuras de apoproteína (proteína sin ligando) y la identificación confiable de sitios desocupados que tienen el potencial de unir ligandos con alta afinidad no sea trivial. En resumen, la identificación del sitio de unión generalmente se basa en la identificación de superficies cóncavas en la proteína que pueden acomodar moléculas del tamaño de un fármaco que también poseen "puntos calientes" apropiados ( superficies hidrofóbicas , sitios de unión de hidrógeno , etc.) que impulsan la unión del ligando. [20] [44]
El diseño de fármacos basado en la estructura intenta utilizar la estructura de las proteínas como base para diseñar nuevos ligandos aplicando los principios del reconocimiento molecular . La unión selectiva de alta afinidad al objetivo es generalmente deseable ya que conduce a fármacos más eficaces con menos efectos secundarios. Por lo tanto, uno de los principios más importantes para diseñar u obtener nuevos ligandos potenciales es predecir la afinidad de unión de un determinado ligando a su objetivo (y antiobjetivos conocidos ) y utilizar la afinidad predicha como criterio de selección. [45]
Böhm desarrolló una de las primeras funciones de puntuación empírica de uso general para describir la energía de enlace de los ligandos a los receptores. [46] [47] Esta función de puntuación empírica tomó la forma:
dónde:
Una ecuación termodinámica "maestra" más general es la siguiente: [48]
dónde:
La idea básica es que la energía libre de enlace total se puede descomponer en componentes independientes que se sabe que son importantes para el proceso de enlace. Cada componente refleja un cierto tipo de alteración de la energía libre durante el proceso de enlace entre un ligando y su receptor objetivo. La ecuación maestra es la combinación lineal de estos componentes. De acuerdo con la ecuación de energía libre de Gibbs, se construyó la relación entre la constante de equilibrio de disociación, K d , y los componentes de la energía libre.
Se utilizan varios métodos computacionales para estimar cada uno de los componentes de la ecuación maestra. Por ejemplo, el cambio en el área de superficie polar tras la unión del ligando se puede utilizar para estimar la energía de desolvatación. El número de enlaces rotatorios congelados tras la unión del ligando es proporcional al término de movimiento. La energía configuracional o de deformación se puede estimar utilizando cálculos de mecánica molecular . Finalmente, la energía de interacción se puede estimar utilizando métodos como el cambio en la superficie no polar, potenciales derivados estadísticamente de la fuerza media , el número de enlaces de hidrógeno formados, etc. En la práctica, los componentes de la ecuación maestra se ajustan a los datos experimentales utilizando regresión lineal múltiple. Esto se puede hacer con un conjunto de entrenamiento diverso que incluya muchos tipos de ligandos y receptores para producir un modelo "global" menos preciso pero más general o un conjunto más restringido de ligandos y receptores para producir un modelo "local" más preciso pero menos general. [49]
Un ejemplo particular de diseño racional de fármacos implica el uso de información tridimensional sobre biomoléculas obtenida a partir de técnicas como la cristalografía de rayos X y la espectroscopia de RMN. El diseño de fármacos asistido por ordenador, en particular, se vuelve mucho más manejable cuando existe una estructura de alta resolución de una proteína diana unida a un ligando potente. Este enfoque para el descubrimiento de fármacos se conoce a veces como diseño de fármacos basado en la estructura. El primer ejemplo inequívoco de la aplicación del diseño de fármacos basado en la estructura que conduce a un fármaco aprobado es el inhibidor de la anhidrasa carbónica dorzolamida , que fue aprobado en 1995. [50] [51]
Otro caso de estudio en el diseño racional de fármacos es el imatinib , un inhibidor de la tirosina quinasa diseñado específicamente para la proteína de fusión bcr-abl que es característica de las leucemias positivas para el cromosoma Filadelfia ( leucemia mieloide crónica y ocasionalmente leucemia linfocítica aguda ). El imatinib es sustancialmente diferente de los fármacos anteriores para el cáncer , ya que la mayoría de los agentes de quimioterapia simplemente se dirigen a las células que se dividen rápidamente, sin diferenciar entre las células cancerosas y otros tejidos. [52]
Otros ejemplos incluyen:
Los tipos de cribado de fármacos incluyen el cribado fenotípico , el cribado de alto rendimiento y el cribado virtual . El cribado fenotípico se caracteriza por el proceso de cribado de fármacos utilizando modelos de enfermedades animales o celulares para identificar compuestos que alteran el fenotipo y producen efectos beneficiosos relacionados con la enfermedad. [54] [55] Las tecnologías emergentes en el cribado de alto rendimiento mejoran sustancialmente la velocidad de procesamiento y disminuyen el volumen de detección necesario. [56] El cribado virtual se completa por computadora, lo que permite que se pueda cribar una gran cantidad de moléculas con un ciclo corto y bajo costo. El cribado virtual utiliza una variedad de métodos computacionales que permiten a los químicos reducir bibliotecas virtuales extensas a tamaños más manejables. [57]
Se ha argumentado que la naturaleza altamente rígida y centrada del diseño racional de fármacos suprime la serendipia en el descubrimiento de fármacos. [58]