El ácido oxalacético (también conocido como ácido oxalacético u OAA ) es un compuesto orgánico cristalino con la fórmula química HO2CC (O)CH2CO2H . El ácido oxalacético, en forma de su base conjugada oxaloacetato , es un intermediario metabólico en muchos procesos que ocurren en los animales. Participa en la gluconeogénesis , el ciclo de la urea , el ciclo del glioxilato , la síntesis de aminoácidos , la síntesis de ácidos grasos y el ciclo del ácido cítrico . [1]
El ácido oxalacético sufre desprotonaciones sucesivas para dar el dianión :
A pH alto , el protón enolizable se ioniza:
Las formas enólicas del ácido oxalacético son particularmente estables. La tautomerización ceto-enólica es catalizada por la enzima oxaloacetato tautomerasa . El trans -enol-oxaloacetato también aparece cuando el tartrato es el sustrato de la fumarasa . [2]

El oxaloacetato se forma de varias formas en la naturaleza. Una de las principales vías es la oxidación del L -malato , catalizada por la malato deshidrogenasa , en el ciclo del ácido cítrico. El malato también se oxida por la succinato deshidrogenasa en una reacción lenta cuyo producto inicial es el enol-oxaloacetato. [3]
También surge de la condensación del piruvato con ácido carbónico, impulsada por la hidrólisis del ATP :
Este proceso, que se produce en el mesófilo de las plantas, se lleva a cabo a través del fosfoenolpiruvato , catalizado por la fosfoenolpiruvato carboxilasa .
El oxaloacetato también puede surgir de la transaminación o desaminación del ácido aspártico .
El oxaloacetato es un intermediario del ciclo del ácido cítrico , donde reacciona con acetil-CoA para formar citrato , catalizado por la citrato sintasa . También participa en la gluconeogénesis , el ciclo de la urea , el ciclo del glioxilato , la síntesis de aminoácidos y la síntesis de ácidos grasos . El oxaloacetato también es un potente inhibidor del complejo II .
La gluconeogénesis [1] es una vía metabólica que consiste en una serie de once reacciones catalizadas por enzimas, que resultan en la generación de glucosa a partir de sustratos no carbohidratos. El comienzo de este proceso tiene lugar en la matriz mitocondrial , donde se encuentran las moléculas de piruvato . Una molécula de piruvato es carboxilada por una enzima piruvato carboxilasa , activada por una molécula de ATP y una molécula de agua. Esta reacción da como resultado la formación de oxaloacetato. El NADH reduce el oxaloacetato a malato . Esta transformación es necesaria para transportar la molécula fuera de las mitocondrias . Una vez en el citosol , el malato se oxida a oxaloacetato nuevamente utilizando NAD+. Luego, el oxaloacetato permanece en el citosol, donde tendrán lugar el resto de reacciones. El oxaloacetato es luego descarboxilado y fosforilado por la fosfoenolpiruvato carboxiquinasa y se convierte en 2-fosfoenolpiruvato utilizando guanosina trifosfato (GTP) como fuente de fosfato. La glucosa se obtiene después de un procesamiento posterior.
El ciclo de la urea es una vía metabólica que da como resultado la formación de urea utilizando una molécula de amonio a partir de aminoácidos degradados, otro grupo de amonio a partir de aspartato y una molécula de bicarbonato. [1] Esta ruta ocurre comúnmente en los hepatocitos . Las reacciones relacionadas con el ciclo de la urea producen NADH , y el NADH se puede producir de dos formas diferentes. Una de ellas utiliza oxaloacetato . En el citosol hay moléculas de fumarato . El fumarato se puede transformar en malato por las acciones de la enzima fumarasa . La malato deshidrogenasa actúa sobre el malato para convertirse en oxaloacetato, produciendo una molécula de NADH. Después de eso, el oxaloacetato se reciclará a aspartato , ya que las transaminasas prefieren estos cetoácidos sobre los demás. Este reciclaje mantiene el flujo de nitrógeno hacia la célula.

El ciclo del glioxilato es una variante del ciclo del ácido cítrico. [4] Es una vía anabólica que ocurre en plantas y bacterias utilizando las enzimas isocitrato liasa y malato sintasa . Algunos pasos intermedios del ciclo son ligeramente diferentes del ciclo del ácido cítrico; sin embargo, el oxaloacetato tiene la misma función en ambos procesos. [1] Esto significa que el oxaloacetato en este ciclo también actúa como reactivo primario y producto final. De hecho, el oxaloacetato es un producto neto del ciclo del glioxilato porque su bucle del ciclo incorpora dos moléculas de acetil-CoA.
En etapas anteriores, el acetil-CoA se transfiere desde la mitocondria al citoplasma, donde reside la sintetasa de ácidos grasos . El acetil-CoA se transporta en forma de citrato, que se ha formado previamente en la matriz mitocondrial a partir del acetil-CoA y el oxaloacetato. Esta reacción suele iniciar el ciclo del ácido cítrico, pero cuando no hay necesidad de energía se transporta al citoplasma, donde se descompone en acetil-CoA citoplasmático y oxaloacetato.
Otra parte del ciclo requiere NADPH para la síntesis de ácidos grasos. [5] Parte de este poder reductor se genera cuando el oxaloacetato citosólico es devuelto a la mitocondria siempre que la capa mitocondrial interna no sea permeable al oxaloacetato. En primer lugar, el oxaloacetato se reduce a malato utilizando NADH. A continuación, el malato se descarboxila a piruvato. Ahora, este piruvato puede entrar fácilmente en la mitocondria, donde es carboxilado nuevamente a oxaloacetato por la piruvato carboxilasa. De esta manera, la transferencia de acetil-CoA que es de la mitocondria al citoplasma produce una molécula de NADH. La reacción general, que es espontánea, puede resumirse como:
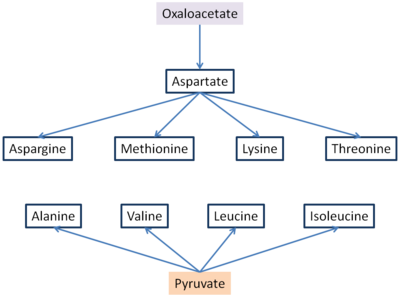
Seis aminoácidos esenciales y tres no esenciales se sintetizan a partir de oxaloacetato y piruvato . [6] El aspartato y la alanina se forman a partir de oxaloacetato y piruvato, respectivamente, por transaminación a partir del glutamato . La asparagina se sintetiza por amidación del aspartato, con la glutamina donando el NH4. Estos son aminoácidos no esenciales, y sus vías biosintéticas simples ocurren en todos los organismos. La metionina, treonina, lisina, isoleucina, valina y leucina son aminoácidos esenciales en humanos y la mayoría de los vertebrados. Sus vías biosintéticas en bacterias son complejas e interconectadas.
El oxaloacetato produce oxalato por hidrólisis. [7]
Este proceso es catalizado por la enzima oxaloacetasa , enzima presente en plantas, pero desconocida en el reino animal. [8]