El ácido clavulánico es un fármaco β-lactámico que funciona como un inhibidor de la β-lactamasa basado en un mecanismo . Si bien no es eficaz por sí solo como antibiótico , cuando se combina con antibióticos del grupo de las penicilinas , puede superar la resistencia a los antibióticos en las bacterias que secretan β-lactamasa , que de otro modo inactiva la mayoría de las penicilinas.
En sus preparados más habituales, el clavulanato potásico (ácido clavulánico como sal de potasio) se combina con:
El ácido clavulánico fue patentado en 1974. [1]
La amoxicilina-ácido clavulánico es un tratamiento de primera línea para muchos tipos de infecciones, incluidas las infecciones de los senos nasales y las infecciones del tracto urinario , incluida la pielonefritis . Esto se debe, en parte, a su eficacia contra las bacterias gramnegativas que tienden a ser más difíciles de controlar que las bacterias grampositivas con antibióticos quimioterapéuticos.
El uso de ácido clavulánico con penicilinas se ha asociado con una mayor incidencia de ictericia colestásica y hepatitis aguda durante el tratamiento o poco después. La ictericia asociada suele ser autolimitada y muy raramente mortal. [2] [3]
El Comité de Seguridad de Medicamentos (CSM) del Reino Unido recomienda que los tratamientos como las preparaciones de amoxicilina/ácido clavulánico se reserven para infecciones bacterianas que probablemente sean causadas por cepas productoras de β-lactamasas resistentes a la amoxicilina, y que el tratamiento normalmente no debe exceder los 14 días.
Se han informado reacciones alérgicas . [4]
El nombre deriva de cepas de Streptomyces clavuligerus , que produce ácido clavulánico. [5] [6]

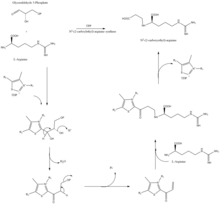
La estructura similar a la β-lactámico del ácido clavulánico parece estructuralmente similar a la penicilina , pero la biosíntesis de esta molécula implica una vía bioquímica diferente. El ácido clavulánico es producido por la bacteria Streptomyces clavuligerus , utilizando gliceraldehído-3-fosfato y L -arginina como materiales de partida. [7] [8] Aunque se conocen cada uno de los intermediarios de la vía, no se comprende completamente el mecanismo exacto de todas las reacciones enzimáticas. El proceso involucra principalmente 3 enzimas: clavaminado sintasa , β-lactama sintetasa y N 2 -(2-carboxietil)-L-arginina (CEA) sintasa . [7] La claveminato sintasa es una oxigenasa no hemo dependiente del hierro y del α-cetoglutarato y está codificada por orf5 del grupo de genes del ácido clavulánico . El mecanismo específico de cómo funciona esta enzima no se comprende completamente, pero esta enzima regula 3 pasos en la síntesis general de ácido clavulánico. Los 3 pasos ocurren en la misma región del centro de reacción catalítico que contiene hierro, pero no ocurren en secuencia y afectan diferentes áreas de la estructura del ácido clavulánico. [9]
La β-lactama sintetasa es una proteína de 54,5 kDa codificada por orf3 del grupo de genes del ácido clavulánico y muestra similitud con la asparagina sintasa , enzimas de clase B. El mecanismo exacto sobre cómo funciona esta enzima para sintetizar la β-lactámica no está probado, pero se cree que ocurre en coordinación con una CEA sintasa y ATP . [10]

CEA sintasa es una proteína de 60,9 kDA y es el primer gen que se encuentra en el grupo de genes de biosíntesis de ácido clavulánico, codificado por orf2 del grupo de genes de ácido clavulánico. El mecanismo específico de funcionamiento de esta enzima aún está bajo investigación; sin embargo, se sabe que esta enzima tiene la capacidad de acoplar gliceraldehído-3-fosfato con L-arginina en presencia de tiamina difosfato (TDP o tiamina pirofosfato ), que es el primer paso de la biosíntesis del ácido clavulánico. [11]
El ácido clavulánico fue descubierto alrededor de 1974-75 por científicos británicos que trabajaban en la compañía farmacéutica Beecham a partir de la bacteria Streptomyces clavuligerus . [12] Después de varios intentos, Beecham finalmente solicitó la protección de la patente estadounidense para el medicamento en 1981, y las patentes estadounidenses 4.525.352, 4.529.720 y 4.560.552 fueron concedidas en 1985.
El ácido clavulánico tiene una actividad antimicrobiana intrínseca insignificante, a pesar de compartir el anillo β-lactámico que es característico de los antibióticos β-lactámicos . Sin embargo, la similitud en la estructura química permite que la molécula interactúe con la enzima β-lactamasa secretada por ciertas bacterias para conferir resistencia a los antibióticos β-lactámicos.
El ácido clavulánico es un inhibidor suicida que se une covalentemente a un residuo de serina en el sitio activo de la β-lactamasa. Esto reestructura la molécula de ácido clavulánico, creando una especie mucho más reactiva que ataca a otro aminoácido en el sitio activo, inactivándolo permanentemente y, por lo tanto, inactivando la enzima.
Esta inhibición restablece la actividad antimicrobiana de los antibióticos β-lactámicos contra las bacterias resistentes a la secreción de lactamasa. A pesar de esto, han surgido algunas cepas bacterianas que son resistentes incluso a tales combinaciones.