En química orgánica , un haluro de arilo (también conocido como haloareno ) es un compuesto aromático en el que uno o más átomos de hidrógeno, unidos directamente a un anillo aromático , son reemplazados por un haluro . Los haloarenos se diferencian de los haloalcanos porque presentan muchas diferencias en los métodos de preparación y las propiedades. Los miembros más importantes son los cloruros de arilo, pero la clase de compuestos es tan amplia que existen muchos derivados y aplicaciones.
Los fluoruros de arilo se utilizan como intermediarios sintéticos, por ejemplo, para la preparación de productos farmacéuticos, pesticidas y cristales líquidos. [1] La conversión de sales de diazonio es una ruta bien establecida para obtener fluoruros de arilo. Por lo tanto, las anilinas son precursoras de los fluoruros de arilo. En la reacción clásica de Schiemann , el tetrafluoroborato es el donante de fluoruro:
En algunos casos se utiliza la sal de flúor:
Muchos fluoruros de arilo comerciales se producen a partir de cloruros de arilo mediante el proceso Halex . El método se utiliza a menudo para cloruros de arilo que también contienen grupos atractores de electrones . Un ejemplo ilustrativo es la síntesis de 2-fluoronitrobenceno a partir de 2-nitroclorobenceno : [2]
Los cloruros de arilo son los haluros de arilo que se producen en mayor escala comercialmente: 150.000 toneladas/año sólo en los EE.UU. (1994). Los niveles de producción están disminuyendo debido a preocupaciones medioambientales. Los clorobencenos se utilizan principalmente como disolventes. [3]
La halogenación de Friedel-Crafts o "cloración directa" es la principal vía de síntesis. Los ácidos de Lewis , por ejemplo el cloruro de hierro (III) , catalizan las reacciones. El haluro de arilo más abundante, el clorobenceno , se produce por esta vía: [4]
La monocloración del benceno va acompañada de la formación de los derivados del diclorobenceno . [3] Los arenos con grupos donadores de electrones reaccionan con halógenos incluso en ausencia de ácidos de Lewis. Por ejemplo, los fenoles y las anilinas reaccionan rápidamente con cloro y agua de bromo para dar productos multihalogenados. Hay disponibles muchos procedimientos de laboratorio detallados. [5] Para los derivados del alquilbenceno, por ejemplo el tolueno , las posiciones de alquilo tienden a ser halogenadas por condiciones de radicales libres , mientras que la halogenación del anillo se favorece en presencia de ácidos de Lewis. [6] La decoloración del agua de bromo por arenos ricos en electrones se utiliza en la prueba del bromo .
La oxicloración del benceno ha sido bien investigada, motivada por la evitación del HCl como coproducto en la halogenación directa: [3]
Sin embargo, esta tecnología no se utiliza ampliamente.
La reacción de Gatterman también se puede utilizar para convertir sales de diazonio en clorobencenos utilizando reactivos a base de cobre. Debido al alto costo de las sales de diazonio , este método se reserva para cloruros especiales.
Los principales bromuros de arilo producidos comercialmente son el anhídrido tetrabromoftálico, el éter de decabromodifenilo y el tetrabromobisfenol-A . Estos materiales se utilizan como retardantes de llama . Se producen por bromación directa de fenoles y éteres de arilo. El anhídrido ftálico es poco reactivo con el bromo, por lo que es necesario el uso de medios ácidos.
La reacción de Gatterman también se puede utilizar para convertir sales de diazonio en bromobencenos utilizando reactivos a base de cobre. Debido al alto costo de las sales de diazonio , este método se reserva para bromuros especiales.
Los yoduros de arilo sintéticos se utilizan como agentes de contraste de rayos X , pero por lo demás estos compuestos no se producen a gran escala. Los yoduros de arilo son sustratos "fáciles" para muchas reacciones, como las reacciones de acoplamiento cruzado y la conversión a reactivos de Grignard , pero son mucho más caros que los cloruros y bromuros de arilo, que son más ligeros y menos reactivos.
Los yoduros de arilo se pueden preparar tratando sales de diazonio con sales de yoduro. [7] Los arenos ricos en electrones, como las anilinas y los derivados dimetoxi, reaccionan directamente con el yodo. [8]
Los reactivos de arilo de litio y de arilo de Grignard reaccionan con yodo para dar el haluro de arilo:
Este método es aplicable a la preparación de todos los haluros de arilo. Una limitación es que la mayoría, pero no todos, [9] los reactivos de Grignard y de aril litio se producen a partir de haluros de arilo.
Aunque el término haluro de arilo incluye derivados halogenados de cualquier compuesto aromático, comúnmente se refiere a los halobencenos, que son específicamente derivados halogenados del benceno . Los grupos de halobencenos incluyen fluorobencenos , clorobencenos , bromobencenos y yodobencenos , así como halobencenos mixtos que contienen al menos dos tipos diferentes de halógenos unidos al mismo anillo de benceno. También hay muchos derivados de halobenceno .
Las halopiridinas se basan en el compuesto aromático piridina . [10] Esto incluye cloropiridinas y bromopiridinas . Las cloropiridinas son intermediarios importantes para productos farmacéuticos y agroquímicos .
Los naftalenos halogenados se basan en naftaleno . Los naftalenos policlorados se utilizaron ampliamente entre los años 1930 y 1950 en la producción de cables y condensadores, debido a sus propiedades aislantes, hidrófobas y retardantes de llama, pero desde entonces se han dejado de utilizar para este fin debido a su toxicidad, persistencia ambiental e introducción de nuevos materiales. [3]
Las hormonas tiroideas triyodotironina (T 3 ) y tiroxina (T 4 ) son yoduros de arilo. La T 4 , un tetrayoduro, se biosintetiza mediante yodación electrofílica del derivado de tirosina. [11] La T 4 sintética es uno de los medicamentos más recetados en los EE. UU. [12]
Los organismos marinos producen muchos compuestos aromáticos clorados y bromados. El cloruro y el bromuro en las aguas oceánicas son la fuente de los halógenos. Varias enzimas peroxidasas (por ejemplo, la bromoperoxidasa ) catalizan las reacciones. Numerosos son derivados de anillos ricos en electrones que se encuentran en la tirosina, el triptófano y varios pirroles. Algunos de estos haluros de arilo naturales exhiben propiedades medicinales útiles. [13] [14]


Las distancias CX para los haluros de arilo siguen la tendencia esperada. Estas distancias para el fluorobenceno, el clorobenceno, el bromobenceno y el 4-yodobenzoato de metilo son 135,6(4), 173,90(23), 189,8(1) y 209,9 pm , respectivamente. [15]
A diferencia de los haluros de alquilo típicos, los haluros de arilo no suelen participar en reacciones de sustitución convencionales. Los haluros de arilo con grupos atractores de electrones en las posiciones orto y para pueden experimentar reacciones S N Ar . Por ejemplo, el 2,4-dinitroclorobenceno reacciona en solución básica para dar un fenol.
A diferencia de la mayoría de las demás reacciones de sustitución, el fluoruro es el mejor grupo saliente y el yoduro el peor. [16] Un artículo de 2018 indica que esta situación puede ser bastante común y ocurrir en sistemas que anteriormente se suponía que procedían a través de mecanismos S N Ar. [17]
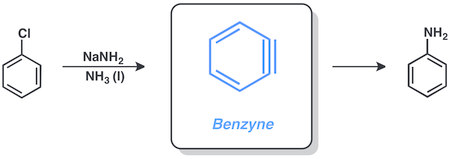
Los haluros de arilo suelen reaccionar por intermedio de bencinos . El clorobenceno y la amida sódica reaccionan en amoníaco líquido para dar anilina por esta vía.
Los haluros de arilo reaccionan con metales, generalmente litio o magnesio , para dar derivados organometálicos que funcionan como fuentes de aniones de arilo. Mediante la reacción de intercambio metal-halógeno , los haluros de arilo se convierten en compuestos de aril-litio. Un ejemplo ilustrativo es la preparación de fenil-litio a partir de bromobenceno utilizando n -butillitio ( n -BuLi):
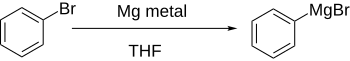
La formación directa de reactivos de Grignard , mediante la adición de magnesio al haluro de arilo en una solución etérea, funciona bien si el anillo aromático no se desactiva significativamente por grupos atractores de electrones.
Los haluros pueden ser desplazados por nucleófilos fuertes a través de reacciones que involucran aniones radicales. Alternativamente, los haluros de arilo, especialmente los bromuros y yoduros, experimentan adición oxidativa y, por lo tanto, están sujetos a reacciones de tipo aminación de Buchwald-Hartwig .
El clorobenceno fue en su día el precursor del fenol , que ahora se obtiene por oxidación del cumeno . A altas temperaturas, los grupos arilo reaccionan con el amoníaco para formar anilinas. [3]
Rhodococcus phenolicus es una bacteria que degrada el diclorobenceno como única fuente de carbono. [18]
Los haluros de arilo producidos en mayor escala son el clorobenceno y los isómeros del diclorobenceno. Una aplicación importante, pero que ya no se utiliza, era el uso del clorobenceno como disolvente para dispersar el herbicida Lasso. En general, la producción de cloruros de arilo (también derivados del naftilo) ha ido disminuyendo desde la década de 1980, en parte debido a preocupaciones medioambientales. [3] La trifenilfosfina se produce a partir del clorobenceno:
Los bromuros de arilo se utilizan ampliamente como retardantes del fuego. El miembro más destacado es el tetrabromobisfenol-A , que se prepara mediante bromación directa del difenol. [19]