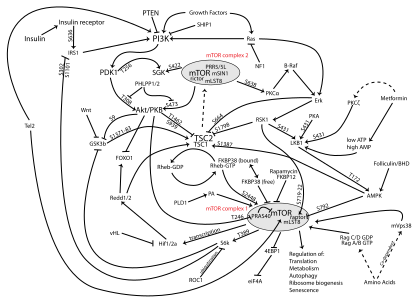
La vía PI3K/AKT/mTOR es una vía de señalización intracelular importante en la regulación del ciclo celular . Por lo tanto, está directamente relacionada con la quiescencia celular , la proliferación , el cáncer y la longevidad. La activación de PI3K fosforila y activa AKT , localizándolo en la membrana plasmática . [1] AKT puede tener una serie de efectos posteriores, como la activación de CREB , [2] la inhibición de p27 , [3] la localización de FOXO en el citoplasma, [3] la activación de PtdIns -3ps, [4] y la activación de mTOR [3] que puede afectar la transcripción de p70 o 4EBP1. [3] Hay muchos factores conocidos que mejoran la vía PI3K/AKT, incluidos EGF , [5] shh , [2] IGF-1 , [2] insulina , [3] y calmodulina . [4] Tanto la leptina como la insulina reclutan la señalización de PI3K para la regulación metabólica. [6] La vía es antagonizada por varios factores, incluidos PTEN , [7] GSK3B , [2] y HB9. [5]
En muchos tipos de cáncer, esta vía es hiperactiva, lo que reduce la apoptosis y permite la proliferación. Sin embargo, esta vía es necesaria para promover el crecimiento y la proliferación en lugar de la diferenciación de las células madre adultas , específicamente las células madre neuronales . [2] Los investigadores están tratando de determinar la dificultad de encontrar una cantidad adecuada de proliferación frente a diferenciación para utilizar este equilibrio en el desarrollo de diversas terapias. [2] Además, se ha descubierto que esta vía es un componente necesario en la potenciación neuronal a largo plazo . [4] [8]
Las células madre neurales (CMN) del cerebro deben encontrar un equilibrio entre mantener su multipotencia mediante la autorrenovación y la proliferación, en lugar de diferenciarse y volverse inactivas. La vía PI3K/AKT es crucial en este proceso de toma de decisiones. Las CMN son capaces de detectar y responder a los cambios en el cerebro o en todo el organismo. Cuando los niveles de glucosa en sangre se elevan de forma aguda, el páncreas libera insulina. La activación de los receptores de insulina activa la vía PI3K/AKT, que promueve la proliferación. [3] De esta manera, cuando hay niveles altos de glucosa y energía abundante en el organismo, la vía PI3K/AKT se activa y las CMN tienden a proliferar. Cuando hay bajas cantidades de energía disponible, la vía PI3K/AKT es menos activa y las células adoptan un estado inactivo. Esto ocurre, en parte, cuando AKT fosforila FOXO, manteniéndolo en el citoplasma. [3] FOXO, cuando se desfosforila, puede entrar al núcleo y funcionar como un factor de transcripción para promover la expresión de varios supresores tumorales como p27 y p21 . [3] Estos supresores tumorales empujan a las células madre neurales a entrar en estado de inactividad. Las células que carecen de FOXO pierden la capacidad de entrar en un estado de inactividad, así como su carácter de célula madre neural, lo que posiblemente les permita entrar en un estado similar al cáncer. [3]
La vía PI3K/AKT tiene un inhibidor natural llamado homólogo de fosfatasa y tensina ( PTEN ), cuya función es limitar la proliferación en las células, ayudando a prevenir el cáncer. Se ha demostrado que la eliminación de PTEN aumenta la masa del cerebro debido a la proliferación descontrolada que se produce. [3] PTEN funciona desfosforilando PIP3 a PIP2, lo que limita la capacidad de AKT de unirse a la membrana, disminuyendo su actividad. Las deficiencias de PTEN se pueden compensar posteriormente para rescatar la diferenciación o la inactividad. La eliminación de PTEN no es tan grave como la eliminación de FOXO por este motivo. [3]
El elemento de respuesta de cAMP, CREB, está estrechamente relacionado con la decisión de la célula de proliferar o no. Las células que se ven obligadas a sobreexpresar AKT aumentan la cantidad de CREB y la proliferación en comparación con las células de tipo salvaje. Estas células también expresan menos marcadores de células gliales y neuronales como GFAP o β-tubulina . [2] Esto se debe a que CREB es un factor de transcripción que influye en la transcripción de la ciclina A que promueve la proliferación. [2] Por ejemplo, las células progenitoras neuronales del hipocampo adulto necesitan un período de inactividad como células madre para diferenciarse más tarde. Esto está regulado por Shh . Shh funciona a través de una dependencia de síntesis proteica lenta, que estimula otras cascadas que funcionan sinérgicamente con la vía PI3K/AKT para inducir la proliferación. Luego, la otra vía puede desactivarse y los efectos de la vía PI3K/AKT se vuelven insuficientes para detener la diferenciación. [2] Se desconocen los detalles de esta vía.
La vía PI3K / AKT / mTOR es un regulador central del cáncer de ovario . Las quinasas PIM se expresan en exceso en muchos tipos de cáncer y también contribuyen a la regulación del cáncer de ovario . Se ha descubierto que las PIM activan de forma directa e indirecta a mTOR y sus efectores ascendentes, como AKT. Además, las quinasas PIM pueden provocar la fosforilación de IRS, que puede alterar PI3K. Esto indica la estrecha interacción de PIM con la cascada PI3K/AKT/mTOR y sus componentes. De forma similar, también se ha informado que AKT realiza la fosforilación de BAD en células de OC. Tanto PIM como la red PI3K/AKT/mTOR pueden inhibir las expresiones de P21 y P27 en células de OC. Estos datos sugieren una fuerte posibilidad de interacción y relevancia de las quinasas PIM y la red PI3K/AKT/mTOR en la regulación del cáncer de ovario. [9] Sin embargo, dirigirse a esta vía en el cáncer de ovario ha sido un desafío y varios ensayos no lograron obtener un beneficio clínico suficiente. [10] [11]
En muchos tipos de cáncer de mama, las aberraciones en la vía PI3K/AKT/mTOR son las anomalías genómicas más comunes. Las aberraciones conocidas más comunes incluyen la mutación del gen PIK3CA y las mutaciones de pérdida de función o silenciamiento epigenético de PTEN. [12] La vía de la fosfoinosítido 3-quinasa (PI3K)/proteína quinasa B (Akt)/diana mamífera de la rapamicina (mTOR) se activa en aproximadamente el 30-40% de los casos de cáncer de mama. En el cáncer de mama triple negativo (CMTN), la activación oncogénica de la vía PI3K/AKT/mTOR puede ocurrir como una función de la sobreexpresión de reguladores ascendentes como EGFR , mutaciones activadoras de PIK3CA , pérdida de función o expresión de la fosfatasa y homólogo de tensina (PTEN), y la inositol polifosfatasa rica en prolina, que son reguladores a la baja de PI3K. [13] Es consistente con la hipótesis de que los inhibidores de PI3K pueden superar la resistencia a la terapia endocrina cuando se adquiere [ cita requerida ]
PIK3CA frecuentemente tiene mutaciones de ganancia de función en el cáncer urotelial. [14] De manera similar a PI3Ka, PI3Kb se expresa en muchas células diferentes y está principalmente involucrada en la activación de plaquetas y el desarrollo de enfermedades trombóticas. Los estudios han demostrado que PI3Kb también contribuye a la proliferación tumoral. Específicamente, tiene un papel importante en la tumorigénesis en cánceres PTEN-negativos. [15] Se informa que interferir con el gen de PI3Kb podría ser un enfoque terapéutico para cánceres de vejiga de alto riesgo con PTEN mutante y pérdida de E-cadherina . Los inhibidores de isoformas específicas de PI3Kb son un tratamiento potencial para cánceres deficientes en PTEN. [16]
La vía PI3K es una fuente importante de resistencia a los fármacos en el cáncer de próstata . Esto es particularmente cierto en el cáncer de próstata resistente a la castración, donde los tumores se vuelven resistentes a la terapia de privación de andrógenos , que bloquea la capacidad de los tumores de utilizar la hormona andrógeno para crecer. [17] Esto se debe a un mecanismo de retroalimentación complejo que existe entre el receptor de andrógenos y la vía PI3K. [18] Como en otros tipos de tumores, las mutaciones en genes clave de esta vía pueden conducir a la hiperactivación de esta vía, por ejemplo en PIK3CA, [19] [20] Los aumentos en el número de copias de PIK3CA y el aumento de la expresión de ARNm también aumentan la activación de la vía en los cánceres de próstata, entre otros. [21] Se ha demostrado que las ganancias en la región genética cercana 3q26.31-32 ocurren simultáneamente con varios miembros cercanos de la familia PI3K, incluidos PIK3CA , PIK3CB y PIK3R4 , lo que conduce a cambios transcripcionales en PIK3C2G , PIK3CA, PIK3CB, PIK3R4, así como a vías asociadas con la proliferación celular . [22] Estas grandes ganancias que abarcan todo el organismo se asocian con el grado de Gleason , el estadio tumoral , la metástasis de los ganglios linfáticos y otras características clínicas agresivas. [22] En pacientes tratados con inhibidores de PI3K, aquellos con ganancias en el número de copias en PIK3CB parecen tener una mayor susceptibilidad a los fármacos. [23]
Los inhibidores de PI3K pueden superar la resistencia a los fármacos y mejorar los resultados del cáncer de mama avanzado (ABC). [12] Los diferentes inhibidores de PI3K muestran diferentes efectos contra varios tipos de PI3K. Los inhibidores de pan-PI3K de clase IA se han estudiado más ampliamente que los inhibidores específicos de isoformas; Pictilisib es otro inhibidor de pan-PI3K con mayor actividad inhibidora de la subunidad α que buparlisib. [13] Idelalisib es el primer inhibidor de PI3K aprobado por la Administración de Alimentos y Medicamentos de los EE. UU. y se utiliza en el tratamiento de la leucemia linfocítica crónica/linfoma linfocítico pequeño y el linfoma folicular recidivante/refractario. Copanlisib está aprobado para el linfoma folicular recidivante en pacientes que han recibido al menos dos terapias sistémicas previas. [24] Duvelisib está aprobado para la leucemia linfocítica crónica/linfoma linfocítico pequeño (LLC/LLP) recidivante/refractario y el linfoma folicular recidivante/refractario, ambas indicaciones para pacientes que han recibido al menos dos terapias previas. [25]
La AKT se encuentra aguas abajo de PI3K y es inhibida por Ipatasertib. [13] Akt es una quinasa de la familia AGC y un nodo de señalización central e integral de la vía PAM . Hay tres isoenzimas Akt, Akt1, Akt2 y Akt3. Los inhibidores de moléculas pequeñas de Akt1 podrían ser especialmente útiles para atacar tumores con una alta prevalencia de mutaciones activadoras de Akt1 E17K, que se observa en el 4-6% de los cánceres de mama y el 1-2% del cáncer colorrectal. [26] La investigación sobre la inhibición de Akt se ha centrado en la inhibición de dos sitios de unión distintos:
Los inhibidores alostéricos de Akt, entre los que destaca MK-2206, se han evaluado ampliamente en un entorno clínico. Recientemente, se han identificado inhibidores alostéricos de Akt adicionales. ARQ-092 es un potente inhibidor pan-Akt que puede inhibir el crecimiento tumoral de forma preclínica y actualmente se encuentra en estudios clínicos de fase I. [26]
Existe una correlación significativa entre la fosforilación de mTOR y la tasa de supervivencia de los pacientes con cáncer de mama triple negativo en estadios I y II. Un modelo de cáncer de mama triple negativo derivado de un paciente en el que se probó el inhibidor de mTOR rapamicina mostró una inhibición del crecimiento tumoral del 77-99 %, que es significativamente mayor que la observada con doxorrubicina; los estudios de fosforilación de proteínas indicaron que la activación constitutiva de la vía mTOR disminuyó con el tratamiento. [13]
Se ha planteado la hipótesis de que el bloqueo de la vía PI3K/AKT/mTOR puede conducir a una mayor actividad antitumoral en el cáncer de mama triple negativo. Los datos preclínicos han demostrado que la combinación de compuestos que actúan sobre diferentes moléculas relacionadas en la vía PI3K/AKT/mTOR produce una actividad sinérgica. Sobre la base de estos hallazgos, se siguen desarrollando nuevos compuestos que actúan sobre diferentes componentes de la vía PI3K/AKT/mTOR simultáneamente. Por ejemplo, gedatolisib inhibe las formas mutantes de PI3K-α con una actividad quinasa elevada en concentraciones equivalentes a la CI50 para la PI3K-α de tipo salvaje. Las isoformas PI3K-β, -δ y -γ fueron inhibidas por gedatolisib en concentraciones aproximadamente 10 veces superiores a las observadas para PI3K-α. [13] Otra ventaja de actuar simultáneamente sobre PI3K y mTOR es la consiguiente inhibición más robusta de los bucles de retroalimentación positivos de la tirosina quinasa del receptor que se observa con la inhibición aislada de PI3K . [27] Gedatolisib se encuentra actualmente en desarrollo para el tratamiento del TNBC, en combinación con el conjugado anticuerpo-fármaco PTK7. Apitolisib (GDC-0980) es un inhibidor de PI3K (subunidades α, δ y γ) que también actúa sobre mTORC [28]
Existen numerosas vías de señalización celular que presentan una comunicación cruzada con la vía PI3K, lo que potencialmente permite que las células cancerosas escapen a la inhibición de PI3K. [29] Como tal, la inhibición de la vía PI3K junto con otros objetivos podría ofrecer una respuesta sinérgica, como la observada con la inhibición codirigida de PI3K y MEK en células de cáncer de pulmón. [30] Más recientemente, se ha sugerido la codirigidez de la vía PI3K con quinasas PIM, con numerosos estudios preclínicos que sugieren el beneficio potencial de este enfoque. [31] [32] El desarrollo de paneles de líneas celulares que sean resistentes a la inhibición de la vía PI3K puede conducir a la identificación de futuros objetivos conjuntos y a una mejor comprensión de qué vías pueden compensar la pérdida de la señalización de PI3K después del tratamiento farmacológico. [33] La inhibición combinada de PI3K con terapias más tradicionales como la quimioterapia también puede ofrecer una respuesta mejorada sobre la inhibición de PI3K sola. [34]
El tipo de señalización del factor de crecimiento puede afectar si las células madre neurales se diferencian o no en neuronas motoras. La preparación de un medio con FGF2 reduce la actividad de la vía PI3K/AKT, que activa GSK3β. Esto aumenta la expresión de HB9. [5] La inhibición directa de PI3K en las células madre neurales conduce a una población de células que son puramente HB9+ y se diferencian con una eficiencia elevada en neuronas motoras. El injerto de estas células en diferentes partes de ratas genera neuronas motoras independientemente del microambiente de las células trasplantadas. [5] Después de una lesión, las células madre neurales entran en una fase de reparación y expresan altos niveles de PI3K para mejorar la proliferación. Esto es mejor para la supervivencia de las neuronas en su conjunto, pero se produce a expensas de la generación de neuronas motoras. Por lo tanto, puede ser difícil para las neuronas motoras lesionadas recuperar su capacidad. [5] El propósito de la investigación moderna es generar células madre neurales que puedan proliferar pero aún así diferenciarse en neuronas motoras. Reducir el efecto de la vía PI3K y aumentar el efecto de GSK3β y HB9 en las células madre neurales es una forma potencial de generar estas células. [5]
PTEN es un supresor tumoral que inhibe la vía PI3K/AKT. Los inhibidores de PTEN, como el bisperoxovanadio, [35] pueden mejorar la vía PI3K/AKT para promover la migración celular, [36] la supervivencia [37] y la proliferación. [7] Si bien existen algunas preocupaciones sobre la posible desregulación del ciclo celular y la tumorigénesis, la inhibición temporal y moderada de PTEN puede conferir neuroprotección contra la lesión cerebral traumática [38] y mejorar la recuperación del SNC al restablecer las conexiones perdidas por axonogénesis . [7] El valor medicinal de los inhibidores de PTEN aún está por determinar. [ cita requerida ]
Para que se produzca la potenciación a largo plazo (LTP), debe haber estimulación de los receptores NMDA , lo que hace que los receptores AMPA se inserten postsinápticamente . PI3K se une a los receptores AMPA en una región conservada para orientar los receptores en la membrana, específicamente en la subunidad GluR. [4] La actividad de PI3K aumenta en respuesta a los iones de calcio y CaM . Además, AKT localiza PtdIns-3Ps en la postsinapsis, lo que recluta proteínas de acoplamiento como tSNARE y Vam7. Esto conduce directamente al acoplamiento de AMPA en la postsinapsis. [4] mTOR activó p70S6K e inactivó 4EBP1, lo que cambia la expresión genética para permitir que se produzca la LTP. [8] El entrenamiento de condicionamiento del miedo a largo plazo se vio afectado en ratas, pero no hubo efecto en el condicionamiento a corto plazo. Específicamente, se perdió el condicionamiento del miedo de la amígdala. Se trata de un tipo de condicionamiento de trazas, una forma de aprendizaje que requiere la asociación de un estímulo condicionado con un estímulo incondicionado. Este efecto se perdió en las inhibiciones de PI3K y aumentó en las sobreexpresiones de PI3K. [8]
Además de su papel en la plasticidad sináptica descrita anteriormente, la vía de señalización PI3K-AKT también tiene un papel importante en el crecimiento cerebral, que se altera cuando se altera la señalización PI3K. Por ejemplo, el volumen intracraneal también está asociado con esta vía, en particular con las variantes intrónicas de AKT3 . [39] La hormona tiroidea se identificó originalmente como el regulador primario del crecimiento y la cognición cerebral, y evidencia reciente ha demostrado que la hormona tiroidea produce algunos de sus efectos en la maduración y plasticidad de las sinapsis a través de PI3K. [40]