
El haluro de sulfinilo tiene la fórmula general R −S (O) −X, donde X es un halógeno. Tienen un nivel de oxidación intermedio entre los haluros de sulfenilo , R-S-X, y los haluros de sulfonilo , R-SO 2 -X. Los ejemplos más conocidos son los cloruros de sulfinilo, compuestos termolábiles y sensibles a la humedad, que son intermedios útiles para la preparación de otros derivados de sufinilo como sulfinamidas, sulfinatos, sulfóxidos y tiosulfinatos. [1] A diferencia del átomo de azufre en los haluros de sulfonilo y los haluros de sulfenilo , el átomo de azufre en los haluros de sulfinilo es quiral , [2] como se muestra para el cloruro de metanosulfinilo.
Los cloruros de ácido sulfínico, o cloruros de sulfinilo, son haluros de sulfinilo con la fórmula general R-S(O)-Cl. El cloruro de metanosulfinilo, CH3S ( O)Cl, se prepara mediante cloración de disulfuro de dimetilo para dar CH3SCl3 , que se trata con anhídrido acético . Es un líquido de color pajizo. [3] El cloruro de toluenosulfinilo se prepara tratando tosilato de sodio con cloruro de tionilo : [4] También es un líquido de color pajizo, hierve cerca de 100 °C a 0,5 mm Hg.
Un enfoque general para la formación de cloruros de sulfinilo es mediante la reacción del tiol correspondiente con cloruro de sulfurilo , SO
2CL
2; en los casos en los que se produce cloruro de sulfenilo , RSCl, una oxidación con ácido trifluoroperacético produce el producto deseado, como en el caso del 2,2,2-trifluoro-1,1-difeniletanotiol : [ 5]
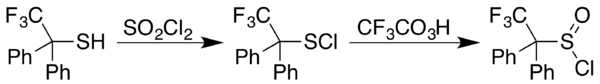
Estos compuestos reaccionan fácilmente con nucleófilos como agua, alcoholes, aminas, tioles y reactivos de Grignard . Si el nucleófilo es agua el producto es un ácido sulfínico , si es un alcohol el producto es un éster sulfínico, si es una amina primaria o secundaria el producto es una sulfinamida , si es un tiol el producto es un tiosulfinato , mientras que si es un reactivo de Grignard el producto es un sulfóxido . Debido a su reactividad e inestabilidad, los cloruros de alcanosulfinilo se utilizan generalmente sin purificación inmediatamente después de su síntesis. No se recomienda el almacenamiento ya que se desarrolla presión dentro del recipiente debido a la liberación de cloruro de hidrógeno.
El tratamiento de cloruros de alcanosulfinilo que tienen hidrógenos α con bases de amina terciaria da como compuestos aislables S -óxidos de tiocarbonilo (sulfinas). Así, el tratamiento del cloruro de n -propanosulfinilo con trietilamina da el S -óxido de sin -propanoetial , el agente lacrimógeno de la cebolla . [6] Tratamiento de cloruro de metanosulfinilo o cloruro de etano-1,2-bis-sulfinilo, ClS(O)CH 2 CH 2 S(O)Cl (preparado mediante cloración oxidativa de 1,2-etanoditiol, HSCH 2 CH 2 SH) , con una amina terciaria en presencia del alcohol secundario quiral derivado de la glucosa , diacetona -D -glucosa, proporciona ésteres de sulfinato ópticamente puros mediante un proceso de resolución cinética dinámica . [7] [8] Los cloruros de sulfinilo sufren reacciones de Friedel-Crafts con arenos dando sulfóxidos .
La hidrólisis a temperatura ambiente de CF 3 SF 3 da el fluoruro de sulfinilo CF 3 S(O)F en unas pocas horas con rendimiento cuantitativo. El tratamiento de CF 3 S(O)F con bromuro de hidrógeno a -78 °C da el bromuro de sulfinilo CF 3 S(O)Br, que es inestable a temperatura ambiente y se desproporciona fácilmente. [9] Los yoduros de sulfinilo son compuestos aparentemente desconocidos.
{{cite journal}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace ){{cite web}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace ){{cite journal}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace ){{cite journal}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace ){{cite journal}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace )