


En química , la hidrofobicidad es la propiedad física de una molécula que aparentemente es repelida por una masa de agua (conocida como hidrófoba ). [1] Por el contrario, los hidrófilos se sienten atraídos por el agua.
Las moléculas hidrófobas tienden a ser no polares y, por tanto, prefieren otras moléculas neutras y disolventes no polares . Como las moléculas de agua son polares, los hidrófobos no se disuelven bien entre ellas. Las moléculas hidrófobas del agua a menudo se agrupan formando micelas . El agua sobre superficies hidrofóbicas exhibirá un alto ángulo de contacto .
Ejemplos de moléculas hidrófobas incluyen los alcanos , los aceites , las grasas y las sustancias grasas en general. Los materiales hidrófobos se utilizan para la eliminación de petróleo del agua, la gestión de derrames de petróleo y procesos de separación química para eliminar sustancias no polares de compuestos polares. [2]
Hidrofóbico suele usarse indistintamente con lipófilo , “amante de las grasas”. Sin embargo, los dos términos no son sinónimos. Si bien las sustancias hidrófobas suelen ser lipófilas, existen excepciones, como las siliconas y los fluorocarbonos . [ cita necesaria ]
El término hidrófobo proviene del griego antiguo ὑδρόφοβος ( hidrófobos ), "tener miedo al agua", construido a partir del griego antiguo ὕδωρ (húdōr) 'agua' y del griego antiguo φόβος (phóbos) 'miedo'. [3]
La interacción hidrofóbica es principalmente un efecto entrópico que se origina a partir de la ruptura de los enlaces de hidrógeno altamente dinámicos entre las moléculas de agua líquida por el soluto no polar, lo que hace que el agua forme una estructura similar a un clatrato alrededor de las moléculas no polares. Esta estructura formada está más ordenada que las moléculas de agua libres debido a que las moléculas de agua se organizan para interactuar tanto como sea posible entre sí y, por lo tanto, da como resultado un estado entrópico más alto que hace que las moléculas no polares se agrupen para reducir el área de superficie expuesta. al agua y disminuir la entropía del sistema. [4] [5] Por lo tanto, las dos fases inmiscibles (hidrófila versus hidrofóbica) cambiarán de modo que su área interfacial correspondiente será mínima. Este efecto se puede visualizar en el fenómeno llamado separación de fases . [ cita necesaria ]

Las superficies superhidrófobas , como las hojas de la planta de loto, son aquellas que resultan extremadamente difíciles de mojar. Los ángulos de contacto de una gota de agua superan los 150°. [6] Esto se conoce como efecto loto y es principalmente una propiedad física relacionada con la tensión interfacial , más que una propiedad química. [7]
En 1805, Thomas Young definió el ángulo de contacto θ analizando las fuerzas que actúan sobre una gota de fluido que descansa sobre una superficie sólida rodeada por un gas. [8]
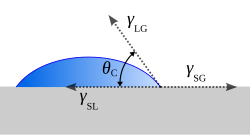

dónde
θ se puede medir utilizando un goniómetro de ángulo de contacto .
Wenzel determinó que cuando el líquido está en íntimo contacto con una superficie microestructurada, θ cambiará a θ W*
donde r es la relación entre el área real y el área proyectada. [9] La ecuación de Wenzel muestra que la microestructuración de una superficie amplifica la tendencia natural de la superficie. Una superficie hidrofóbica (una que tiene un ángulo de contacto original mayor a 90°) se vuelve más hidrofóbica cuando se microestructura: su nuevo ángulo de contacto se vuelve mayor que el original. Sin embargo, una superficie hidrófila (una que tiene un ángulo de contacto original inferior a 90°) se vuelve más hidrófila cuando se microestructura: su nuevo ángulo de contacto se vuelve menor que el original. [10] Cassie y Baxter descubrieron que si el líquido se suspende en la parte superior de las microestructuras, θ cambiará a θ CB* :
donde φ es la fracción de área del sólido que toca al líquido. [11] El líquido en el estado de Cassie-Baxter es más móvil que en el estado de Wenzel. [ cita necesaria ]
Podemos predecir si debería existir el estado de Wenzel o Cassie-Baxter calculando el nuevo ángulo de contacto con ambas ecuaciones. Según un argumento de minimización de la energía libre, la relación que predijo el nuevo ángulo de contacto más pequeño es el estado que tiene más probabilidades de existir. Expresado en términos matemáticos, para que exista el estado de Cassie-Baxter, debe ser cierta la siguiente desigualdad. [12]
Un criterio alternativo reciente para el estado de Cassie-Baxter afirma que el estado de Cassie-Baxter existe cuando se cumplen los dos criterios siguientes: 1) las fuerzas de la línea de contacto superan las fuerzas del cuerpo del peso de la gota no soportada y 2) las microestructuras son lo suficientemente altas como para evitar que el líquido que une las microestructuras para que no toquen la base de las microestructuras. [13]
Recientemente se ha desarrollado un nuevo criterio para el cambio entre los estados de Wenzel y Cassie-Baxter basado en la rugosidad y la energía de la superficie . [14] El criterio se centra en la capacidad de atrapar aire bajo gotas de líquido sobre superficies rugosas, lo que podría indicar si el modelo de Wenzel o el modelo de Cassie-Baxter deben usarse para cierta combinación de rugosidad y energía de la superficie. [ cita necesaria ]
El ángulo de contacto es una medida de hidrofobicidad estática, y la histéresis del ángulo de contacto y el ángulo de deslizamiento son medidas dinámicas. La histéresis del ángulo de contacto es un fenómeno que caracteriza la heterogeneidad de la superficie. [15] Cuando una pipeta inyecta un líquido sobre un sólido, el líquido formará algún ángulo de contacto. A medida que la pipeta inyecta más líquido, la gota aumentará de volumen, el ángulo de contacto aumentará, pero su límite trifásico permanecerá estacionario hasta que avance repentinamente hacia afuera. El ángulo de contacto que tenía la gota inmediatamente antes de avanzar hacia afuera se denomina ángulo de contacto de avance. El ángulo de contacto de retroceso ahora se mide bombeando el líquido nuevamente fuera de la gota. La gota disminuirá de volumen, el ángulo de contacto disminuirá, pero su límite trifásico permanecerá estacionario hasta que retroceda repentinamente hacia adentro. El ángulo de contacto que tenía la gota inmediatamente antes de retroceder hacia adentro se denomina ángulo de contacto de retroceso. La diferencia entre los ángulos de contacto de avance y retroceso se denomina histéresis del ángulo de contacto y se puede utilizar para caracterizar la heterogeneidad, rugosidad y movilidad de la superficie. [16] Las superficies que no son homogéneas tendrán dominios que impedirán el movimiento de la línea de contacto. El ángulo de deslizamiento es otra medida dinámica de hidrofobicidad y se mide depositando una gota sobre una superficie e inclinando la superficie hasta que la gota comienza a deslizarse. En general, los líquidos en el estado de Cassie-Baxter exhiben ángulos de deslizamiento e histéresis del ángulo de contacto más bajos que los del estado de Wenzel. [ cita necesaria ]
Dettre y Johnson descubrieron en 1964 que el fenómeno del efecto de loto superhidrófobo estaba relacionado con superficies hidrófobas rugosas y desarrollaron un modelo teórico basado en experimentos con perlas de vidrio recubiertas con parafina o telómero de TFE. La propiedad de autolimpieza de las superficies micro- nanoestructuradas superhidrófobas se informó en 1977. [17] Se desarrollaron materiales superhidrófobos formados por plasma de perfluoroalquilo, perfluoropoliéter y RF, que se utilizaron para electrohumectación y se comercializaron para aplicaciones biomédicas entre 1986 y 1995. [18 ] [19] [20] [21] Desde mediados de la década de 1990 han surgido otras tecnologías y aplicaciones. [22] En 2002 se dio a conocer una composición jerárquica superhidrófoba duradera, aplicada en uno o dos pasos, que comprende partículas de tamaño nanométrico ≤ 100 nanómetros superpuestas a una superficie que tiene características de tamaño micrométrico o partículas ≤ 100 micrómetros. Se observó que las partículas más grandes protegían a las partículas más pequeñas de la abrasión mecánica. [23]
En investigaciones recientes, se ha informado de superhidrofobicidad al permitir que el dímero de alquilceteno (AKD) se solidifique en una superficie fractal nanoestructurada. [24] Desde entonces, muchos artículos han presentado métodos de fabricación para producir superficies superhidrófobas, incluida la deposición de partículas, [25] técnicas sol-gel, [26] tratamientos con plasma, [27] deposición de vapor, [25] y técnicas de fundición. [28] Las oportunidades actuales para el impacto de la investigación residen principalmente en la investigación fundamental y la fabricación práctica. [29] Recientemente han surgido debates sobre la aplicabilidad de los modelos Wenzel y Cassie-Baxter. En un experimento diseñado para desafiar la perspectiva de la energía superficial del modelo de Wenzel y Cassie-Baxter y promover una perspectiva de línea de contacto, se colocaron gotas de agua en un punto hidrofóbico suave en un campo hidrofóbico rugoso, un punto hidrofóbico rugoso en un campo hidrofóbico suave, y una mancha hidrofílica en un campo hidrofóbico. [30] Los experimentos demostraron que la química y la geometría de la superficie en la línea de contacto afectaron el ángulo de contacto y la histéresis del ángulo de contacto , pero el área de la superficie dentro de la línea de contacto no tuvo ningún efecto. También se ha propuesto el argumento de que una mayor irregularidad en la línea de contacto mejora la movilidad de las gotas. [31]
Muchos materiales hidrófobos que se encuentran en la naturaleza se basan en la ley de Cassie y son bifásicos en el nivel submicrométrico con un componente de aire. El efecto loto se basa en este principio. Inspirándose en él , se han preparado muchas superficies superhidrófobas funcionales. [32]
Un ejemplo de material superhidrófobo biónico o biomimético en nanotecnología es la película de nanopin . [ cita necesaria ]
Un estudio presenta una superficie de pentóxido de vanadio que cambia reversiblemente entre superhidrofobicidad y superhidrofilicidad bajo la influencia de la radiación ultravioleta. [33] Según el estudio, cualquier superficie puede modificarse a este efecto mediante la aplicación de una suspensión de partículas de V 2 O 5 similares a rosas , por ejemplo con una impresora de inyección de tinta . Una vez más, la hidrofobicidad es inducida por bolsas de aire interlaminares (separadas por distancias de 2,1 nm ). También se explica el efecto UV. La luz ultravioleta crea pares electrón-hueco , y los huecos reaccionan con el oxígeno de la red, creando vacantes de oxígeno en la superficie, mientras que los electrones reducen V 5+ a V 3+ . Las vacantes de oxígeno las cubre el agua, y es esta absorbencia de agua por la superficie del vanadio lo que lo hace hidrófilo. Mediante un almacenamiento prolongado en la oscuridad, el agua es reemplazada por oxígeno y se pierde nuevamente la hidrofilicidad . [ cita necesaria ]
Una mayoría significativa de superficies hidrófobas tienen sus propiedades hidrófobas impartidas mediante modificación estructural o química de una superficie de un material a granel, ya sea mediante revestimientos o tratamientos superficiales. Es decir, la presencia de especies moleculares (generalmente orgánicas) o características estructurales dan como resultado ángulos de contacto elevados del agua. En los últimos años, se ha demostrado que los óxidos de tierras raras poseen hidrofobicidad intrínseca. [34] La hidrofobicidad intrínseca de los óxidos de tierras raras depende de la orientación de la superficie y los niveles de vacantes de oxígeno, y es naturalmente más robusta que los recubrimientos o tratamientos de superficie, y tiene aplicaciones potenciales en condensadores y catalizadores que pueden operar a altas temperaturas o ambientes corrosivos. [35]
El hormigón hidrofóbico se produce desde mediados del siglo XX. [ cita necesaria ]
La reciente investigación activa sobre materiales superhidrófobos podría eventualmente conducir a más aplicaciones industriales. [36]
Se ha informado de una rutina simple de recubrir tela de algodón con partículas de sílice [37] o titania [38] mediante la técnica sol-gel , que protege la tela de la luz ultravioleta y la vuelve superhidrófoba.
Se ha informado de una rutina eficaz para hacer que el polietileno sea superhidrófobo y, por tanto, autolimpiante. [39] El 99% de la suciedad de una superficie de este tipo se elimina fácilmente.
Las superficies superhidrófobas estampadas también son prometedoras para dispositivos de microfluidos de laboratorio en un chip y pueden mejorar drásticamente el bioanálisis basado en superficies. [40]
En el sector farmacéutico, la hidrofobicidad de las mezclas farmacéuticas afecta importantes atributos de calidad de los productos finales, como la disolución y la dureza del fármaco . [41] Se han desarrollado métodos para medir la hidrofobicidad de materiales farmacéuticos. [42] [43]
El desarrollo de superficies hidrofóbicas de enfriamiento radiativo pasivo diurno (PDRC), cuya efectividad en la reflectancia solar y la emitancia térmica se basa en su limpieza, ha mejorado la "autolimpieza" de estas superficies. Se han seguido desarrollando PDRC hidrofóbicos escalables y sostenibles que evitan los COV . [44]