Un reordenamiento alílico o desplazamiento alílico es una reacción química orgánica en la que la reacción en un centro vecino a un doble enlace hace que el doble enlace se desplace a un par de átomos adyacente:

Se encuentra tanto en la sustitución nucleofílica como en la electrófila , aunque suele estar suprimido en relación con la sustitución no alílica. Por ejemplo, la reacción de 1-cloro-2-buteno con hidróxido de sodio da lugar a 2-buten-1-ol y 3-buten-2-ol:

En la sustitución similar de 1-cloro-3-metil-2-buteno, el 2-metil-3-buten-2-ol secundario se produce con un rendimiento del 85%, mientras que el del 3-metil-2-buten-1-ol primario es del 15%.
Los desplazamientos alílicos se producen porque el estado de transición es un intermediario alílico . En otros aspectos son similares a la sustitución nucleofílica clásica y admiten mecanismos tanto bimoleculares como monomoleculares (respectivamente, las sustituciones S N 2' y S N 1'/S N i' ).
Los desplazamientos alílicos se convierten en la vía de reacción dominante cuando existe una resistencia sustancial a una sustitución normal (no alílica). En el caso de la sustitución nucleofílica, dicha resistencia se conoce cuando existe un impedimento estérico sustancial en el grupo saliente o alrededor de él , o si hay un sustituyente geminal que desestabiliza una acumulación de carga positiva. Los efectos de la sustitución en el grupo vinilo son menos claros. [1]
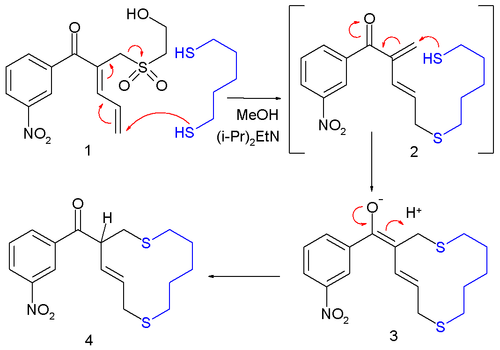
Aunque son aún más raros que S N ', los desplazamientos alílicos pueden ocurrir de forma viníloga, como un "desplazamiento butadienílico": [2]
En la reducción S N 2' , un hidruro desplaza alílicamente un buen grupo saliente en una reducción orgánica formal , similar a la síntesis de dienos de Whiting . Un ejemplo ocurrió en la síntesis total de taxol (anillo C): [3]
El hidruro es hidruro de litio y aluminio y el grupo saliente es una sal de fosfonio ; el desplazamiento alílico provoca el doble enlace exocíclico en el producto. Solo cuando el anillo de ciclohexano está correctamente sustituido, el protón se sumará en trans al grupo metilo adyacente .
Los cambios alílicos también pueden ocurrir con electrófilos . En el ejemplo siguiente, el grupo carbonilo en el benzaldehído es activado por ácido diborónico antes de la reacción con el alcohol alílico (ver: Reacción de Prins ): [4]

El sistema catalizador activo en esta reacción es una combinación de un compuesto de pinza de paladio y ácido p -toluenosulfónico , el producto de reacción se obtiene como un solo regioisómero y estereoisómero .
Los cambios alílicos repetidos pueden "cambiar de posición" un doble enlace entre dos posibles ubicaciones: [5]

Una reacción S N 2' debería explicar el resultado de la reacción de una aziridina que lleva un grupo bromuro de metileno con metil-litio : [6]
En esta reacción se pierde un equivalente de acetileno .