.jpg/440px-Triphenylbismuth(III).jpg)
La química del organobismuto es la química de compuestos organometálicos que contienen un enlace químico carbono - bismuto . Las aplicaciones son pocas. [1] [2] Los principales estados de oxidación del bismuto son Bi(III) y Bi(V) como en todos los elementos superiores del grupo 15 . La energía de un enlace al carbono en este grupo disminuye en el orden P > As > Sb > Bi. [3] El primer uso reportado de bismuto en química orgánica fue en la oxidación de alcoholes por Frederick Challenger en 1934 (usando Ph 3 Bi (OH) 2 ). [4] El conocimiento sobre las especies metiladas de bismuto en medios ambientales y biológicos es limitado. [5]
El trietilbismuto, el primer compuesto de organobismuto conocido, fue preparado en 1850 por Löwig y Schweizer a partir de yodoetano y una aleación de potasio-bismuto. Como ocurre con la mayoría de los compuestos de trialquilbismuto, el BiEt 3 tiene un olor extremadamente acre y desagradable y se oxida espontáneamente en el aire. [6] La química de estos complejos comenzó a recibir atención significativa cuando los reactivos de Grignard y los compuestos de organolitio estuvieron disponibles.

Los compuestos de triorganobismuto (III) son monoméricos con estructuras piramidales que recuerdan a la química del organofosforado (III). Sin embargo, los haluros adoptan estructuras hipervalentes. Esta tendencia queda ilustrada por la estructura laminar adoptada por el dicloruro de metilbismuto . [7]
La mayoría de los compuestos alifáticos de organobismuto (III) se oxidan fácilmente y los miembros más ligeros son pirofóricos . Las dialquilhalobismutinas no se pueden almacenar, ya que se descomponen incluso en atmósferas inertes. [8] : 413
Los diarilbismutinos se encuentran entre los agentes estornudos más potentes que se conocen. [8] : 413
Los heterociclos de organobismuto se basan en Bi (III). El compuesto cíclico bismol , un análogo estructural del pirrol , no ha sido aislado, pero se conocen bismoles sustituidos. [9] Se ha detectado bismabenceno en el laboratorio. [10]
La metodología más general y ampliamente utilizada para la síntesis de complejos homolépticos de trialquil y triarilbismuto hace reaccionar BiX 3 con reactivos de organolitio o magnesio : [6]
Los compuestos de triorganobismuto se prepararon por primera vez a partir de K 3 Bi y haluros orgánicos: [6]
Este método es generalmente más difícil y produce un rendimiento menor. Sin embargo, en 2006 siguió siendo el único método para, por ejemplo, la síntesis de (Me 3 Si) 3 Bi. [6]
Los compuestos de triaril bismuto (III) suelen ser sólidos cristalinos estables al aire y los sustituyentes reaccionarán antes que los enlaces carbono-bismuto en condiciones apropiadas: [11]

Los compuestos de organobismuto asimétricos proceden de forma más natural de los haluros de organobismuto (inestables) RBiX 2 y R 2 BiX. [6]
En la industria, los compuestos de triarilbismuto catalizan diversas polimerizaciones de alquenos y alquinos . [8] : 415
Los compuestos de triarilbismuto tienen un uso muy limitado en la síntesis orgánica. [12] Sus enlaces son débiles y fácilmente desplazados por otros elementos, metálicos o no metálicos. [8] : 413 Estas reacciones se desarrollan más fácilmente que en el caso de los congéneres más ligeros. Por supuesto, el trifenilbismuto se redistribuye con su trihaluro para dar derivados mixtos como el cloruro de difenilbismuto (Ph 2 BiCl). [13] Curiosamente, los reactivos de bismuto(III) pueden transferir sustituyentes a compuestos de talio(III) : [8] : 414
Bi(CH 2 = CMe) 3 + 3 TlCl 3 → (CH 2 = CMe) 2 TlCl + 2 BiCl 3 a −40 °C
Los compuestos de triarilbismuto (III) también se pueden emplear en transformaciones de formación de enlaces C – N y C – C con un cocatalizador metálico apropiado. Por ejemplo, Barton y sus compañeros de trabajo demostraron que las aminas podían N -arilarse con un reactivo de bismuto (III) en presencia de sal de cobre (II). [14]

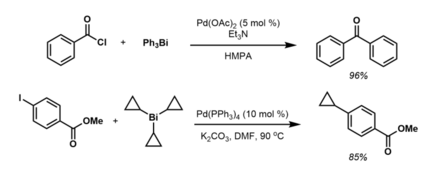
Asimismo, los cloruros de acilo reaccionan bajo catálisis con Pd(0) para formar una variedad de fenilcetonas. [15] Aunque no son formalmente arenos, los reactivos de triciclopropilbismuto (III) reaccionan con haluros y triflatos de arilo bajo catálisis con Pd (0) de manera similar para producir una variedad de aril y heteroaril ciclopropanos: [16]
La estabilidad térmica de los compuestos R 5 M disminuye en el orden As > Sb > Bi. Los compuestos de arilo son más estables que los compuestos de alquilo. Me 5 Bi se descompone explosivamente a 20°C. [ cita necesaria ]
La naturaleza de los ligandos de arilo es importante para determinar si la geometría del complejo es bipiramidal trigonal o plana cuadrada y su color. [6] En general, los compuestos homolépticos del tipo Ar 5 Bi adoptan estructuras piramidales cuadradas. El compuesto de pentafenilo tiene un color intenso y es termocrómico , posiblemente debido al equilibrio entre geometrías. [17]
Los carboxilatos rara vez forman complejos quelantes de bismuto. En cambio, los carboxilatos de organobismuto son típicamente poliméricos, y cada oxígeno del carboxilato se coordina con un átomo de bismuto diferente. [18] : 330–332, 344–345 No ocurre lo mismo con los xantatos . [18] : 334, 340
Los haluros de bismuto coordinados con arenos son complejos piano-taburete . [18] : 337, 341–343
Curiosamente, aunque se conocen muy pocos compuestos inorgánicos de Bi V , existe una amplia variedad de complejos de organobismuto pentacoordinados. [8] : 415 Los complejos de triarorganobismuto se oxidan fácilmente a complejos de bismuto (V) cuando se tratan con cloro o bromo, dando Ar 3 BiX 2 (X = Cl, Br). En cambio, las reacciones con yodo desplazan los ligandos para dar Ar 3-x BiI x tricoordinado , mientras que las reacciones con flúor son demasiado vigorosas para el control. [6]
Luego se puede acceder a complejos de organobismuto (V) totalmente carbonados mediante el desplazamiento del enlace bismuto-halógeno recién formado con un alquilo o aril litio o un reactivo de Grignard. Por ejemplo:
El inestable Ph 5 Bi de color púrpura fue el primero en sintetizarse de esta manera. [6]
Bi(V) forma fácilmente un ion onio, por ejemplo, mediante protonación con ácido p -toluenosulfónico : [19]
El pentafenilbismuto forma un complejo de ateína tras el tratamiento con fenil litio : [20]
Los reactivos de organobismuto(V) son útiles para una amplia variedad de transformaciones orgánicas. En comparación con sus congéneres más ligeros, los compuestos de Bi (V) son oxidantes fuertes, deshidrogenando alcoholes de todo tipo hasta carbonilo y escindiendo glicoles hasta aldehído. También participan en transferencias de arilo . [6]
Los compuestos Ph 3 Bi (OOtBu) 2 , Ph 3 BiCO 3 y (Ph 3 BiCl) 2 O han sido investigados para la oxidación de oxima , tiol , fenol y fosfina . [21] [ página necesaria ] En general, la oxidación se acelera cuando los ligandos de arilo tienen sustituyentes aceptores de electrones y ataca a los alcoholes antes que a los tioles o seleniuros. [8] : 416–417 Las hidracinas se deshidrogenan en compuestos azo y los tioles en una mezcla de sulfuros y disulfuros. [8] : 417–418 Los altos rendimientos requieren condiciones fuertemente básicas (en ausencia de ellas, el carbonato es el más efectivo), lo que sugiere que las especies activas son óxidos de triarilbismuto. Sin embargo, los compuestos de pentaarilbismuto también extraerán hidrógeno. [8] : 416–417
En general, los compuestos de bismuto (V) se arilan de manera ineficiente, transfiriendo solo uno de los cinco ligandos al sustrato [22] y dejando un residuo de triarilbismuto (III). [23] Reoxidar el complejo Bi III a Bi V es difícil e impide cerrar un ciclo catalítico en torno a esta química. [22] Sin embargo, Ph 5 Bi y Ph 3 BiCl 2 arilan 1,3-dicarbonilos y arenos : [24]
En la reacción, el reactivo de bismuto(V) pierde un grupo arilo y se une al oxígeno. La arilación y eliminación posteriores son asincrónicas y concertadas: [23]

Los donantes de pares de electrones adyacentes determinan la regioselectividad.
En presencia de una sal de cobre, dichos reactivos arilan aminas y alcoholes. También bajo luz ultravioleta , monoarilatan glicoles. El impedimento estérico gobierna su alta selectividad: los alcoholes secundarios están arilados sobre los terciarios y los alcoholes axiales están arilados sobre los ecuatoriales. [8] : 417–431