La plastoquinona ( PQ ) es una molécula terpenoide - quinona ( meroterpenoide ) implicada en la cadena de transporte de electrones en las reacciones de la fotosíntesis dependientes de la luz . La forma más común de plastoquinona, conocida como PQ-A o PQ-9, es una molécula de 2,3-dimetil-1,4- benzoquinona con una cadena lateral de nueve unidades de isoprenilo . Existen otras formas de plastoquinona, como aquellas con cadenas laterales más cortas como PQ-3 (que tiene 3 unidades laterales de isoprenilo en lugar de 9), así como análogos como PQ-B, PQ-C y PQ-D, que difieren en sus cadenas laterales. [1] Las unidades de benzoquinona e isoprenilo son no polares y anclan la molécula dentro de la sección interna de una bicapa lipídica , donde generalmente se encuentran las colas hidrofóbicas . [1]
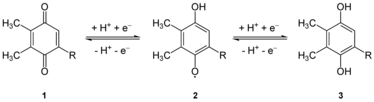
Las plastoquinonas son muy similares estructuralmente a la ubiquinona o coenzima Q10 , y se diferencian por la longitud de la cadena lateral de isoprenilo, la sustitución de los grupos metoxi por grupos metilo y la eliminación del grupo metilo en la posición 2 de la quinona. Al igual que la ubiquinona, puede presentarse en varios estados de oxidación: plastoquinona, plastosemiquinona (inestable) y plastoquinol , que se diferencia de la plastoquinona por tener dos grupos hidroxilo en lugar de dos grupos carbonilo . [2]
El plastoquinol, la forma reducida, también funciona como antioxidante al reducir las especies reactivas de oxígeno , algunas producidas a partir de reacciones fotosintéticas, que podrían dañar la membrana celular. [3] Un ejemplo de cómo lo hace es reaccionando con superóxidos para formar peróxido de hidrógeno y plastosemiquinona. [3]
El prefijo plasto- significa plastidio o cloroplasto , en alusión a su ubicación dentro de la célula. [4]

El papel que juega la plastoquinona en la fotosíntesis, más concretamente en las reacciones de la fotosíntesis dependientes de la luz, es el de portador de electrones móvil a través de la membrana del tilacoide . [2]
La plastoquinona se reduce cuando acepta dos electrones del fotosistema II y dos cationes de hidrógeno (H + ) del estroma del cloroplasto, formando así plastoquinol (PQH 2 ). Transfiere los electrones más abajo en la cadena de transporte de electrones a la plastocianina , un transportador de electrones móvil y soluble en agua, a través del complejo proteico citocromo b 6 f . [2] El complejo proteico citocromo b 6 f cataliza la transferencia de electrones entre la plastoquinona y la plastocianina, pero también transporta los dos protones a la luz de los discos tilacoides . [2] Esta transferencia de protones forma un gradiente electroquímico, que es utilizado por la ATP sintasa al final de las reacciones dependientes de la luz para formar ATP a partir de ADP y Pi . [2]
La plastoquinona se encuentra dentro del fotosistema II en dos sitios de unión específicos, conocidos como Q A y Q B. La plastoquinona en Q A , el sitio de unión primario, está muy estrechamente unida, en comparación con la plastoquinona en Q B , el sitio de unión secundario, que se elimina mucho más fácilmente. [5] A Q A solo se le transfiere un electrón, por lo que tiene que transferir un electrón a Q B dos veces antes de que Q B pueda recoger dos protones del estroma y ser reemplazado por otra molécula de plastoquinona. El QB protonado luego se une a un conjunto de moléculas de plastoquinona libres en la membrana del tilacoide. [2] [5] Las moléculas de plastoquinona libres eventualmente transfieren electrones a la plastocianina soluble en agua para continuar las reacciones dependientes de la luz. [2] Hay sitios de unión de plastoquinona adicionales dentro del fotosistema II (Q C y posiblemente Q D ), pero su función y/o existencia no se han dilucidado completamente. [5]
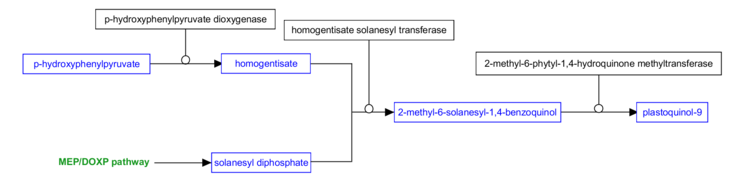
El p-hidroxifenilpiruvato se sintetiza a partir de tirosina , mientras que el solanesil difosfato se sintetiza mediante la vía MEP/DOXP . El homogeneizado se forma a partir de p-hidroxifenilpiruvato y luego se combina con difosfato de solanesilo mediante una reacción de condensación . El intermedio resultante, 2-metil-6-solanesil-1,4-benzoquinol, luego se metila para formar el producto final, plastoquinol-9. [1] Esta vía se utiliza en la mayoría de los organismos fotosintéticos, como algas y plantas. [1] Sin embargo, las cianobacterias parecen no utilizar homogentisato para sintetizar plastoquinol, lo que posiblemente resulte en una vía diferente a la que se muestra a continuación. [1]
Algunos derivados que fueron diseñados para penetrar las membranas celulares mitocondriales ( SkQ1 (plastoquinonil-decil-trifenilfosfonio), SkQR1 (el análogo de SkQ1 que contiene rodamina ), SkQ3) tienen actividad antioxidante y protonófora . [6] SkQ1 se ha propuesto como un tratamiento antienvejecimiento, con la posible reducción de los problemas de visión relacionados con la edad debido a su capacidad antioxidante. [7] [8] [9] Esta capacidad antioxidante resulta tanto de su capacidad antioxidante para reducir las especies reactivas de oxígeno (derivadas de la parte de la molécula que contiene plastoquinonol), que a menudo se forman dentro de las mitocondrias, como de su capacidad para aumentar la concentración de iones. intercambio a través de membranas (derivado de la parte de la molécula que contiene cationes que pueden disolverse dentro de las membranas). [9] Específicamente, al igual que el plastoquinol, se ha demostrado que SkQ1 elimina los superóxidos tanto dentro de las células (in vivo) como fuera de las células (in vitro). [10] SkQR1 y SkQ1 también se han propuesto como una posible forma de tratar problemas cerebrales como el Alzheimer debido a su capacidad para reparar potencialmente los daños causados por la beta amiloide . [9] Además, se ha demostrado que SkQR1 es una forma de reducir los problemas causados por el trauma cerebral a través de sus capacidades antioxidantes, que ayudan a prevenir las señales de muerte celular al reducir las cantidades de especies reactivas de oxígeno provenientes de las mitocondrias. [11]