La olefinación de Takai en química orgánica describe la reacción orgánica de un aldehído con un compuesto de diorganocromo para formar un alqueno . Es una reacción con nombre , llamada así por Kazuhiko Takai , quien la informó por primera vez en 1986. [1] En la reacción original, la especie de organocromo se genera a partir de yodoformo o bromoformo y un exceso de cloruro de cromo (II) y el producto es un haluro de vinilo . Una ventaja principal de esta reacción es la configuración E del doble enlace que se forma. Según el informe original, las alternativas existentes, como la reacción de Wittig, solo dieron mezclas.
En el mecanismo de reacción propuesto por Takai, el cromo (II) se oxida a cromo (III) eliminando dos equivalentes de un haluro. El complejo carbodianión geminal así formado (determinado como [Cr 2 Cl 4 (CHI)(THF) 4 ]) [2] [3] reacciona con el aldehído en una adición 1,2 a lo largo de uno de los enlaces carbono-cromo y en el siguiente paso ambos grupos portadores de cromo participan en una reacción de eliminación . En la proyección de Newman se puede ver cómo los volúmenes estéricos de los grupos cromo y los volúmenes estéricos de los grupos alquilo y halógeno impulsan esta reacción hacia la eliminación anti. [4]
Antes de la introducción de este protocolo basado en cromo, las reacciones de olefinación generalmente daban alquenos Z o mezclas de isómeros. [1] Se habían realizado reacciones de olefinación similares utilizando una variedad de reactivos como cloruro de zinc y plomo; [5] sin embargo, estas reacciones de olefinación a menudo conducen a la formación de dioles (la reacción de McMurry) en lugar de la metilenación o alquilidenación de aldehídos. [6] Para evitar este problema, el grupo de Takai examinó el potencial sintético de las sales de cromo (II).
La reacción emplea principalmente el uso de aldehídos, pero también pueden utilizarse cetonas. Sin embargo, las cetonas no reaccionan tan bien como los aldehídos; por lo tanto, para un compuesto con grupos aldehído y cetona, la reacción puede apuntar solo al grupo aldehído y dejar intacto el grupo cetona. [1]
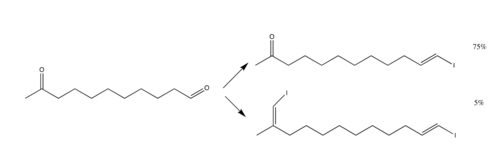
Las desventajas de la reacción incluyen el hecho de que estequiométricamente, se deben utilizar cuatro equivalentes de cloruro de cromo, ya que hay una reducción de dos átomos de halógeno. [3] Existen formas de limitar la cantidad de cloruro de cromo, concretamente mediante la utilización del equivalente de zinc, [7] pero este método sigue siendo impopular.
En una segunda publicación, el alcance de la reacción se amplió a los intermedios de diorganocromo que contienen grupos alquilo en lugar de halógenos: [8]