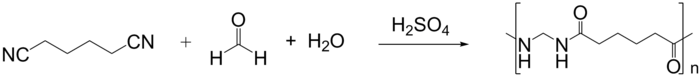Una poliamida es un polímero con unidades repetidas unidas por enlaces amida . [1]
Las poliamidas se producen tanto de forma natural como artificial. Ejemplos de poliamidas naturales son las proteínas , como la lana y la seda . Las poliamidas fabricadas artificialmente se pueden fabricar mediante polimerización por crecimiento escalonado o síntesis en fase sólida, obteniéndose materiales como nailon , aramidas y poliaspartato de sodio . Las poliamidas sintéticas se utilizan habitualmente en la industria textil, la automovilística, las alfombras, los utensilios de cocina y la ropa deportiva debido a su gran durabilidad y resistencia. La industria de fabricación de transporte es el principal consumidor, representando el 35% del consumo de poliamida (PA). [2]
Los polímeros de aminoácidos se conocen como polipéptidos o proteínas .
Según la composición de su cadena principal, las poliamidas sintéticas se clasifican de la siguiente manera:
Todas las poliamidas se obtienen mediante la formación de una función amida para unir dos moléculas de monómero. Los monómeros pueden ser amidas (normalmente en forma de lactama cíclica, como la caprolactama ), α,ω-aminoácidos o una mezcla estequiométrica de una diamina y un diácido. Ambos tipos de precursores dan lugar a un homopolímero. Las poliamidas se copolimerizan fácilmente, por lo que son posibles muchas mezclas de monómeros que, a su vez, pueden dar lugar a muchos copolímeros. Además, muchos polímeros de nailon son miscibles entre sí, lo que permite la creación de mezclas.
La producción de polímeros requiere la unión repetida de dos grupos para formar un enlace amida. En este caso, esto implica específicamente enlaces amida , y los dos grupos involucrados son un grupo amina y un componente carbonilo terminal de un grupo funcional . Estos reaccionan para producir un enlace carbono-nitrógeno, creando un enlace amida singular . Este proceso implica la eliminación de otros átomos que previamente formaban parte de los grupos funcionales. El componente carbonilo puede ser parte de un grupo de ácido carboxílico o del derivado de haluro de acilo más reactivo . El grupo amina y el grupo de ácido carboxílico pueden estar en el mismo monómero, o el polímero puede estar constituido por dos monómeros bifuncionales diferentes , uno con dos grupos amina y el otro con dos grupos de ácido carboxílico o cloruro de ácido.
La reacción de condensación se utiliza para producir sintéticamente polímeros de nailon en la industria. Los nailon deben incluir específicamente un monómero de cadena lineal ( alifático ). El enlace amida se produce a partir de un grupo amina (también conocido como grupo amino) y un grupo de ácido carboxílico . El hidroxilo del ácido carboxílico se combina con un hidrógeno de la amina y da lugar al agua, el subproducto de eliminación que da nombre a la reacción.
Como ejemplo de reacciones de condensación, considere que en los organismos vivos, los aminoácidos se condensan entre sí mediante una enzima para formar enlaces amida (conocidos como péptidos ). Las poliamidas resultantes se conocen como proteínas o polipéptidos. En el diagrama siguiente, considere los aminoácidos como monómeros alifáticos individuales que reaccionan con moléculas idénticas para formar una poliamida, centrándose únicamente en los grupos amino y ácido. Ignore los grupos sustituyentes R ; suponga que la diferencia entre los grupos R es insignificante:

Para poliamidas o aramidas totalmente aromáticas, como el Kevlar , se utiliza el cloruro de acilo, que es más reactivo, como monómero. La reacción de polimerización con el grupo amina elimina el cloruro de hidrógeno . La ruta del cloruro de ácido se puede utilizar como síntesis de laboratorio para evitar el calentamiento y obtener una reacción casi instantánea. [3] La fracción aromática en sí no participa en la reacción de eliminación, pero sí aumenta la rigidez y la resistencia del material resultante, lo que da lugar a la reconocida resistencia del Kevlar.
En el diagrama que aparece a continuación, una aramida está formada por dos monómeros diferentes que se alternan continuamente para formar la cadena polimérica. Las aramidas son poliamidas aromáticas:

Las poliamidas también pueden sintetizarse a partir de dinitrilos utilizando catálisis ácida mediante la aplicación de la reacción de Ritter. Este método es aplicable para la preparación de nailon 1,6 a partir de adiponitrilo , formaldehído y agua. [4] Además, las poliamidas también pueden sintetizarse a partir de glicoles y dinitrilos utilizando este método. [5]