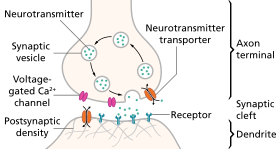
La neurotransmisión (del latín: transmissio "paso, cruce" de transmisore "enviar, dejar pasar") es el proceso mediante el cual las moléculas de señalización llamadas neurotransmisores son liberadas por el axón terminal de una neurona (la neurona presináptica) y se unen y reaccionan con la receptores en las dendritas de otra neurona (la neurona postsináptica) a poca distancia. Un proceso similar ocurre en la neurotransmisión retrógrada , donde las dendritas de la neurona postsináptica liberan neurotransmisores retrógrados (p. ej., endocannabinoides ; sintetizados en respuesta a un aumento en los niveles de calcio intracelular ) que envían señales a través de receptores que se encuentran en la terminal del axón de la neurona presináptica. principalmente en las sinapsis GABAérgicas y glutamatérgicas . [1] [2] [3] [4]
La neurotransmisión está regulada por varios factores diferentes: la disponibilidad y tasa de síntesis del neurotransmisor, la liberación de ese neurotransmisor, la actividad basal de la célula postsináptica, el número de receptores postsinápticos disponibles a los que se une el neurotransmisor y la posterior eliminación o desactivación del neurotransmisor por enzimas o recaptación presináptica. [5] [6]
En respuesta a un potencial de acción umbral o potencial eléctrico graduado , se libera un neurotransmisor en la terminal presináptica . El neurotransmisor liberado puede luego moverse a través de la sinapsis para ser detectado y unirse a los receptores de la neurona postsináptica. La unión de neurotransmisores puede influir en la neurona postsináptica de forma inhibidora o excitadora . La unión de neurotransmisores a receptores en la neurona postsináptica puede desencadenar cambios a corto plazo, como cambios en el potencial de membrana llamados potenciales postsinápticos , o cambios a más largo plazo mediante la activación de cascadas de señalización .
Las neuronas forman redes neuronales biológicas complejas a través de las cuales viajan los impulsos nerviosos (potenciales de acción). Las neuronas no se tocan entre sí (excepto en el caso de una sinapsis eléctrica a través de una unión gap ); en cambio, las neuronas interactúan en puntos de contacto cercanos llamados sinapsis. Una neurona transporta su información a través de un potencial de acción. Cuando el impulso nervioso llega a la sinapsis, puede provocar la liberación de neurotransmisores, que influyen en otra neurona (postsináptica). La neurona postsináptica puede recibir información de muchas neuronas adicionales, tanto excitadoras como inhibidoras. Las influencias excitatorias e inhibidoras se suman, y si el efecto neto es inhibidor, será menos probable que la neurona se "dispare" (es decir, genere un potencial de acción), y si el efecto neto es excitador, será más probable que la neurona se "dispare" (es decir, genere un potencial de acción). fuego. La probabilidad de que una neurona se dispare depende de qué tan lejos esté su potencial de membrana del potencial umbral , el voltaje al que se activa un potencial de acción porque se activan suficientes canales de sodio dependientes del voltaje para que la corriente neta de sodio entrante exceda todas las corrientes salientes. [7] Las entradas excitatorias acercan una neurona al umbral, mientras que las entradas inhibidoras la alejan del umbral. Un potencial de acción es un evento de "todo o nada"; las neuronas cuyas membranas no han alcanzado el umbral no se activarán, mientras que aquellas que sí lo hagan deben hacerlo. Una vez que se inicia el potencial de acción (tradicionalmente en el montículo del axón ), se propagará a lo largo del axón, lo que provocará la liberación de neurotransmisores en el botón sináptico para transmitir información a otra neurona adyacente.
Los neurotransmisores se empaquetan espontáneamente en vesículas y se liberan en paquetes cuantos individuales independientemente de los potenciales de acción presinápticos. Esta liberación lenta es detectable y produce efectos microinhibitorios o microexcitadores en la neurona postsináptica. Un potencial de acción amplifica brevemente este proceso. Los neurotransmisores que contienen vesículas se agrupan alrededor de sitios activos y, una vez liberados, pueden reciclarse mediante uno de los tres mecanismos propuestos. El primer mecanismo propuesto implica la apertura parcial y luego el nuevo cierre de la vesícula. Los dos segundos implican la fusión completa de la vesícula con la membrana, seguida del reciclaje o reciclaje hacia el endosoma. La fusión vesicular está impulsada en gran medida por la concentración de calcio en microdominios ubicados cerca de los canales de calcio, lo que permite solo microsegundos de liberación de neurotransmisores, mientras que volver a la concentración normal de calcio lleva un par de cientos de microsegundos. Se cree que la exocitosis de las vesículas está impulsada por un complejo proteico llamado SNARE , que es el objetivo de las toxinas botulínicas . Una vez liberado, un neurotransmisor ingresa a la sinapsis y encuentra receptores. Los receptores de neurotransmisores pueden ser ionotrópicos o acoplados a proteínas g. Los receptores ionotrópicos permiten el paso de iones cuando son agonizados por un ligando. El modelo principal implica un receptor compuesto de múltiples subunidades que permiten la coordinación de la preferencia de iones. Los receptores acoplados a proteína G, también llamados receptores metabotrópicos, cuando se unen a un ligando experimentan cambios conformacionales que producen una respuesta intracelular. La interrupción de la actividad de los neurotransmisores suele realizarse mediante un transportador, aunque también es posible una desactivación enzimática. [9]
Cada neurona se conecta con muchas otras neuronas y recibe numerosos impulsos de ellas. La suma es la suma de estos impulsos en el montículo del axón. Si la neurona sólo recibe impulsos excitadores, generará un potencial de acción. Si, por el contrario, la neurona recibe tantos impulsos inhibidores como excitadores, la inhibición anula la excitación y el impulso nervioso se detendrá allí. [10] La generación de potencial de acción es proporcional a la probabilidad y el patrón de liberación de neurotransmisores y a la sensibilización del receptor postsináptico. [11] [12] [13]
La suma espacial significa que los efectos de los impulsos recibidos en diferentes lugares de la neurona se suman, de modo que la neurona puede dispararse cuando dichos impulsos se reciben simultáneamente, incluso si cada impulso por sí solo no fuera suficiente para provocar la activación.
La suma temporal significa que los efectos de los impulsos recibidos en el mismo lugar pueden sumarse si los impulsos se reciben en una sucesión temporal cercana. Por lo tanto, la neurona puede dispararse cuando se reciben múltiples impulsos, incluso si cada impulso por sí solo no fuera suficiente para provocar el disparo. [14]
La neurotransmisión implica tanto una convergencia como una divergencia de información. Primero, una neurona está influenciada por muchas otras, lo que resulta en una convergencia de entradas. Cuando la neurona se activa, la señal se envía a muchas otras neuronas, lo que da como resultado una divergencia en la salida. Muchas otras neuronas están influenciadas por esta neurona. [ cita necesaria ]
La cotransmisión es la liberación de varios tipos de neurotransmisores desde una única terminal nerviosa .
En la terminal nerviosa, los neurotransmisores están presentes dentro de vesículas recubiertas de membrana de 35 a 50 nm llamadas vesículas sinápticas . Para liberar neurotransmisores, las vesículas sinápticas se acoplan y fusionan transitoriamente en la base de estructuras lipoproteicas especializadas en forma de copa de 10 a 15 nm en la membrana presináptica llamadas porosomas . [15] Se ha resuelto el proteoma del porosoma neuronal , proporcionando la arquitectura molecular y la composición completa de la maquinaria. [16]
Estudios recientes en una gran variedad de sistemas han demostrado que la mayoría, si no todas, las neuronas liberan varios mensajeros químicos diferentes. [17] La cotransmisión permite efectos más complejos en los receptores postsinápticos y, por lo tanto, permite que se produzca una comunicación más compleja entre las neuronas.
En la neurociencia moderna, las neuronas suelen clasificarse según su cotransmisor. Por ejemplo, las "neuronas GABAérgicas" del cuerpo estriado utilizan péptidos opioides o sustancia P como cotransmisor principal.
Algunas neuronas pueden liberar al menos dos neurotransmisores al mismo tiempo, siendo el otro un cotransmisor, para proporcionar la retroalimentación negativa estabilizadora necesaria para una codificación significativa, en ausencia de interneuronas inhibidoras . [18] Los ejemplos incluyen:
La noradrenalina y el ATP son cotransmisores simpáticos . Se ha descubierto que el endocannabinoide anadamida y el cannabinoide WIN 55,212-2 pueden modificar la respuesta general a la estimulación del nervio simpático e indican que los receptores CB1 preuncionales median la acción inhibidora del sistema simpático . Por tanto, los cannabinoides pueden inhibir los componentes noradrenérgicos y purinérgicos de la neurotransmisión simpática. [19]
Un par inusual de cotransmisores es el GABA y el glutamato, que se liberan desde las mismas terminales axónicas de las neuronas que se originan en el área tegmental ventral (VTA), el globo pálido interno y el núcleo supramamilar . [20] Los dos primeros se proyectan hacia la habénula , mientras que se sabe que las proyecciones del núcleo supramamilar se dirigen a la circunvolución dentada del hipocampo. [20]
La neurotransmisión está genéticamente asociada con otras características o rasgos. Por ejemplo, los análisis de enriquecimiento de diferentes vías de señalización llevaron al descubrimiento de una asociación genética con el volumen intracraneal. [21]
Por lo tanto, es concebible que niveles bajos de receptores CB1 estén ubicados en terminales glutamatérgicos y GABAérgicos que inciden en las neuronas DA [127, 214], donde pueden ajustar la liberación de neurotransmisores inhibidores y excitadores y regular la activación de las neuronas DA.
Consistentemente, los experimentos electrofisiológicos in vitro de laboratorios independientes han proporcionado evidencia de la localización del receptor CB1 en las terminales de los axones glutamatérgicos y GABAérgicos en el VTA y SNc.
La interacción directa CB1-HcrtR1 se propuso por primera vez en 2003 (Hilairet et al., 2003). De hecho, se observó un aumento de 100 veces en la potencia de la hipocretina-1 para activar la señalización ERK cuando se coexpresaron CB1 y HcrtR1... En este estudio, se comparó una mayor potencia de la hipocretina-1 para regular el heterómero CB1-HcrtR1. con el homómero HcrtR1-HcrtR1 (Ward et al., 2011b). Estos datos proporcionan una identificación inequívoca de la heteromerización CB1-HcrtR1, que tiene un impacto funcional sustancial. ... La existencia de una interacción entre los sistemas hipocretinérgico y endocannabinoide está fuertemente respaldada por su distribución anatómica parcialmente superpuesta y su papel común en varios procesos fisiológicos y patológicos. Sin embargo, se sabe poco sobre los mecanismos subyacentes a esta interacción. ... Actuando como mensajeros retrógrados, los endocannabinoides modulan las entradas sinápticas glutamatérgicas excitadoras y GABAérgicas inhibidoras en las neuronas dopaminérgicas del VTA y la transmisión de glutamato en la NAc. Por lo tanto, la activación de los receptores CB1 presentes en los terminales de los axones de las neuronas GABAérgicas en el VTA inhibe la transmisión de GABA, eliminando esta entrada inhibidora en las neuronas dopaminérgicas (Riegel y Lupica, 2004). La transmisión sináptica del glutamato en VTA y NAc, principalmente desde neuronas del PFC, está modulada de manera similar por la activación de los receptores CB1 (Melis et al., 2004).