El núcleo subtalámico ( STN ) es un pequeño núcleo en forma de lente en el cerebro donde forma parte, desde un punto de vista funcional, del sistema de ganglios basales . En términos de anatomía, es la mayor parte del subtálamo . Como sugiere su nombre, el núcleo subtalámico se encuentra ventral al tálamo . También es dorsal a la sustancia negra y medial a la cápsula interna . Fue descrito por primera vez por Jules Bernard Luys en 1865, [1] y el término corpus Luysi o cuerpo de Luys todavía se utiliza a veces.
El tipo principal de neurona que se encuentra en el núcleo subtalámico tiene dendritas bastante largas y escasamente espinosas . [2] [3] En las neuronas ubicadas más centralmente, los ejes dendríticos tienen una forma más elipsoidal . [4] Las dimensiones de estos cenadores (1200 μm, 600 μm y 300 μm) son similares en muchas especies, incluidas ratas, gatos, monos y humanos, lo cual es inusual. Sin embargo, el número de neuronas aumenta con el tamaño del cerebro y con las dimensiones externas del núcleo. Las neuronas principales son glutamatérgicas , lo que les confiere una posición funcional particular en el sistema de los ganglios basales. En los seres humanos también hay una pequeña cantidad (alrededor del 7,5%) de interneuronas GABAérgicas que participan en los circuitos locales; sin embargo, los cenadores dendríticos de las neuronas subtalámicas se alejan del borde e interactúan principalmente entre sí. [5]
La estructura del núcleo subtalámico aún no se ha explorado ni comprendido completamente, pero probablemente esté compuesto por varios dominios internos. El núcleo subtalámico de los primates a menudo se divide en tres dominios anatómico-funcionales internos. Sin embargo, este llamado modelo tripartito ha sido debatido porque no explica completamente la complejidad del núcleo subtalámico en la función cerebral. [6] [7]
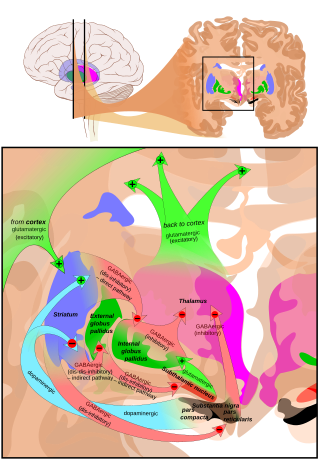
El núcleo subtalámico recibe su aporte principal del globo pálido externo (GPe), [8] no tanto a través del asa lenticular como se suele decir, sino a través de fibras radiantes que cruzan primero el pálido medial y la cápsula interna (ver figura). Estos aferentes son GABAérgicos e inhiben las neuronas en el núcleo subtalámico. Las entradas excitatorias y glutamatérgicas provienen de la corteza cerebral (particularmente la corteza motora) y de la pars parafascicularis del complejo central. El núcleo subtalámico también recibe aferencias neuromoduladoras , en particular axones dopaminérgicos de la sustancia negra pars compacta. [9] También recibe aferencias del núcleo pedunculopontino .
Los axones de las neuronas del núcleo subtalámico abandonan el núcleo en dirección dorsal. Los axones eferentes son glutamatérgicos (excitadores). A excepción de la conexión con el cuerpo estriado (17,3% en macacos), la mayoría de las neuronas principales subtalámicas tienen múltiples objetivos y se dirigen a los demás elementos del núcleo de los ganglios basales. [10] Algunos envían axones a la sustancia negra medialmente y a los núcleos medial y lateral del pálido lateralmente (3 objetivos, 21,3%). Algunos tienen 2 dianas con el pálido lateral y la sustancia negra (2,7%) o el pálido lateral y el medial (48%). Hay menos objetivos únicos para el pálido lateral. En el pálido, las terminales subtalámicas terminan en bandas paralelas al borde pálido. [10] [11] Cuando se suman todos los axones que alcanzan este objetivo, la principal eferencia del núcleo subtalámico es, en el 82,7% de los casos, claramente el globo pálido interno (GPi).
Algunos investigadores han informado sobre garantías internas de axones . [12] Sin embargo, hay poca evidencia funcional para esto.
Los primeros registros eléctricos intracelulares de neuronas subtalámicas se realizaron utilizando electrodos afilados en una preparación de rodajas de rata. [ cita necesaria ] En estas grabaciones se realizaron tres observaciones clave, las cuales han dominado los informes posteriores sobre las propiedades de disparo subtalámico. La primera observación fue que, en ausencia de inyección de corriente o estimulación sináptica, la mayoría de las células se activaban espontáneamente. La segunda observación es que estas células son capaces de dispararse transitoriamente a frecuencias muy altas. La tercera observación se refiere a comportamientos no lineales cuando las células se despolarizan transitoriamente después de hiperpolarizarse por debajo de –65 mV. Luego pueden activar corrientes de calcio y sodio dependientes de voltaje para disparar ráfagas de potenciales de acción.
Varios estudios recientes se han centrado en la capacidad de marcapasos autónomos de las neuronas subtalámicas. Estas células a menudo se denominan "marcapasos de pico rápido", [13] ya que pueden generar potenciales de acción espontáneos a frecuencias de 80 a 90 Hz en primates.
Es probable que la actividad oscilatoria y sincrónica [14] [15] sea un patrón típico de descarga en neuronas subtalámicas registradas en pacientes y modelos animales, caracterizado por la pérdida de células dopaminérgicas en la sustancia negra pars compacta , que es la principal patología que subyace al Parkinson. enfermedad .
Fuertes conexiones recíprocas unen el núcleo subtalámico y el segmento externo del globo pálido . Ambos son marcapasos de aceleración rápida. Juntos, se cree que constituyen el "marcapasos central de los ganglios basales" [16] con explosiones sincrónicas.
La conexión del pálido lateral con el núcleo subtalámico es también la que se encuentra en el sistema de ganglios basales donde la reducción entre los elementos emisores/receptores es probablemente la más fuerte. En términos de volumen, en el ser humano el pálido lateral mide 808 mm 3 , el núcleo subtalámico sólo 158 mm 3 . [17] Esto traducido en número de neuronas representa una fuerte compresión con pérdida de precisión del mapa.
Algunos axones del pálido lateral van al cuerpo estriado. [18] La actividad del pálido medial está influenciada por las aferencias del pálido lateral y del núcleo subtalámico. [19] Lo mismo ocurre con la sustancia negra pars reticulata . [11] El núcleo subtalámico envía axones a otro regulador: el complejo pedúnculo-pontino (id).
Se cree que el sistema lateropallido-subtalámico desempeña un papel clave en la generación de los patrones de actividad observados en la enfermedad de Parkinson . [20]
La estimulación crónica del STN, llamada estimulación cerebral profunda (DBS), se utiliza para tratar a pacientes con enfermedad de Parkinson . Las primeras en ser estimuladas son las arborizaciones terminales de los axones aferentes, que modifican la actividad de las neuronas subtalámicas. Sin embargo, se ha demostrado en cortes talámicos de ratones [21] que el estímulo también hace que los astrocitos cercanos liberen trifosfato de adenosina (ATP), un precursor de la adenosina (a través de un proceso catabólico). A su vez, la activación del receptor de adenosina A1 deprime la transmisión excitatoria en el tálamo, imitando así la ablación del núcleo subtalámico.
La destrucción unilateral o alteración del núcleo subtalámico, que comúnmente puede ocurrir a través de un accidente cerebrovascular de vaso pequeño en pacientes con diabetes, hipertensión o antecedentes de tabaquismo, produce hemibalismo .
Como una de las funciones sospechosas del STN es el control de los impulsos, la disfunción en esta región se ha implicado en el trastorno obsesivo-compulsivo . [22] La estimulación artificial del STN se ha mostrado prometedora para corregir la conducta impulsiva grave y puede usarse más adelante como tratamiento alternativo para el trastorno. [23]
Se desconoce la función del STN, pero las teorías actuales lo sitúan como un componente del sistema de control de los ganglios basales que puede realizar la selección de acciones. Se cree que implementa la llamada "vía hiperdirecta" de control motor, en contraste con las vías directas e indirectas implementadas en otras partes de los ganglios basales. También se ha demostrado que la disfunción STN aumenta la impulsividad en individuos a los que se les presentan dos estímulos igualmente gratificantes. [24]
Las investigaciones han sugerido que el subtálamo es un centro extrapiramidal . Mantiene bajo control las respuestas musculares y el daño puede provocar hemibalismo (un movimiento violento del brazo y la pierna hacia un lado del cuerpo). [25]
El papel fisiológico del STN ha estado oculto durante mucho tiempo por su papel patológico. Pero últimamente, la investigación sobre la fisiología del STN ha llevado al descubrimiento de que el STN es necesario para lograr el movimiento deseado, incluida la locomoción, el equilibrio y la coordinación motora. De hecho, participa en la parada o interrupción de tareas motoras en curso. Además, la excitación de STN generalmente se correlacionó con una reducción significativa de la actividad locomotora, mientras que, por el contrario, la inhibición de STN mejoró la locomoción. [26] [27] [28]