
En la ciencia de los materiales , la microscopía de fuerza química ( CFM ) es una variación de la microscopía de fuerza atómica (AFM) que se ha convertido en una herramienta versátil para la caracterización de superficies de materiales . Con AFM, la morfología estructural se sondea utilizando modos simples de golpeteo o contacto que utilizan interacciones de van der Waals entre la punta y la muestra para mantener una amplitud de deflexión de la sonda constante (modo de fuerza constante) o mantener la altura mientras se mide la deflexión de la punta (modo de altura constante). CFM, por otro lado, utiliza interacciones químicas entre la punta de la sonda funcionalizada y la muestra. La química de elección es típicamente una punta y una superficie recubiertas de oro con tioles R−SH unidos, siendo R los grupos funcionales de interés. CFM permite la capacidad de determinar la naturaleza química de las superficies, independientemente de su morfología específica, y facilita los estudios de la entalpía de enlace químico básico y la energía superficial . Normalmente, CFM está limitado por las vibraciones térmicas dentro del voladizo que sostiene la sonda. Esto limita la resolución de la medición de fuerza a ~1 pN, lo que sigue siendo muy adecuado considerando que las interacciones débiles de COOH/CH 3 son ~20 pN por par. [1] [2] La hidrofobicidad se utiliza como el ejemplo principal a lo largo de esta consideración de CFM, pero ciertamente cualquier tipo de enlace se puede probar con este método.
El CFM fue desarrollado principalmente por Charles Lieber en la Universidad de Harvard en 1994. [1] El método se demostró utilizando hidrofobicidad donde las moléculas polares (por ejemplo, COOH) tienden a tener la unión más fuerte entre sí, seguidas por la unión no polar (por ejemplo, CH 3 -CH 3 ), y una combinación es la más débil. Las puntas de la sonda se funcionalizan y los sustratos se modelan con estas moléculas. Se probaron todas las combinaciones de funcionalización, tanto por contacto y eliminación de la punta como por mapeo espacial de sustratos modelados con ambas fracciones y observando la complementariedad en el contraste de la imagen. Ambos métodos se analizan a continuación. El instrumento AFM utilizado es similar al de la Figura 1.
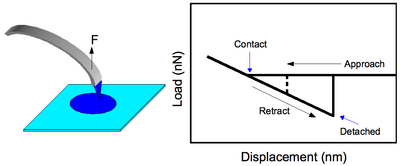
Este es el modo más simple de operación de CFM, donde una punta funcionalizada se pone en contacto con la superficie y se tira de ella para observar la fuerza con la que se produce la separación ( ver Figura 2). La teoría de la mecánica de adhesión de Johnson-Kendall-Roberts (JKR) predice este valor como [1] [2]
(1)
donde con siendo el radio de la punta, y siendo varias energías superficiales entre la punta, la muestra y el medio en el que se encuentra cada una (líquidos discutidos a continuación). generalmente se obtiene de SEM y y de mediciones del ángulo de contacto en sustratos con las fracciones dadas. Cuando se usan los mismos grupos funcionales, y lo que resulta en Hacer esto dos veces con dos fracciones diferentes (por ejemplo, COOH y CH 3 ) da valores de y , los cuales pueden usarse juntos en el mismo experimento para determinar . Por lo tanto, se puede calcular para cualquier combinación de funcionalidades para comparar con los valores determinados por CFM.
Para una punta y una superficie funcionalizadas de manera similar, en el desprendimiento de la punta, la teoría JKR también predice un radio de contacto de [2]
(2)
con un módulo de Young "efectivo" de la punta derivado del valor real y la relación de Poisson . Si uno conoce el área efectiva de un solo grupo funcional, (por ejemplo, a partir de simulaciones de química cuántica), el número total de ligandos que participan en la tensión se puede estimar como Como se dijo anteriormente, la resolución de fuerza de CFM permite probar enlaces individuales incluso de la variedad más débil, pero la curvatura de la punta generalmente lo impide. Usando la ecuación 2, se ha determinado un radio de curvatura < 10 nm como el requisito para realizar pruebas de tracción de fracciones lineales individuales. [2]
Una nota rápida para mencionar es que el trabajo correspondiente a la histéresis en el perfil de fuerza (Figura 2) no se correlaciona con la energía de enlace. El trabajo realizado al retraer la punta se aproxima debido al comportamiento lineal de la deformación, donde es la fuerza y es el desplazamiento inmediatamente antes de la liberación. Usando los resultados de Frisbie et al., [1] normalizados a los 50 grupos funcionales estimados en contacto, los valores de trabajo se estiman en 39 eV, 0.25 eV y 4.3 eV para las interacciones COOH/COOH , COOH/CH 3 y CH 3 /CH 3 , respectivamente. Aproximadamente, las energías de enlace intermolecular se pueden calcular mediante: es el punto de ebullición. Según esto, = 32,5 meV para el ácido fórmico , HCOOH , y 9,73 meV para el metano , CH 4 , siendo cada valor aproximadamente 3 órdenes de magnitud menor de lo que el experimento podría sugerir. Incluso si se considerara la pasivación de la superficie con EtOH (discutida más adelante), el gran error parece irrecuperable. Los enlaces de hidrógeno más fuertes tienen como máximo ~1 eV de energía. [3] Esto implica fuertemente que el voladizo tiene una constante de fuerza menor o del orden de la de las interacciones de enlace y, por lo tanto, no puede tratarse como perfectamente rígido. Esto abre una vía para aumentar la utilidad de CFM si se pueden usar voladizos más rígidos manteniendo al mismo tiempo la resolución de fuerza.
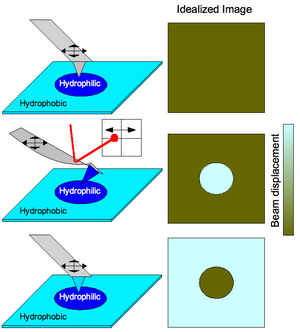
Las interacciones químicas también se pueden utilizar para mapear sustratos preestampados con funcionalidades variables (ver Figura 3). El escaneo de una superficie que tiene hidrofobicidad variable con una punta que no tiene grupos funcionales unidos produciría una imagen sin contraste porque la superficie no tiene características morfológicas (operación AFM simple). La funcionalización de una punta para que sea hidrófila haría que el voladizo se doblara cuando la punta escanea a través de porciones hidrófilas del sustrato debido a fuertes interacciones punta-sustrato. Esto se detecta por deflexión láser en un detector sensible a la posición , produciendo así una imagen de perfil químico de la superficie. Generalmente, un área más brillante correspondería a una mayor amplitud de deflexión, por lo que una unión más fuerte corresponde a áreas más claras de un mapa de imagen CFM. Cuando la funcionalización del voladizo se cambia de modo que la punta se dobla cuando encuentra áreas hidrófobas del sustrato, se observa la imagen complementaria.
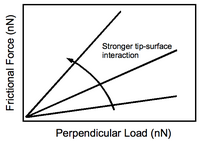
La respuesta de la fuerza de fricción a la cantidad de carga perpendicular aplicada por la punta sobre el sustrato se muestra en la Figura 4. El aumento de las interacciones punta-sustrato produce una pendiente más pronunciada, como cabría esperar. El hecho de que el contraste entre las diferentes funcionalidades de la superficie se puede mejorar con una aplicación de mayor fuerza perpendicular es de importancia experimental. Por supuesto, esto se produce a costa de posibles daños al sustrato.
La fuerza capilar es un problema importante en las mediciones de fuerza de tracción, ya que refuerza efectivamente la interacción punta-superficie. Por lo general, es causada por la humedad adsorbida en sustratos del entorno ambiental. Para eliminar esta fuerza adicional, se pueden realizar mediciones en líquidos. Con la punta y el sustrato terminados en X en el líquido L, la adición a F ad se calcula utilizando la ecuación 1 con W XLX = 2γ LL ; es decir, la fuerza adicional proviene de la atracción de las moléculas del líquido entre sí. Esto es ~10 pN para EtOH, lo que aún permite la observación incluso de las interacciones polares/apolares más débiles (~20 pN). [2] La elección del líquido depende de qué interacciones sean de interés. Cuando el solvente es inmiscible con grupos funcionales, existe un enlace punta-superficie más grande de lo habitual. Por lo tanto, los solventes orgánicos son apropiados para estudiar van der Waals y el enlace de hidrógeno, mientras que los electrolitos son mejores para investigar las fuerzas hidrofóbicas y electrostáticas.

Una implementación biológica del CFM a escala nanométrica es el desdoblamiento de proteínas con la punta y la superficie funcionalizadas (véase la Figura 5). [4] Debido al aumento del área de contacto, la punta y la superficie actúan como anclas que sostienen los haces de proteínas mientras se separan. A medida que se produce el desenrollado, la fuerza necesaria aumenta, lo que indica varias etapas de desenrollado: (1) separación en haces, (2) separación de los haces en dominios de proteína cristalina unidos por fuerzas de van der Waals, y (3) linealización de la proteína al superar el enlace secundario. Con este método se proporciona información sobre la estructura interna de estas proteínas complejas, así como una mejor comprensión de las interacciones constituyentes.
Una segunda consideración es la que aprovecha las propiedades únicas de los materiales a nanoescala. La alta relación de aspecto de los nanotubos de carbono (fácilmente >1000) se explota para obtener imágenes de superficies con características profundas. [5] El uso del material de carbono amplía la química de funcionalización, ya que existen innumerables rutas para la modificación química de las paredes laterales de los nanotubos (por ejemplo, con diazonio, alquilos simples, hidrógeno, ozono/oxígeno y aminas). Los nanotubos de paredes múltiples se utilizan típicamente por su rigidez. Debido a sus extremos aproximadamente planos, se puede estimar el número de grupos funcionales que están en contacto con el sustrato conociendo el diámetro del tubo y el número de paredes, lo que ayuda a determinar las propiedades de tracción de la fracción individual. Ciertamente, este método también tiene implicaciones obvias en la tribología .