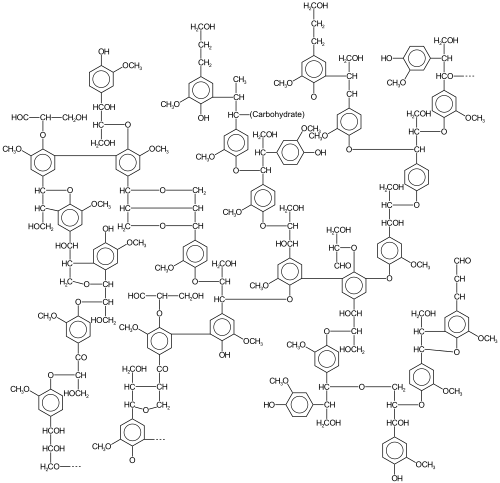
La lignina es una clase de polímeros orgánicos complejos que forman materiales estructurales clave en los tejidos de soporte de la mayoría de las plantas. [1] Las ligninas son particularmente importantes en la formación de las paredes celulares , especialmente en la madera y la corteza , porque aportan rigidez y no se pudren fácilmente. Químicamente, las ligninas son polímeros obtenidos mediante la reticulación de precursores fenólicos . [2]
La lignina fue mencionada por primera vez en 1813 por el botánico suizo AP de Candolle , quien la describió como un material fibroso, insípido, insoluble en agua y alcohol pero soluble en soluciones alcalinas débiles, y que puede precipitarse de una solución usando ácido. [3] Llamó a la sustancia "ligina", que se deriva de la palabra latina lignum , [4] que significa madera. Es uno de los polímeros orgánicos más abundantes en la Tierra , superado sólo por la celulosa y la quitina . La lignina constituye el 30% del carbono orgánico terrestre no fósil [5] de la Tierra y entre el 20 y el 35% de la masa seca de la madera. [6]
La lignina está presente en las algas rojas , lo que sugiere que el ancestro común de las plantas y las algas rojas también sintetizó lignina. Este hallazgo también sugiere que la función original de la lignina era estructural, ya que desempeña este papel en el alga roja Calliarthron , donde sostiene las articulaciones entre segmentos calcificados . [7]
La composición de la lignina varía de una especie a otra. Un ejemplo de composición de una muestra de álamo temblón [8] es 63,4% carbono, 5,9% hidrógeno, 0,7% cenizas (componentes minerales) y 30% oxígeno (por diferencia), [9] correspondiente aproximadamente a la fórmula (C 31 H 34 O 11 ) norte .
La lignina es una colección de polímeros altamente heterogéneos derivados de un puñado de lignoles precursores. La heterogeneidad surge de la diversidad y el grado de reticulación entre estos lignoles. Los lignoles que se reticulan son de tres tipos principales, todos derivados del fenilpropano: alcohol coniferílico (3-metoxi-4-hidroxifenilpropano; su radical, G, a veces se llama guaiacilo), alcohol sinapílico (3,5-dimetoxi-4-hidroxifenilpropano; su radical, S, a veces se llama siringilo) y alcohol paracumarílico (4-hidroxifenilpropano; su radical, H, a veces se llama 4-hidroxifenilo). [ cita necesaria ]
Las cantidades relativas de los "monómeros" precursores (lignoles o monolignoles) varían según la fuente vegetal. [5] Las ligninas generalmente se clasifican según su proporción siringilo/guaiacilo (S/G). La lignina de las gimnospermas se deriva del alcohol coniferílico , que da lugar a G tras la pirólisis. En las angiospermas, parte del alcohol coniferílico se convierte en S. Por tanto, la lignina en las angiospermas tiene componentes tanto G como S. [10] [11]
Las masas moleculares de la lignina superan las 10.000 u . Es hidrófobo ya que es rico en subunidades aromáticas . El grado de polimerización es difícil de medir, ya que el material es heterogéneo. Se han descrito diferentes tipos de lignina según el medio de aislamiento. [12]

Muchos pastos tienen principalmente G, mientras que algunas palmas tienen principalmente S. [13] Todas las ligninas contienen pequeñas cantidades de monolignoles incompletos o modificados, y otros monómeros son prominentes en las plantas no leñosas. [14]
La lignina llena los espacios en la pared celular entre los componentes de celulosa , hemicelulosa y pectina , especialmente en los tejidos vasculares y de soporte: traqueidas del xilema , elementos vasculares y células esclereidas . [ cita necesaria ]
La lignina juega un papel crucial en la conducción de agua y nutrientes acuosos en los tallos de las plantas . Los componentes polisacáridos de las paredes celulares de las plantas son altamente hidrófilos y, por tanto, permeables al agua, mientras que la lignina es más hidrófoba . La reticulación de polisacáridos por la lignina es un obstáculo para la absorción de agua en la pared celular. Así, la lignina hace posible que el tejido vascular de la planta conduzca el agua de manera eficiente. [15] La lignina está presente en todas las plantas vasculares , pero no en las briófitas , lo que respalda la idea de que la función original de la lignina estaba restringida al transporte de agua.
Está unido covalentemente a la hemicelulosa y por tanto entrecruza diferentes polisacáridos vegetales , confiriendo resistencia mecánica a la pared celular y por extensión a la planta en su conjunto. [16] Su función más comúnmente observada es el soporte mediante el fortalecimiento de la madera (compuesta principalmente por células del xilema y fibras de esclerénquima lignificadas ) en las plantas vasculares. [17] [18] [19]
Finalmente, la lignina también confiere resistencia a las enfermedades al acumularse en el sitio de infiltración del patógeno, lo que hace que la célula vegetal sea menos accesible a la degradación de la pared celular. [20]

La producción comercial mundial de lignina es consecuencia de la fabricación de papel. En 1988 se produjeron en todo el mundo más de 220 millones de toneladas de papel. [21] Gran parte de este artículo fue deshonrado; la lignina comprende aproximadamente 1/3 de la masa de lignocelulosa, el precursor del papel. La lignina es un impedimento para la fabricación de papel ya que tiene color, amarillea en el aire y su presencia debilita el papel. Una vez separada de la celulosa, se quema como combustible. Sólo una fracción se utiliza en una amplia gama de aplicaciones de bajo volumen donde la forma pero no la calidad es importante. [22]
La pulpa mecánica o de alto rendimiento , que se utiliza para fabricar papel de periódico , todavía contiene la mayor parte de la lignina presente originalmente en la madera. Esta lignina es responsable del color amarillento del papel de periódico con el tiempo. [4] El papel de alta calidad requiere la eliminación de la lignina de la pulpa. Estos procesos de deslignificación son tecnologías centrales de la industria de fabricación de papel, así como la fuente de importantes preocupaciones ambientales. [ cita necesaria ]
En la fabricación de pulpa al sulfito , la lignina se elimina de la pulpa de madera en forma de lignosulfonatos , para los cuales se han propuesto muchas aplicaciones. [23] Se utilizan como dispersantes , humectantes , estabilizadores de emulsión y secuestrantes ( tratamiento de agua ). [24] El lignosulfonato también fue la primera familia de reductores de agua o superplastificantes que se agregaron en la década de 1930 como mezcla al concreto fresco para disminuir la relación agua-cemento ( w/c ), el principal parámetro que controla la porosidad del concreto . y por tanto su resistencia mecánica , su difusividad y su conductividad hidráulica , todos parámetros esenciales para su durabilidad. Tiene aplicación como agente supresor de polvo ambientalmente sostenible para carreteras. Además, la lignina se puede utilizar para fabricar plástico biodegradable junto con celulosa como alternativa a los plásticos fabricados con hidrocarburos si la extracción de lignina se logra mediante un proceso más viable desde el punto de vista ambiental que la fabricación de plástico genérico. [25]
La lignina extraída mediante el proceso kraft generalmente se quema para obtener su valor como combustible, proporcionando energía para impulsar la fábrica de papel. Existen dos procesos comerciales para eliminar la lignina del licor negro para usos de mayor valor: LignoBoost (Suecia) y LignoForce (Canadá). La lignina de mayor calidad presenta el potencial de convertirse en una fuente renovable de compuestos aromáticos para la industria química, con un mercado direccionable de más de 130.000 millones de dólares. [26]
Dado que es el biopolímero más frecuente después de la celulosa , la lignina ha sido investigada como materia prima para la producción de biocombustibles y puede convertirse en un extracto vegetal crucial en el desarrollo de una nueva clase de biocombustibles. [27] [28]
La biosíntesis de lignina comienza en el citosol con la síntesis de monolignoles glicosilados a partir del aminoácido fenilalanina . Estas primeras reacciones se comparten con la vía de los fenilpropanoides . La glucosa adjunta los hace solubles en agua y menos tóxicos . Una vez transportada a través de la membrana celular hasta el apoplasto , la glucosa se elimina y comienza la polimerización. [29] Gran parte de su anabolismo no se comprende incluso después de más de un siglo de estudio. [5]

La etapa de polimerización , es decir, un acoplamiento radical-radical, está catalizada por enzimas oxidativas . Tanto las enzimas peroxidasa como lacasa están presentes en las paredes celulares de las plantas y no se sabe si uno o ambos grupos participan en la polimerización. También podrían estar implicados oxidantes de bajo peso molecular. La enzima oxidativa cataliza la formación de radicales monolignol . A menudo se dice que estos radicales experimentan un acoplamiento no catalizado para formar el polímero de lignina . [30] Una teoría alternativa invoca un control biológico no especificado. [1]
A diferencia de otros biopolímeros (p. ej. proteínas, ADN e incluso celulosa), la lignina resiste la degradación. Es inmune a la hidrólisis catalizada tanto por ácidos como por bases. La degradabilidad varía según la especie y el tipo de tejido vegetal. Por ejemplo, la lignina siringilo (S) es más susceptible a la degradación por descomposición fúngica, ya que tiene menos enlaces aril-arilo y un potencial redox más bajo que las unidades guaiacilo. [31] [32] Debido a que está entrecruzada con otros componentes de la pared celular, la lignina minimiza la accesibilidad de la celulosa y la hemicelulosa a las enzimas microbianas, lo que lleva a una digestibilidad reducida de la biomasa. [15]
Algunas enzimas ligninolíticas incluyen hemo peroxidasas como lignina peroxidasas , manganeso peroxidasas , peroxidasas versátiles y peroxidasas decolorantes de tintes , así como lacasas a base de cobre . Las lignina peroxidasas oxidan la lignina no fenólica, mientras que las peroxidasas de manganeso solo oxidan las estructuras fenólicas. Las peroxidasas decolorantes de tintes, o DyP, exhiben actividad catalítica en una amplia gama de compuestos modelo de lignina, pero se desconoce su sustrato in vivo . En general, las lacasas oxidan sustratos fenólicos, pero se ha demostrado que algunas lacasas fúngicas oxidan sustratos no fenólicos en presencia de mediadores redox sintéticos. [33] [34]
En Phanerochaete chrysosporium [35] y otros hongos de pudrición blanca se encuentran enzimas ligninolíticas bien estudiadas . Algunos hongos de pudrición blanca, como Ceriporiopsis subvermispora , pueden degradar la lignina de la lignocelulosa , pero otros carecen de esta capacidad. La mayor parte de la degradación de la lignina por hongos implica la secreción de peroxidasas . También se secretan muchas lacasas fúngicas , que facilitan la degradación de compuestos fenólicos derivados de la lignina, aunque también se han descrito varias lacasas fúngicas intracelulares. Un aspecto importante de la degradación de la lignina fúngica es la actividad de enzimas accesorias para producir el H 2 O 2 necesario para la función de la lignina peroxidasa y otras hemo peroxidasas . [33]
Las bacterias carecen de la mayoría de las enzimas empleadas por los hongos para degradar la lignina y los derivados de la lignina (ácidos alifáticos, furanos y fenólicos solubilizados) inhiben el crecimiento de las bacterias. [36] Sin embargo, la degradación bacteriana puede ser bastante extensa, [37] especialmente en sistemas acuáticos como lagos, ríos y arroyos, donde los aportes de material terrestre (por ejemplo, hojarasca ) pueden ingresar a los cursos de agua. La actividad ligninolítica de las bacterias no se ha estudiado extensamente a pesar de que se describió por primera vez en 1930. Se han caracterizado muchas DyP bacterianas. Las bacterias no expresan ninguna de las peroxidasas de tipo vegetal (lignina peroxidasa, Mn peroxidasa o peroxidasas versátiles), pero tres de las cuatro clases de DyP solo se encuentran en bacterias. A diferencia de los hongos, la mayoría de las enzimas bacterianas involucradas en la degradación de la lignina son intracelulares, incluidas dos clases de DyP y la mayoría de las lacasas bacterianas. [34]
En el medio ambiente, la lignina se puede degradar bióticamente a través de bacterias o abióticamente mediante alteración fotoquímica y, a menudo, esta última ayuda a la primera. [38] Además de la presencia o ausencia de luz, varios factores ambientales afectan la biodegradabilidad de la lignina, incluida la composición de la comunidad bacteriana, las asociaciones minerales y el estado redox. [39] [40]
En los gusanos de barco , la lignina que ingiere es digerida por bacterias simbiontes del " subgrupo similar a Alteromonas " en el subórgano tiflosol de su ciego . [41]
La pirólisis de la lignina durante la combustión de la madera o la producción de carbón vegetal produce una variedad de productos, de los cuales los más característicos son los fenoles metoxi sustituidos . De ellos, los más importantes son el guaiacol y el siringol y sus derivados. Su presencia puede utilizarse para rastrear una fuente de humo hasta un fuego de leña. En la cocina , la lignina en forma de madera dura es una fuente importante de estos dos compuestos, que imparten el aroma y el sabor característicos a los alimentos ahumados como la barbacoa . Los principales compuestos aromáticos del jamón ahumado son el guaiacol y sus derivados 4, 5 y 6 metílicos, así como el 2,6-dimetilfenol. Estos compuestos se producen por degradación térmica de la lignina de la madera utilizada en el ahumadero. [42]
El método convencional para la cuantificación de lignina en la industria de la celulosa es la prueba de lignina Klason y lignina soluble en ácido, que es un procedimiento estandarizado. La celulosa se digiere térmicamente en presencia de ácido. El residuo se denomina lignina Klason. La lignina soluble en ácido (ASL) se cuantifica mediante la intensidad de su espectroscopia ultravioleta . También se puede analizar la composición de carbohidratos de los licores Klason, aunque pueden existir productos de degradación de azúcares (furfural y 5-hidroximetilfurfural ). [43]
Para la detección de lignina se utiliza una solución de ácido clorhídrico y floroglucinol (prueba de Wiesner). Se desarrolla un color rojo brillante debido a la presencia de grupos coniferaldehído en la lignina. [44]
La tioglucólisis es una técnica analítica para la cuantificación de lignina . [45] La estructura de la lignina también se puede estudiar mediante simulación computacional. [46]
La termoquimiolisis (descomposición química de una sustancia al vacío y a alta temperatura) con hidróxido de tetrametilamonio (TMAH) u óxido cúprico [47] también se ha utilizado para caracterizar las ligninas. La proporción de siringil lignol (S) a vanilil lignol (V) y cinamil lignol (C) a vanilil lignol (V) es variable según el tipo de planta y, por lo tanto, se puede utilizar para rastrear fuentes de plantas en sistemas acuáticos (leñosos versus no leñosos). leñosas y angiospermas versus gimnospermas). [48] Las proporciones de las formas de ácido carboxílico (Ad) a aldehído (Al) de los lignoles (Ad/Al) revelan información diagenética, y las proporciones más altas indican un material más altamente degradado. [31] [32] Los aumentos en el valor (Ad/Al) indican que se ha producido una reacción de escisión oxidativa en la cadena lateral de alquillignina, que se ha demostrado que es un paso en la descomposición de la madera en muchos casos de pudrición blanca y algunos de pudrición blanda. hongos . [31] [32] [49] [50] [51]
La lignina y sus modelos han sido bien examinados mediante espectroscopia de RMN de 1 H y 13 C. Debido a la complejidad estructural de las ligninas, los espectros están mal resueltos y la cuantificación es un desafío. [52]