El lamellipodium ( pl.: lamellipodia ) (del latín lamella , relacionado con lámina , "lámina delgada", y el radical griego pod- , "pie") es una proteína citoesquelética de actina que se proyecta en el borde anterior de la célula . Contiene una malla de actina casi bidimensional; toda la estructura impulsa a la célula a través de un sustrato. [1] Dentro de los lamellipodios hay costillas de actina llamadas micropuntas , que, cuando se extienden más allá de la frontera del lamellipodium, se denominan filopodios . [2] El lamellipodio nace de la nucleación de actina en la membrana plasmática de la célula [1] y es el área principal de incorporación de actina o formación de microfilamentos de la célula.
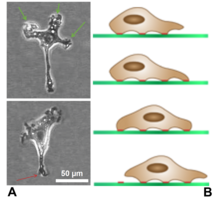
Los lamellipodios se encuentran principalmente en todas las células móviles, como los queratinocitos de peces y ranas, que participan en la rápida reparación de las heridas . Los lamellipodios de estos queratinocitos les permiten moverse a velocidades de 10 a 20 μm/min sobre las superficies epiteliales . Cuando se separa de la parte principal de una célula, un lamelipodio todavía puede arrastrarse libremente por sí solo.
Los lamellipodia son un rasgo característico en el borde frontal, de ataque, de las células móviles. Se cree que son el motor real que impulsa la célula hacia adelante durante el proceso de migración celular . La punta del lamellipodium es el sitio donde se produce la exocitosis en las células de mamíferos migratorias como parte de su ciclo endocítico mediado por clatrina . Esto, junto con la polimerización de actina allí, ayuda a extender la laminilla hacia adelante y así hacer avanzar el frente de la célula. Por tanto, actúa como un dispositivo de dirección para las células en el proceso de quimiotaxis . También es el sitio desde donde migran las partículas o agregados adheridos a la superficie celular en un proceso conocido como formación de capa .
Estructuralmente, los extremos con púas de los microfilamentos ( monómeros de actina localizados en forma unida a ATP ) miran hacia el borde "de búsqueda" de la célula, mientras que los extremos puntiagudos (monómeros de actina localizados en forma unida a ADP ) miran hacia la laminilla detrás. [4] Esto crea una cinta de correr a lo largo del lamellipodio, lo que ayuda en el flujo retrógrado de partículas. [4] Los complejos Arp2/3 están presentes en las uniones microfilamento-microfilamento en los lamellipodios y ayudan a crear la red de actina. Arp2/3 solo puede unirse a microfilamentos previamente existentes, pero una vez unido crea un sitio para la extensión de nuevos microfilamentos, lo que crea ramificaciones. [5] Otra molécula que se encuentra a menudo en la polimerización de actina con Arp2/3 es la cortactina , que parece vincular la señalización de la tirosina quinasa con la reorganización del citoesqueleto en el lamellipodio y sus estructuras asociadas. [5]
Rac y Cdc42 son dos GTPasas de la familia Rho que normalmente son citosólicas pero que también pueden encontrarse en la membrana celular bajo ciertas condiciones. [2] Cuando se activa Cdc42, puede interactuar con los receptores de la familia de proteínas del síndrome de Wiskott-Aldrich (WASp), en particular N-WASp , que luego activa Arp2/3. Esto estimula la ramificación de actina y aumenta la motilidad celular . [2] Rac1 induce que cortactina se localice en la membrana celular, donde se une simultáneamente a la actina F y a Arp2/3. El resultado es una reorganización estructural del lamellipodium y la consiguiente motilidad celular. [5] Rac promueve lamellipodia mientras que cdc42 promueve filopodios. [6]
Las proteínas Ena/VASP se encuentran en el borde de ataque de los lamelipodios, donde promueven la polimerización de actina necesaria para la protrusión lamelipodial y la quimiotaxis. Además, Ena/VASP previene la acción de la proteína bloqueadora , que detiene la polimerización de actina. [7]