Una fragmentación de Grob es una reacción de eliminación que rompe una cadena alifática neutra en tres fragmentos: un ion positivo que abarca los átomos 1 y 2 (el " electrófugo "), un fragmento neutro insaturado que abarca las posiciones 3 y 4, y un ion negativo (el " nucleófugo ") que comprende el resto de la cadena. [1] [2] [3]
Por ejemplo, el ion positivo puede ser un ion carbenio , carbonio o acilio ; el fragmento neutro podría ser un alqueno , alquino o imina ; y el fragmento negativo podría ser un ion tosilo o hidroxilo :

La reacción debe su nombre al químico suizo Cyril A. Grob .
Alternativamente, el átomo 1 podría comenzar como un anión, en cuyo caso se vuelve neutral en lugar de pasar de neutral a catiónico.
Un ejemplo temprano de fragmentación es la deshidratación de di(terc-butil)metanol que produce 2-metil-2-buteno e isobuteno , una reacción descrita en 1933 por Frank C. Whitmore . [4] Esta reacción se produce mediante la formación de un carbocatión secundario seguida de una reacción de reordenamiento a un carbocatión terciario más estable y la eliminación de un catión t -butilo:

Albert Eschenmoser en 1952 investigó la fragmentación catalizada por bases de ciertas betahidroxicetonas : [5]

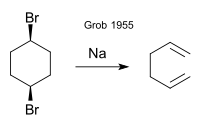
El trabajo original de Grob (1955) trata de la formación de 1,5-hexadieno a partir de cis - o trans -1,4-dibromociclohexano por sodio metálico: [1]
Según los revisores Prantz y Mulzer (2010), el nombre de fragmentación de Grob fue elegido "en un desprecio más o menos evidente por las contribuciones anteriores". [6]
El mecanismo de reacción varía con el reactivo y las condiciones de reacción, y la fragmentación se produce en una reacción concertada o en dos pasos con un intermediario carbocatiónico cuando el nucleófugo sale primero, o en dos pasos con un intermediario aniónico cuando el electrofugo sale primero. La vía carbaniónica es más común y se ve facilitada por la estabilidad del catión formado y la capacidad del nucleófugo para formar grupos salientes. Con sustratos cíclicos, la geometría preferida de eliminación es que el enlace sigma que expulsa al grupo saliente sea anti a él, de manera análoga a la orientación conformacional en el mecanismo E2 de las reacciones de eliminación .
Un ejemplo de una fragmentación tipo Grob en la síntesis orgánica es la expansión de la cetona de Wieland-Miescher a thapsigargina : [7]

En esta reacción, la reducción diastereoselectiva de la cetona 1 con borohidruro de sodio produce el alcohol 2 , que se funcionaliza al mesilato 3 con cloruro de mesilo en piridina . La selectividad de la reducción inicial de la cetona 1 es el resultado del borohidruro que se acerca desde la cara inferior para evitar el choque estérico con el grupo metilo axial. Luego, la reducción de la enona al alcohol alílico 4 con hidruro de tri- terc -butoxialuminio en tetrahidrofurano seguida de hidroboración con borano en THF produce el borano 5 (solo se muestra un sustituyente para mayor claridad). La diastereoselectividad de la hidroboración es el resultado de dos factores: evitar el grupo metilo axial, así como la adición axial de hidruro para evitar una conformación de barco torcido en el estado de transición . La fragmentación de Grob a 6 tiene lugar con metóxido de sodio en metanol a reflujo . Un grupo metóxido ataca al átomo de boro dando un complejo de borato que se fragmenta. Como cada átomo de boro puede contener tres moléculas de sustrato (R), el subproducto final del boro es el borato de trimetilo . Como se ve en la figura 6 , el mesilato, al estar en posición ecuatorial, permite que su orbital de estrella sigma se alinee idealmente con el enlace sigma dibujado, lo que permite la geometría correcta de la olefina que se ve en la figura 7 .
Otro ejemplo es una reacción de fragmentación de alcohol epoxi como parte de la síntesis total de Holton Taxol .
La fragmentación de 3-aza-Grob es una variación que tiene lugar cuando una electrófuga y una nucleófuga se sitúan en las posiciones 1 y 5 de una cadena de amina secundaria o terciaria con el nitrógeno en la posición 3. [8] [9] Los productos de la reacción son un fragmento electrófugo, una imina y un fragmento nucleófugo (como un alcohol).

La fragmentación de 3-aza-Grob puede realizarse con varios nucleófugos diferentes. Se ha informado que el mecanismo de reacción comienza con la reducción de una amida protegida con éter para formar un alcohol secundario. Luego, la fragmentación tiene lugar en un paso concertado para formar los productos de reacción.

Se ha descubierto que el alcance de la reacción cubre los grupos protectores de THF y tetrahidrotiofeno utilizando varios agentes hidruro. [10]