
La cromatografía de gases-espectrometría de masas ( GC-MS ) es un método analítico que combina las características de la cromatografía de gases y la espectrometría de masas para identificar diferentes sustancias dentro de una muestra de prueba. [1] Las aplicaciones de GC-MS incluyen detección de drogas , investigación de incendios , análisis ambiental, investigación de explosivos , análisis de alimentos y sabores e identificación de muestras desconocidas, incluidas muestras de materiales obtenidas del planeta Marte durante misiones de sonda ya en la década de 1970. GC-MS también se puede utilizar en la seguridad de los aeropuertos para detectar sustancias en el equipaje o en seres humanos. Además, puede identificar oligoelementos en materiales que antes se pensaba que se habían desintegrado más allá de la identificación. Al igual que la cromatografía líquida-espectrometría de masas , permite el análisis y la detección incluso de pequeñas cantidades de una sustancia. [2]
GC-MS se ha considerado como un " estándar de oro " para la identificación forense de sustancias porque se utiliza para realizar una prueba 100% específica , que identifica positivamente la presencia de una sustancia en particular. Una prueba no específica simplemente indica que está presente alguna de varias sustancias de una categoría. Aunque una prueba no específica podría sugerir estadísticamente la identidad de la sustancia, esto podría dar lugar a una identificación falsamente positiva . Sin embargo, las altas temperaturas (300 °C) utilizadas en el puerto de inyección (y el horno) del GC-MS pueden provocar la degradación térmica de las moléculas inyectadas, [3] lo que da lugar a la medición de productos de degradación en lugar de las moléculas reales. de interés.
El primer acoplamiento en línea de cromatografía de gases a un espectrómetro de masas se informó a finales de la década de 1950. [4] [5] Ya en diciembre de 1954 se había sugerido un interés en acoplar los métodos. [6] El desarrollo de computadoras miniaturizadas y asequibles ha ayudado a simplificar el uso de este instrumento, además de permitir grandes mejoras en la cantidad de tiempo que lleva analizar una muestra. En 1964, Electronic Associates, Inc. (EAI) , un importante proveedor estadounidense de computadoras analógicas, comenzó el desarrollo de un espectrómetro de masas cuadrupolo controlado por computadora bajo la dirección de Robert E. Finnigan . [7] En 1966, la división EAI de Finnigan y su colaborador Mike Uthe había vendido más de 500 instrumentos analizadores de gases residuales cuadrupolos. [7] En 1967, Finnigan dejó EAI para formar Finnigan Instrument Corporation junto con Roger Sant, TZ Chou, Michael Story, Lloyd Friedman y William Fies. [8] A principios de 1968, entregaron el primer prototipo de instrumentos GC/MS de cuadrupolo a Stanford y la Universidad Purdue. [7] Cuando Finnigan Instrument Corporation fue adquirida por Thermo Instrument Systems (más tarde Thermo Fisher Scientific ) en 1990, se la consideraba "el principal fabricante mundial de espectrómetros de masas". [9]

El GC-MS se compone de dos componentes principales: el cromatógrafo de gases y el espectrómetro de masas . El cromatógrafo de gases utiliza una columna capilar cuyas propiedades con respecto a la separación de moléculas dependen de las dimensiones de la columna (longitud, diámetro, espesor de la película) así como de las propiedades de las fases (por ejemplo, 5% de fenilpolisiloxano). La diferencia en las propiedades químicas entre diferentes moléculas en una mezcla y su afinidad relativa por la fase estacionaria de la columna promoverá la separación de las moléculas a medida que la muestra viaja a lo largo de la columna. Las moléculas son retenidas por la columna y luego eluyen (se desprenden) de la columna en diferentes momentos (llamado tiempo de retención), y esto permite que el espectrómetro de masas aguas abajo capture, ionice, acelere, desvíe y detecte las moléculas ionizadas por separado. El espectrómetro de masas hace esto rompiendo cada molécula en fragmentos ionizados y detectando estos fragmentos utilizando su relación masa-carga.

Estos dos componentes, utilizados juntos, permiten un grado mucho más preciso de identificación de sustancias que cualquiera de las unidades utilizadas por separado. No es posible realizar una identificación precisa de una molécula en particular mediante cromatografía de gases o espectrometría de masas únicamente. El proceso de espectrometría de masas normalmente requiere una muestra muy pura, mientras que la cromatografía de gases que utiliza un detector tradicional (por ejemplo, detector de ionización de llama ) no puede diferenciar entre múltiples moléculas que tardan la misma cantidad de tiempo en viajar a través de la columna ( es decir, tienen el mismo tiempo de retención). , lo que da como resultado dos o más moléculas que coeluyen. A veces, dos moléculas diferentes también pueden tener un patrón similar de fragmentos ionizados en un espectrómetro de masas (espectro de masas). La combinación de los dos procesos reduce la posibilidad de error, ya que es extremadamente improbable que dos moléculas diferentes se comporten de la misma manera tanto en un cromatógrafo de gases como en un espectrómetro de masas. Por lo tanto, cuando aparece un espectro de masas identificador en un tiempo de retención característico en un análisis GC-MS, generalmente aumenta la certeza de que el analito de interés está en la muestra.
Para el análisis de compuestos volátiles , se puede utilizar un sistema concentrador de purga y trampa (P&T) para introducir muestras. Los analitos objetivo se extraen mezclando la muestra con agua y purgándolos con gas inerte (p. ej., gas nitrógeno ) en una cámara hermética; esto se conoce como purga o burbujeo . Los compuestos volátiles se mueven hacia el espacio superior sobre el agua y son arrastrados a lo largo de un gradiente de presión (causado por la introducción del gas de purga) fuera de la cámara. Los compuestos volátiles se arrastran a lo largo de una línea calentada hacia una "trampa". La trampa es una columna de material adsorbente a temperatura ambiente que retiene los compuestos devolviéndolos a la fase líquida. Luego se calienta la trampa y los compuestos de la muestra se introducen en la columna GC-MS a través de una interfaz de volátiles, que es un sistema de entrada dividida. P&T GC–MS es particularmente adecuado para compuestos orgánicos volátiles (COV) y compuestos BTEX (compuestos aromáticos asociados con el petróleo). [10]
Una alternativa más rápida es el sistema de "bucle cerrado de purga". En este sistema, el gas inerte se burbujea a través del agua hasta que las concentraciones de compuestos orgánicos en la fase de vapor están en equilibrio con las concentraciones en la fase acuosa. A continuación se analiza directamente la fase gaseosa. [11]
El tipo más común de espectrómetro de masas (MS) asociado con un cromatógrafo de gases (GC) es el espectrómetro de masas cuadrupolo, a veces denominado por el nombre comercial de Hewlett-Packard (ahora Agilent ) "Detector selectivo de masas" (MSD). Otro detector relativamente común es el espectrómetro de masas con trampa de iones. Además, se puede encontrar un espectrómetro de masas de sector magnético; sin embargo, estos instrumentos en particular son costosos y voluminosos y no suelen encontrarse en laboratorios de servicios de alto rendimiento. Se pueden encontrar otros detectores, como el tiempo de vuelo (TOF), los cuadrupolos en tándem (MS-MS) (ver más abajo) o, en el caso de una trampa de iones, MS n donde n indica el número de etapas de espectrometría de masas.
Cuando se agrega una segunda fase de fragmentación de masa, por ejemplo usando un segundo cuadrupolo en un instrumento cuadrupolo, se llama MS en tándem (MS/MS). A veces se puede utilizar MS/MS para cuantificar niveles bajos de compuestos objetivo en presencia de un fondo de matriz de muestra alto.
El primer cuadrupolo (Q1) está conectado con una celda de colisión (Q2) y otro cuadrupolo (Q3). Ambos cuadrupolos se pueden utilizar en modo de escaneo o estático, según el tipo de análisis MS/MS que se esté realizando. Los tipos de análisis incluyen escaneo de iones de producto, escaneo de iones precursores, monitoreo de reacciones seleccionadas (SRM) (a veces denominado monitoreo de reacciones múltiples (MRM)) y escaneo de pérdida neutra. Por ejemplo: cuando Q1 está en modo estático (mirando solo una masa como en SIM) y Q3 está en modo de escaneo, se obtiene el llamado espectro de iones producto (también llamado "espectro hijo"). De este espectro, se puede seleccionar un ion producto destacado que puede ser el ion producto del ion precursor elegido. El par se denomina "transición" y constituye la base del SRM. SRM es muy específico y prácticamente elimina el fondo de matriz.
Después de que las moléculas viajan a lo largo de la columna, pasan a través de la línea de transferencia y entran en el espectrómetro de masas, se ionizan mediante varios métodos y, por lo general, solo se utiliza un método en un momento dado. Una vez que la muestra se fragmenta, será detectada, generalmente mediante un multiplicador de electrones , que esencialmente convierte el fragmento de masa ionizada en una señal eléctrica que luego se detecta.
La técnica de ionización elegida es independiente del uso de escaneo completo o SIM.
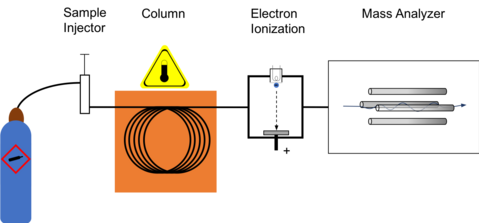
Con diferencia, la forma de ionización más común y quizás estándar es la ionización electrónica (EI). Las moléculas ingresan al MS (la fuente es un cuadrupolo o la propia trampa de iones en un MS con trampa de iones) donde son bombardeadas con electrones libres emitidos por un filamento, no muy diferente al filamento que se encontraría en una bombilla estándar. Los electrones bombardean las moléculas, provocando que la molécula se fragmente de forma característica y reproducible. Esta técnica de "ionización dura" da como resultado la creación de más fragmentos de baja relación masa-carga (m/z) y pocas moléculas, si es que hay alguna, que se acerquen a la unidad de masa molecular. Los espectrometristas de masas consideran la ionización dura como el empleo del bombardeo de electrones moleculares, mientras que la "ionización suave" se carga mediante la colisión molecular con un gas introducido. El patrón de fragmentación molecular depende de la energía de los electrones aplicada al sistema, normalmente 70 eV (electronvoltios). El uso de 70 eV facilita la comparación de los espectros generados con los espectros de la biblioteca utilizando software proporcionado por el fabricante o software desarrollado por el Instituto Nacional de Estándares (NIST-USA). Las búsquedas en bibliotecas espectrales emplean algoritmos de coincidencia como la coincidencia basada en probabilidad [12] y la coincidencia de producto escalar [13] que se utilizan con métodos de análisis escritos por muchas agencias de estandarización de métodos. Las fuentes de bibliotecas incluyen NIST, [14] Wiley, [15] AAFS, [16] y fabricantes de instrumentos.
El proceso de "ionización dura" de la ionización de electrones puede suavizarse enfriando las moléculas antes de su ionización, lo que da como resultado espectros de masas más ricos en información. [17] [18] En este método denominado ionización de electrones en frío (EI-frío), las moléculas salen de la columna de GC, se mezclan con helio agregado y se expanden al vacío a través de una boquilla supersónica especialmente diseñada, formando un haz molecular supersónico (SMB). ). Las colisiones con el gas de reposición en el chorro supersónico en expansión reducen la energía vibratoria (y rotacional) interna de las moléculas del analito, reduciendo así el grado de fragmentación causado por los electrones durante el proceso de ionización. [17] [18] Los espectros de masas de EI frío se caracterizan por un ion molecular abundante mientras se conserva el patrón de fragmentación habitual, lo que hace que los espectros de masas de EI frío sean compatibles con las técnicas de identificación de búsqueda en bibliotecas. Los iones moleculares mejorados aumentan las probabilidades de identificación de compuestos conocidos y desconocidos, amplifican los efectos espectrales de masas de isómeros y permiten el uso del análisis de abundancia de isótopos para dilucidar fórmulas elementales. [19]
En la ionización química (CI), se introduce en el espectrómetro de masas un gas reactivo, normalmente metano o amoníaco . Dependiendo de la técnica (CI positivo o CI negativo) elegida, este gas reactivo interactuará con los electrones y el analito y provocará una ionización "suave" de la molécula de interés. Una ionización más suave fragmenta la molécula en menor grado que la ionización dura de EI. Uno de los principales beneficios de utilizar la ionización química es que se produce un fragmento de masa que se corresponde estrechamente con el peso molecular del analito de interés. [20]
En la ionización química positiva (PCI), el gas reactivo interactúa con la molécula objetivo, generalmente con un intercambio de protones. Esto produce la especie en cantidades relativamente altas.
En la ionización química negativa (NCI), el gas reactivo disminuye el impacto de los electrones libres sobre el analito objetivo. Esta disminución de energía normalmente deja al fragmento en gran cantidad.
Un espectrómetro de masas normalmente se utiliza de dos maneras: escaneo completo o monitoreo selectivo de iones (SIM). El instrumento GC-MS típico es capaz de realizar ambas funciones de forma individual o concomitante, según la configuración del instrumento en particular.
El objetivo principal del análisis de instrumentos es cuantificar una cantidad de sustancia. Esto se hace comparando las concentraciones relativas entre las masas atómicas en el espectro generado. Son posibles dos tipos de análisis: comparativo y original. El análisis comparativo esencialmente compara el espectro dado con una biblioteca de espectro para ver si sus características están presentes para alguna muestra de la biblioteca. Esto se realiza mejor con una computadora porque hay una gran cantidad de distorsiones visuales que pueden ocurrir debido a variaciones de escala. Las computadoras también pueden correlacionar simultáneamente más datos (como los tiempos de retención identificados por GC), para relacionar ciertos datos con mayor precisión. Se demostró que el aprendizaje profundo conduce a resultados prometedores en la identificación de COV a partir de datos sin procesar de GC-MS. [21]
Otro método de análisis mide los picos entre sí. En este método, al pico más alto se le asigna el 100% del valor y a los demás picos se les asignan valores proporcionales. Se asignan todos los valores superiores al 3%. La masa total del compuesto desconocido normalmente está indicada por el pico original. El valor de este pico original se puede utilizar para ajustarlo a una fórmula química que contenga los diversos elementos que se cree que están en el compuesto. El patrón de isótopos en el espectro, que es único para elementos que tienen muchos isótopos naturales, también se puede utilizar para identificar los distintos elementos presentes. Una vez que una fórmula química se ha hecho coincidir con el espectro, se pueden identificar la estructura molecular y el enlace, y deben ser consistentes con las características registradas por GC-MS. Normalmente, esta identificación se realiza automáticamente mediante programas que vienen con el instrumento, dada una lista de los elementos que podrían estar presentes en la muestra.
Un análisis de "espectro completo" considera todos los "picos" dentro de un espectro. Por el contrario, el monitoreo selectivo de iones (SIM) solo monitorea iones seleccionados asociados con una sustancia específica. Esto se hace bajo el supuesto de que, en un tiempo de retención determinado, un conjunto de iones es característico de un determinado compuesto. Se trata de un análisis rápido y eficaz, especialmente si el analista tiene información previa sobre una muestra o sólo busca unas pocas sustancias concretas. Cuando disminuye la cantidad de información recopilada sobre los iones en un pico cromatográfico de gases determinado, aumenta la sensibilidad del análisis. Por lo tanto, el análisis SIM permite detectar y medir una cantidad menor de un compuesto, pero se reduce el grado de certeza sobre la identidad de ese compuesto.
Al recopilar datos en el modo de escaneo completo, se determina un rango objetivo de fragmentos de masa y se coloca en el método del instrumento. Un ejemplo de un rango amplio típico de fragmentos de masa a monitorear sería m/z 50 a m/z 400. La determinación de qué rango usar está dictada en gran medida por lo que uno anticipa que estará en la muestra mientras se conoce el solvente y otros posibles interferencias. Un MS no debe configurarse para buscar fragmentos de masa demasiado baja o de lo contrario se puede detectar aire (que se encuentra como m/z 28 debido al nitrógeno), dióxido de carbono ( m/z 44) u otras posibles interferencias. Además, si se va a utilizar un rango de exploración grande, la sensibilidad del instrumento disminuye debido a que se realizan menos exploraciones por segundo, ya que cada exploración tendrá que detectar una amplia gama de fragmentos de masa.
El escaneo completo es útil para determinar compuestos desconocidos en una muestra. Proporciona más información que SIM a la hora de confirmar o resolver compuestos en una muestra. Durante el desarrollo del método del instrumento, puede ser común analizar primero las soluciones de prueba en modo de escaneo completo para determinar el tiempo de retención y la huella digital del fragmento de masa antes de pasar a un método de instrumento SIM.
En el monitoreo selectivo de iones (SIM), ciertos fragmentos de iones se ingresan en el método del instrumento y el espectrómetro de masas solo detecta esos fragmentos de masa. Las ventajas de SIM son que el límite de detección es menor ya que el instrumento sólo observa una pequeña cantidad de fragmentos (por ejemplo, tres fragmentos) durante cada escaneo. Se pueden realizar más exploraciones cada segundo. Dado que sólo se monitorean unos pocos fragmentos de masa de interés, las interferencias de la matriz suelen ser menores. Para confirmar adicionalmente la probabilidad de un resultado potencialmente positivo, es relativamente importante asegurarse de que las proporciones iónicas de los distintos fragmentos de masa sean comparables a un estándar de referencia conocido.
GC-MS se está convirtiendo en la herramienta preferida para rastrear contaminantes orgánicos en el medio ambiente. El costo de los equipos GC-MS ha disminuido significativamente y al mismo tiempo ha aumentado la confiabilidad, lo que ha contribuido a su mayor adopción en estudios ambientales .
GC-MS puede analizar las partículas de un cuerpo humano para ayudar a vincular a un criminal con un crimen . El análisis de desechos de incendios mediante GC-MS está bien establecido, e incluso existe una norma establecida de la Sociedad Estadounidense de Pruebas y Materiales (ASTM) para el análisis de desechos de incendios. GCMS/MS es especialmente útil en este caso, ya que las muestras suelen contener matrices muy complejas y los resultados, utilizados en los tribunales, deben ser muy precisos.
La GC-MS se utiliza cada vez más para la detección de narcóticos ilegales y, con el tiempo, puede sustituir a los perros detectores de drogas. [1] El Instituto Robert Koch de Alemania desarrolló recientemente un método GC-MS simple y selectivo para detectar el consumo de marihuana. Implica identificar un metabolito ácido del tetrahidrocannabinol (THC), el ingrediente activo de la marihuana, en muestras de orina mediante el empleo de derivatización en la preparación de la muestra. [22] La GC-MS también se utiliza comúnmente en toxicología forense para encontrar drogas y/o venenos en muestras biológicas de sospechosos, víctimas o fallecidos. En la detección de drogas, los métodos GC-MS utilizan con frecuencia la extracción líquido-líquido como parte de la preparación de la muestra, en la que los compuestos objetivo se extraen del plasma sanguíneo. [23]
GC-MS es la principal herramienta utilizada en los laboratorios antidopaje deportivos para analizar muestras de orina de los atletas en busca de drogas prohibidas para mejorar el rendimiento, por ejemplo, esteroides anabólicos . [24]
Como novedad posterior al 11 de septiembre, los sistemas de detección de explosivos se han convertido en parte de todos los aeropuertos de EE. UU . Estos sistemas funcionan con una gran cantidad de tecnologías, muchas de ellas basadas en GC-MS. Solo hay tres fabricantes certificados por la FAA para proporcionar estos sistemas, [ cita necesaria ] uno de los cuales es ThermoDetection (anteriormente Thermedics), que produce EGIS, una línea de detectores de explosivos basada en GC-MS. Los otros dos fabricantes son Barringer Technologies, ahora propiedad de Smith'sDetection Systems, e Ion Track Instruments, parte de General Electric Infrastructure Security Systems.
Como parte del impulso posterior al 11 de septiembre hacia una mayor capacidad en materia de seguridad nacional y preparación para la salud pública, las unidades GC-MS tradicionales con espectrómetros de masas cuadrupolos de transmisión, así como aquellas con trampa de iones cilíndrica (CIT-MS) y trampa de iones toroidal (T -ITMS) se han modificado los espectrómetros de masas para su portabilidad sobre el terreno y la detección casi en tiempo real de agentes de guerra química (CWA), como el sarín, el somán y el VX. [25] Estos complejos y grandes sistemas GC-MS se han modificado y configurado con cromatógrafos de gases de baja masa térmica (LTM) calentados resistivamente que reducen el tiempo de análisis a menos del diez por ciento del tiempo requerido en los sistemas de laboratorio tradicionales. [26] Además, los sistemas son más pequeños y más móviles, incluidas unidades que están montadas en laboratorios analíticos móviles (MAL), como los utilizados por la Fuerza de Respuesta a Incidentes Biológicos y Químicos del Cuerpo de Marines de los Estados Unidos (MAL) y otros laboratorios similares, y sistemas que son llevados en mano por equipos de dos personas o individuos, mucho menos los detectores de masas más pequeños. [27] Dependiendo del sistema, los analitos pueden introducirse mediante inyección líquida, desorberse de tubos absorbentes mediante un proceso de desorción térmica o con microextracción en fase sólida (SPME).
GC-MS se utiliza para el análisis de mezclas de compuestos orgánicos desconocidos. Un uso crítico de esta tecnología es el uso de GC-MS para determinar la composición de bioaceites procesados a partir de biomasa cruda. [28] La GC-MS también se utiliza en la identificación de componentes de fase continua en un material inteligente, el fluido magnetorreológico (MR) . [29]
Los alimentos y bebidas contienen numerosos compuestos aromáticos , algunos presentes de forma natural en las materias primas y otros que se forman durante el procesamiento. GC-MS se usa ampliamente para el análisis de estos compuestos que incluyen ésteres , ácidos grasos , alcoholes , aldehídos , terpenos , etc. También se usa para detectar y medir contaminantes provenientes del deterioro o la adulteración que pueden ser dañinos y que a menudo están controlados por autoridades gubernamentales. agencias, por ejemplo pesticidas .
Varios sistemas GC-MS han abandonado la Tierra. Dos de ellos fueron llevados a Marte por el programa Viking . [30] Venera 11 y 12 y Pioneer Venus analizaron la atmósfera de Venus con GC-MS. [31] La sonda Huygens de la misión Cassini-Huygens aterrizó un GC-MS en la luna más grande de Saturno , Titán . [32] El instrumento de análisis de muestras en Marte (SAM) del rover MSL Curiosity contiene un cromatógrafo de gases y un espectrómetro de masas cuadrupolo que se pueden utilizar en conjunto como GC-MS. [33] El material del cometa 67P/Churyumov–Gerasimenko fue analizado por la misión Rosetta con un GC-MS quiral en 2014. [34]
Docenas de enfermedades metabólicas congénitas, también conocidas como errores congénitos del metabolismo (IEM, por sus siglas en inglés), ahora son detectables mediante pruebas de detección en recién nacidos , especialmente las pruebas que utilizan cromatografía de gases y espectrometría de masas. La GC-MS puede determinar compuestos en la orina incluso en concentraciones menores. Estos compuestos normalmente no están presentes, pero aparecen en personas que padecen trastornos metabólicos. Esta se está convirtiendo cada vez más en una forma común de diagnosticar IEM para un diagnóstico más temprano y la institución de un tratamiento que eventualmente conduzca a un mejor resultado. Ahora es posible evaluar a un recién nacido para detectar más de 100 trastornos metabólicos genéticos mediante un análisis de orina al nacer basado en GC-MS.
En combinación con el marcaje isotópico de compuestos metabólicos, la GC-MS se utiliza para determinar la actividad metabólica . La mayoría de las aplicaciones se basan en el uso de 13 C como etiquetado y la medición de relaciones 13 C- 12 C con un espectrómetro de masas de relaciones isotópicas (IRMS); un MS con un detector diseñado para medir algunos iones seleccionados y devolver valores como proporciones.