La hipocinesia es una de las clasificaciones de los trastornos del movimiento y se refiere a la disminución del movimiento corporal. [1] La hipocinesia se caracteriza por una pérdida parcial o completa del movimiento muscular debido a una alteración en los ganglios basales . [ cita requerida ] La hipocinesia es un síntoma de la enfermedad de Parkinson que se manifiesta como rigidez muscular e incapacidad para producir movimiento. También se asocia con trastornos de salud mental e inactividad prolongada debido a enfermedades, entre otras enfermedades.
La otra categoría de trastorno del movimiento es la hipercinesia , que presenta una exageración del movimiento no deseado, como espasmos o contorsiones en la enfermedad de Huntington o el síndrome de Tourette . [2]
La hipocinesia describe una variedad de trastornos más específicos:
La causa más común de hipocinesia es la enfermedad de Parkinson y las afecciones relacionadas con ella.
Otras afecciones también pueden causar lentitud de movimientos, como el hipotiroidismo y la depresión grave. Estas afecciones deben descartarse cuidadosamente antes de realizar un diagnóstico de parkinsonismo.
El resto de este artículo describe la hipocinesia asociada con la enfermedad de Parkinson y las afecciones relacionadas con esta enfermedad.
Dopamina
El principal neurotransmisor que se cree que está involucrado en la hipocinesia es la dopamina . [11] [12] Esencial para el circuito ganglionar basal-tálamocortical, que procesa la función motora, el agotamiento de dopamina es común en estas áreas de pacientes hipocinesias. [12] La bradicinesia se correlaciona con el agotamiento dopaminérgico lateralizado en la sustancia negra . [12] La vía de la dopamina en la sustancia negra es esencial para la función motora, y comúnmente una lesión en esta área se correlaciona con la hipocinesia mostrada. [12] [13] El temblor y la rigidez, sin embargo, parecen deberse solo parcialmente a los déficits de dopamina en la sustancia negra, lo que sugiere que otros procesos están involucrados en el control motor. [12] Los tratamientos para la hipocinesia a menudo intentan prevenir la degradación de la dopamina por la MAO-B o aumentar la cantidad de neurotransmisor presente en el sistema. [12] [13]
GABA y glutamato
El neurotransmisor inhibidor GABA y el glutamato excitador se encuentran en muchas partes del sistema nervioso central , incluidas las vías motoras que implican hipocinesia. En una vía, el glutamato en la sustancia negra excita la liberación de GABA en el tálamo, que luego inhibe la liberación de glutamato en la corteza y, por lo tanto, reduce la actividad motora. Si inicialmente hay demasiado glutamato en la sustancia negra, entonces, a través de la interacción con el GABA en el tálamo y el glutamato en la corteza, los movimientos se reducirán o no ocurrirán en absoluto. [14]
Otra vía directa desde los ganglios basales envía mensajes inhibidores de GABA al globo pálido y a la sustancia negra, que a su vez envían GABA al tálamo. En la vía indirecta, los ganglios basales envían GABA al globo pálido, que a su vez lo envía al núcleo subtalámico, que luego, desinhibido, envía glutamato a las estructuras de salida de los ganglios basales. La inhibición de la liberación de GABA podría interrumpir el circuito de retroalimentación a los ganglios basales y producir movimientos hipocinéticos. [15]
El GABA y el glutamato suelen interactuar entre sí y con la dopamina directamente. En los ganglios basales, la vía nigroestriatal es donde el GABA y la dopamina se alojan en las mismas neuronas y se liberan juntos. [16]
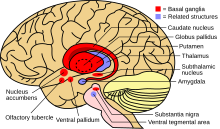
Los síntomas hipocinéticos surgen de un daño en los ganglios basales, que desempeñan un papel en la producción de fuerza y el cálculo del esfuerzo necesario para realizar un movimiento. [17] Dos posibles vías neuronales permiten que los ganglios basales produzcan movimiento. Cuando se activa, la vía directa envía información sensorial y motora desde la corteza cerebral a la primera estructura de los ganglios basales, el putamen . Esa información inhibe directamente el globo pálido interno y permite el movimiento libre. La vía indirecta, que viaja a través del putamen, el globo pálido externo y el núcleo subtalámico, activa el umbral interno del globo pálido e inhibe la comunicación del tálamo con la corteza motora, lo que produce síntomas hipocinéticos. [17]
Cuando los niveles de dopamina disminuyen, el patrón normal de activación de ondas de las oscilaciones neuronales de los ganglios basales cambia y la tendencia a las oscilaciones aumenta, particularmente en la onda beta de los ganglios basales. [18] Investigaciones recientes indican que, cuando las oscilaciones se activan simultáneamente, el procesamiento se interrumpe en el tálamo y la corteza, lo que afecta actividades como la planificación motora y el aprendizaje de secuencias, además de causar temblores hipocinéticos. [17]
Los fármacos dopaminérgicos se utilizan habitualmente en las primeras etapas de la hipocinesia para tratar a los pacientes. [13] Sin embargo, con el aumento de la ingesta, pueden volverse ineficaces debido al desarrollo de lesiones noradrenérgicas . [13] Si bien inicialmente los fármacos dopaminérgicos pueden ser eficaces, estas lesiones noradrenérgicas se asocian con el desarrollo de un trastorno de la marcha hipocinesia más adelante. [12] [13]
Algunos pacientes con Parkinson no pueden moverse durante el sueño, lo que lleva al diagnóstico de "hipocinesia nocturna". Los médicos han tenido éxito en el tratamiento de este trastorno del sueño con fármacos dopaminérgicos de liberación lenta o de administración nocturna y, en algunos casos, con estimulación continua mediante el agonista de la dopamina rotigotina . A pesar de la mejora de la movilidad durante el sueño, muchos pacientes con Parkinson informan de una experiencia de sueño extremadamente incómoda incluso después de los tratamientos dopaminérgicos. [19]
Una vez que la reacción a los fármacos dopaminérgicos comienza a fluctuar en los pacientes con Parkinson, a menudo se utiliza la estimulación cerebral profunda (ECP) del núcleo subtalámico y del globo pálido interno para tratar la hipocinesia. [13] [20] [21] La ECP, al igual que los fármacos dopaminérgicos, inicialmente proporciona alivio, pero el uso crónico provoca una hipocinesia peor y congelamiento de la marcha. [13] [22] Se ha demostrado que la ECP de menor frecuencia en patrones irregulares es más eficaz y menos perjudicial en el tratamiento. [21] [22]

La palidotomía posteroventral (PVP) es un tipo específico de estimulación cerebral profunda que destruye una pequeña parte del globo pálido al cicatrizar el tejido neural, lo que reduce la actividad cerebral y, por lo tanto, los temblores y la rigidez. Se sospecha que la PVP recalibra la actividad de los ganglios basales en la vía talamocortical. Se ha informado que la PVP en el hemisferio dominante altera las capacidades de procesamiento verbal de la función ejecutiva, y la PVP bilateral puede alterar los procesos de atención concentrada. [17]
Muchos pacientes con acinesia también desarrollan una acinesia lingüística en la que su capacidad para producir movimientos verbales refleja sus síntomas de acinesia física, especialmente después de una PVP fallida. [23] Los pacientes suelen ser capaces de mantener niveles normales de fluidez, pero a menudo se detienen a mitad de frase, incapaces de recordar o producir una palabra deseada. [23] Según un estudio de pacientes de Parkinson con hipocinesia articulatoria, [24] los sujetos con velocidades de habla más rápidas experimentaron más problemas al intentar producir lenguaje conversacional que aquellos que normalmente hablaban a velocidades más lentas. [25]
El metilfenidato , comúnmente utilizado para tratar el TDAH, se ha utilizado junto con la levodopa para tratar la hipocinesia a corto plazo. [13] Los dos trabajan juntos para aumentar los niveles de dopamina en el cuerpo estriado y la corteza prefrontal . [13] El metilfenidato inhibe principalmente la recaptación de dopamina y noradrenalina al bloquear los transportadores presinápticos, y la levodopa aumenta la cantidad de dopamina, mejorando generalmente la marcha hipocinesia. [13] [26] Sin embargo, algunos pacientes tienen reacciones adversas de náuseas y dolor de cabeza al tratamiento y aún es necesario evaluar los efectos a largo plazo del tratamiento farmacológico. [13]
Los nuevos tratamientos incluyen el aumento del número de células dopaminérgicas mediante el trasplante de células madre a los ganglios basales o la estimulación de la producción y el movimiento de células madre endógenas a los ganglios basales. [27] La integración exitosa de células madre puede aliviar los síntomas hipocinéticos y disminuir la dosis necesaria de fármacos dopaminérgicos. Sin embargo, son posibles diversas complicaciones, incluida la posible formación de tumores, la migración celular inapropiada, el rechazo de células por parte del sistema inmunológico y la hemorragia cerebral , lo que hace que muchos médicos crean que los riesgos superan los posibles beneficios. [28]
Otro tratamiento, aún en fase experimental, es la administración de antagonistas del receptor del péptido nociceptivo FQ (NOP) . Este tratamiento ha demostrado reducir la hipocinesia en estudios realizados en animales al aumentar el FQ nociceptivo en la sustancia negra y el núcleo subtalámico. Se pueden tomar dosis bajas junto con el tratamiento dopaminérgico para disminuir la cantidad de L-dopa necesaria, lo que puede reducir sus efectos secundarios a largo plazo y mejorar el rendimiento motor. [29]
También se ha demostrado que la terapia de baile reduce los movimientos hipoquinéticos y la rigidez, aunque está más dirigida a los aspectos musculares del trastorno que a la actividad neuronal. [30]
Se ha demostrado que la bradicinesia precede al deterioro de las funciones ejecutivas, la memoria de trabajo y la atención. [11] [31] Estas deficiencias cognitivas pueden estar vinculadas a la disfunción de los ganglios basales y la corteza prefrontal , que también está vinculada a la disfunción motora de la hipocinesia. [11] El temblor y la rigidez no han tenido conexiones observables con los deterioros cognitivos, lo que apoya la idea de que no están tan involucrados en la vía de la dopamina en el circuito ganglionar basal-tálamocortical. [11] [12] Los tratamientos dopaminérgicos han mostrado una mejora en las funciones cognitivas asociadas con la hipocinesia, lo que sugiere que también dependen de los niveles de dopamina en el sistema. [31]
A menudo se debate si la eficiencia, el vigor y la velocidad de los movimientos en pacientes con hipocinesia están vinculados a la motivación para recibir estímulos gratificantes y no castigadores. Los ganglios basales se han vinculado a los incentivos detrás del movimiento, por lo que se sugiere que un análisis de costo/beneficio del movimiento planificado podría verse afectado en la hipocinesia. No se ha demostrado que las recompensas cambien los aspectos del movimiento de un individuo hipocinesia. [32] De hecho, la planificación y el control motor de un paciente con hipocinesia ya son lo más eficientes posible (como lo demuestra un movimiento ligeramente más rápido, pero generalmente el mismo después de la estimulación cerebral profunda del núcleo subtalámico ). [33] Esto sugiere que los individuos hipocinéticos simplemente tienen un rango de movimiento más estrecho que no aumenta en relación con la motivación. [32] [34]
Otros estudios han llegado a la misma conclusión sobre las recompensas y la hipocinesia, pero han demostrado que los estímulos aversivos pueden, de hecho, reducir el movimiento hipocinesia. La dopamina está menos involucrada o tiene un papel más complejo en la respuesta al castigo que en la de las recompensas, ya que el cuerpo estriado hipodopaminérgico permite más movimiento en respuesta a los estímulos aversivos. [35]
Género
La hipocinesia suele manifestarse en mayor proporción en hombres que en mujeres, lo que se refleja en poblaciones jóvenes y de mediana edad, donde las mujeres presentan niveles más elevados de dopamina nigroestriatal que los hombres. Sin embargo, en los ancianos, esta diferenciación no está presente. Por lo general, las mujeres presentan más temblores al inicio de la hipocinesia. En este trastorno, los hombres tienden a mostrar más rigidez y las mujeres, un comportamiento motor más bradicinésico. [36]
Edad de aparición
La hipocinesia se manifiesta en el cerebro y externamente es ligeramente diferente según el momento en que el individuo se vea afectado por primera vez. En la hipocinesia de inicio temprano (menores de 45 años de edad), por lo general se produce una pérdida de células ligeramente mayor en la sustancia negra con una mayor distonía y rigidez muscular. En la hipocinesia de inicio temprano (mayores de 70 años de edad), por lo general se observa una marcha más hipocinésica y dificultad para caminar, pero no distonía. Ambos inicios pueden presentar temblor en reposo, aunque se encuentra más generalmente en los casos de inicio temprano. [37]
El estrés provoca alteraciones de la circulación cerebral , aumentando el flujo sanguíneo en el giro supramarginal y el giro angular del lóbulo parietal , el lóbulo frontal y el giro temporal superior del hemisferio izquierdo. También se produce un aumento de la actividad cardíaca y un cambio en el tono de los vasos cardíacos, lo que es una indicación elemental del desarrollo del estrés. En pacientes con estrés normal, una respuesta adaptativa de lucha o huida suele desencadenarse por la activación del sistema nervioso simpático . Los pacientes con hipocinesia experimentan estos síntomas típicos de estrés de forma regular debido al daño en el sistema de ganglios basales. Por lo tanto, cuando una víctima de hipocinesia está bajo estrés, no muestra una respuesta típica de lucha o huida, lo que coloca al paciente bajo un mayor peligro de estímulos potencialmente dañinos. [38] El ejercicio de bajo impacto, la eliminación del consumo de drogas y alcohol y la meditación regular pueden ayudar a restablecer las respuestas normales al estrés en pacientes con hipocinesia. [39]
Aunque a menudo se asocia con la enfermedad de Parkinson, la hipocinesia puede estar presente en una amplia variedad de otras afecciones.
...el deterioro del equilibrio que compromete la capacidad de mantener o cambiar la postura, como estar de pie y caminar. ... se observó una mayor discapacidad y más depresión en los pacientes con EP con inestabilidad postural predominante y trastorno de la marcha que en aquellos que tenían EP con predominio de temblor. Además, no solo se correlaciona con las caídas, sino también con el miedo a futuras caídas, que puede ser incapacitante por sí mismo.