La antitrombina (AT) es una pequeña glicoproteína que inactiva varias enzimas del sistema de coagulación . Es una proteína de 464 aminoácidos producida por el hígado . Contiene tres enlaces disulfuro y un total de cuatro posibles sitios de glicosilación . La α-antitrombina es la forma dominante de antitrombina que se encuentra en el plasma sanguíneo y tiene un oligosacárido que ocupa cada uno de sus cuatro sitios de glicosilación. Un único sitio de glicosilación permanece constantemente desocupado en la forma menor de antitrombina, la β-antitrombina. [5] Su actividad aumenta muchas veces gracias al fármaco anticoagulante heparina , que mejora la unión de la antitrombina al factor IIa (trombina) y al factor Xa . [6]
La antitrombina también se denomina antitrombina III (AT III). Las denominaciones desde antitrombina I hasta antitrombina IV se originan en los primeros estudios realizados en la década de 1950 por Seegers, Johnson y Fell. [7]
La antitrombina I (AT I) se refiere a la unión de la trombina a la fibrina , después de que la trombina ha activado el fibrinógeno , en un sitio de unión no catalítico de la trombina. La antitrombina II (AT II) se refiere a un cofactor en plasma que, junto con la heparina, interfiere con la interacción de la trombina y el fibrinógeno . La antitrombina III (AT III) se refiere a una sustancia en plasma que inactiva la trombina. La antitrombina IV (AT IV) se refiere a una antitrombina que se activa durante y poco después de la coagulación sanguínea . [8] Sólo AT III y posiblemente AT I son médicamente significativos. La AT III generalmente se denomina únicamente "antitrombina" y es la antitrombina III la que se analiza en este artículo.

La antitrombina tiene una vida media en el plasma sanguíneo de aproximadamente 3 días. [9] La concentración normal de antitrombina en el plasma sanguíneo humano es alta, aproximadamente 0,12 mg/ml, lo que equivale a una concentración molar de 2,3 μM. [10] La antitrombina se ha aislado del plasma de un gran número de especies además de los humanos. [11] Como se deduce de la secuenciación de proteínas y ADNc , las antitrombinas de vaca, oveja, conejo y ratón tienen 433 aminoácidos de longitud, que es un aminoácido más largo que la antitrombina humana. Se cree que el aminoácido extra se produce en la posición 6 del aminoácido. Las antitrombinas de vaca, oveja, conejo, ratón y humanos comparten entre un 84 y un 89 % de identidad de secuencia de aminoácidos. [12] Seis de los aminoácidos forman tres enlaces disulfuro intramoleculares , Cys 8-Cys128, Cys21-Cys95 y Cys248-Cys430. Todos ellos tienen cuatro sitios potenciales de N-glicosilación . Estos ocurren en los aminoácidos 96, 135, 155 y 192 de la asparagina (Asn) en humanos y en números de aminoácidos similares en otras especies. Todos estos sitios están ocupados por cadenas laterales de oligosacáridos unidas covalentemente en la forma predominante de antitrombina humana, la α-antitrombina, lo que da como resultado un peso molecular para esta forma de antitrombina de 58.200. [5] El sitio potencial de glicosilación en la asparagina 135 no está ocupado en una forma menor (alrededor del 10%) de antitrombina, β-antitrombina (ver Figura 1 ). [13]
Se han producido antitrombinas recombinantes con propiedades similares a las de la antitrombina humana normal utilizando células de insectos infectadas con baculovirus y líneas celulares de mamíferos cultivadas en cultivos celulares . [14] [15] [16] [17] Estas antitrombinas recombinantes generalmente tienen patrones de glicosilación diferentes a los de la antitrombina normal y generalmente se usan en estudios estructurales de antitrombina. Por esta razón, muchas de las estructuras de antitrombina almacenadas en el banco de datos de proteínas y presentadas en este artículo muestran patrones de glicosilación variables.
La antitrombina comienza en su estado nativo, que tiene una energía libre más alta en comparación con el estado latente, al que decae en promedio después de 3 días. El estado latente tiene la misma forma que el estado activado, es decir, cuando inhibe la trombina. Como tal, es un ejemplo clásico de la utilidad del control cinético versus termodinámico del plegamiento de proteínas.


La antitrombina es una serpina (inhibidor de la serina proteasa) y, por tanto, tiene una estructura similar a la mayoría de los demás inhibidores de la proteasa plasmática , como la alfa 1-antiquimotripsina , la alfa 2-antiplasmina y el cofactor II de heparina .
Las proteasas diana fisiológicas de la antitrombina son las de la vía de activación por contacto (anteriormente conocida como vía intrínseca), es decir, las formas activadas del Factor X (Xa), Factor IX (IXa), Factor XI (XIa), Factor XII (XIIa). y, en mayor medida, el Factor II (trombina) (IIa), y también la forma activada del Factor VII (VIIa) de la vía del factor tisular (anteriormente conocida como vía extrínseca). [20] El inhibidor también inactiva la calicreína y la plasmina [ cita necesaria ] , que también participan en la coagulación sanguínea. Sin embargo, inactiva otras serina proteasas que no participan en la coagulación, como la tripsina y la subunidad C1s de la enzima C1 implicada en la vía clásica del complemento . [12] [21]
La inactivación de la proteasa resulta de atrapar la proteasa en un complejo equimolar con antitrombina en el que el sitio activo de la enzima proteasa es inaccesible a su sustrato habitual . [12] La formación de un complejo antitrombina-proteasa implica una interacción entre la proteasa y un enlace peptídico reactivo específico dentro de la antitrombina. En la antitrombina humana, este enlace se produce entre la arginina (arg) 393 y la serina (ser) 394 (ver Figura 2 y Figura 3 ). [12]
Se cree que las enzimas proteasas quedan atrapadas en complejos inactivos de antitrombina-proteasa como consecuencia de su ataque al enlace reactivo. Aunque atacar un enlace similar dentro del sustrato de proteasa normal da como resultado una rápida escisión proteolítica del sustrato, iniciar un ataque al enlace reactivo de antitrombina hace que la antitrombina se active y atrape la enzima en una etapa intermedia del proceso proteolítico. Con el tiempo, la trombina es capaz de escindir el enlace reactivo dentro de la antitrombina y un complejo antitrombina-trombina inactivo se disociará; sin embargo, el tiempo necesario para que esto ocurra puede ser superior a 3 días. [22] Sin embargo, los enlaces P3-P4 y P1'-P2' pueden escindirse rápidamente mediante la elastasa de neutrófilos y la enzima bacteriana termolisina , respectivamente, lo que da como resultado antitrombinas inactivas que ya no pueden inhibir la actividad de la trombina. [23]
La tasa de inhibición de la actividad proteasa por parte de la antitrombina aumenta en gran medida por su unión adicional a la heparina , al igual que su inactivación por la elastasa de neutrófilos . [23]
La antitrombina inactiva sus enzimas diana fisiológicas, la trombina, el factor Xa y el factor IXa con constantes de velocidad de 7–11 x 10 3 , 2,5 x 10 3 M −1 s −1 y 1 x 10 M −1 s −1 respectivamente. [5] [24] La tasa de inactivación de antitrombina-trombina aumenta a 1,5 - 4 x 10 7 M −1 s −1 en presencia de heparina, es decir, la reacción se acelera entre 2000 y 4000 veces. [25] [26] [27] [28] La inhibición del factor Xa se acelera sólo de 500 a 1000 veces en presencia de heparina y la constante de velocidad máxima es 10 veces menor que la de la inhibición de trombina. [25] [28] La tasa de aumento de la inhibición del factor IXa de antitrombina muestra un aumento aproximado de 1 millón de veces en presencia de heparina y niveles fisiológicos de calcio . [24]
AT-III se une a una secuencia de sulfatación de pentasacárido específica contenida dentro del polímero de heparina
GlcNAc/NS(6S)-GlcA-GlcNS(3S,6S)-IdoA(2S)-GlcNS(6S)
Al unirse a esta secuencia de pentasacárido, la heparina aumenta la inhibición de la actividad de la proteasa como resultado de dos mecanismos distintos. [29] En un mecanismo, la estimulación con heparina de la inhibición del factor IXa y Xa depende de un cambio conformacional dentro de la antitrombina que involucra el bucle del sitio reactivo y, por lo tanto, es alostérico . [30] En otro mecanismo, la estimulación de la inhibición de la trombina depende de la formación de un complejo ternario entre AT-III, trombina y heparina. [30]

El aumento de la inhibición de los factores IXa y Xa requiere la secuencia mínima de pentasacárido de heparina. Los cambios conformacionales que ocurren dentro de la antitrombina en respuesta a la unión del pentasacárido están bien documentados. [18] [31] [32]
En ausencia de heparina, los aminoácidos P14 y P15 (ver Figura 3 ) del bucle del sitio reactivo están incrustados dentro del cuerpo principal de la proteína (específicamente la parte superior de la hoja beta A). Esta característica es común con otras serpinas como el cofactor II de heparina , la alfa 1-antiquimotripsina y MENT .
El cambio conformacional más relevante para la inhibición del Factor IXa y Xa involucra los aminoácidos P14 y P15 dentro de la región N-terminal del bucle del sitio reactivo (encerrado en un círculo en la Figura 4 modelo B ). Esta región ha sido denominada región bisagra. El cambio conformacional dentro de la región bisagra en respuesta a la unión de heparina da como resultado la expulsión de P14 y P15 del cuerpo principal de la proteína y se ha demostrado que al prevenir este cambio conformacional, no se produce un aumento de la inhibición de los factores IXa y Xa. [30] Se cree que la mayor flexibilidad dada al bucle del sitio reactivo como resultado del cambio conformacional de la región bisagra es un factor clave para influir en el aumento de la inhibición del Factor IXa y Xa. Se ha calculado que en ausencia del pentasacárido sólo una de cada 400 moléculas de antitrombina (0,25%) se encuentra en conformación activa con los aminoácidos P14 y P15 expulsados. [30]
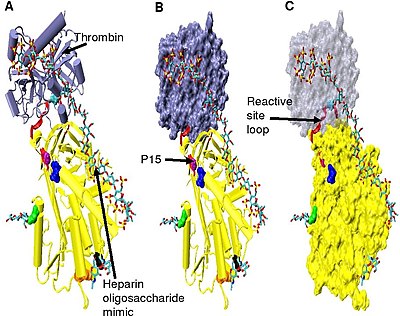
El aumento de la inhibición de la trombina requiere un mínimo de pentasacárido de heparina más al menos 13 unidades monoméricas adicionales. [33] Se cree que esto se debe al requisito de que la antitrombina y la trombina deben unirse a la misma cadena de heparina adyacentes entre sí. Esto se puede ver en la serie de modelos que se muestran en la Figura 5 .
En las estructuras mostradas en la Figura 5, la porción C-terminal (lado P') del bucle del sitio reactivo está en una conformación extendida en comparación con otras estructuras de antitrombina no activadas o activadas con heparina. [34] La región P' de la antitrombina es inusualmente larga en relación con la región P' de otras serpinas y en estructuras de antitrombina no activadas o activadas con heparina forma un giro β fuertemente unido por enlaces de hidrógeno . El alargamiento P' se produce mediante la rotura de todos los enlaces de hidrógeno implicados en el giro β . [34]
La región bisagra de la antitrombina en el complejo de la Figura 5 no se pudo modelar debido a su flexibilidad conformacional y los aminoácidos P9-P14 no se observan en esta estructura. Esta flexibilidad conformacional indica que puede existir un equilibrio dentro del complejo entre una conformación de antitrombina insertada en un bucle del sitio reactivo P14 P15 y una conformación expulsada del bucle del sitio reactivo P14 P15. En apoyo de esto, el análisis del posicionamiento de P15 Gly en el complejo de la Figura 5 (etiquetado en el modelo B) muestra que está insertado en la hoja beta A (ver modelo C). [34]
La α-antitrombina y la β-antitrombina difieren en su afinidad por la heparina. [35] La diferencia en la constante de disociación entre los dos es tres veces mayor para el pentasacárido que se muestra en la Figura 3 y más de diez veces para la heparina completa, teniendo la β-antitrombina una mayor afinidad. [36] Se cree que la mayor afinidad de la β-antitrombina se debe al aumento de la velocidad a la que se producen cambios conformacionales posteriores dentro de la proteína tras la unión inicial de la heparina. Para la α-antitrombina, no se cree que la glicosilación adicional en Asn-135 interfiera con la unión inicial de heparina, sino que inhibe cualquier cambio conformacional resultante. [35]
Aunque está presente en sólo 5 a 10% de los niveles de α-antitrombina, debido a su mayor afinidad por la heparina, se cree que la β-antitrombina es más importante que la α-antitrombina para controlar los eventos trombogénicos resultantes de la lesión tisular. De hecho, la inhibición de la trombina después de una lesión de la aorta se ha atribuido únicamente a la antitrombina β. [37]
La evidencia del importante papel que desempeña la antitrombina en la regulación de la coagulación sanguínea normal se demuestra por la correlación entre las deficiencias de antitrombina heredadas o adquiridas y un mayor riesgo de que cualquier individuo afectado desarrolle una enfermedad trombótica. [38] La deficiencia de antitrombina generalmente sale a la luz cuando un paciente sufre trombosis venosa recurrente y embolia pulmonar .
La deficiencia de antitrombina adquirida se produce como resultado de tres mecanismos claramente diferentes. El primer mecanismo es el aumento de la excreción que puede ocurrir con la insuficiencia renal asociada con el síndrome nefrótico de proteinuria . El segundo mecanismo resulta de una disminución de la producción, como se observa en la insuficiencia hepática , la cirrosis o un hígado inmaduro secundario a un parto prematuro . El tercer mecanismo resulta del consumo acelerado, que es más pronunciado como consecuencia de lesiones traumáticas graves , pero también puede observarse en menor escala como resultado de intervenciones como cirugía mayor o bypass cardiopulmonar . [39]
La incidencia de la deficiencia hereditaria de antitrombina se ha estimado entre 1:2000 y 1:5000 en la población normal; la primera familia que sufrió una deficiencia hereditaria de antitrombina se describió en 1965. [40] [41] Posteriormente, se propuso que la La clasificación de la deficiencia hereditaria de antitrombina puede designarse como tipo I o tipo II, basándose en análisis de antitrombina funcionales e inmunoquímicos . [42] El mantenimiento de un nivel adecuado de actividad antitrombina, que es al menos el 70% del nivel funcional normal, es esencial para garantizar una inhibición eficaz de las proteasas de la coagulación sanguínea. [43] Por lo general, como resultado de la deficiencia de antitrombina tipo I o tipo II, los niveles funcionales de antitrombina se reducen a menos del 50% de lo normal. [44]
La deficiencia de antitrombina de tipo I se caracteriza por una disminución tanto de la actividad como de la concentración de antitrombina en la sangre de los individuos afectados. La deficiencia de tipo I se dividió originalmente en dos subgrupos, Ia y Ib, según la afinidad por la heparina. La antitrombina de los individuos del subgrupo Ia mostró una afinidad normal por la heparina, mientras que la antitrombina de los individuos del subgrupo Ib mostró una afinidad reducida por la heparina. [45] El análisis funcional posterior de un grupo de casos 1b encontró que no solo tenían una afinidad reducida por la heparina, sino también anomalías múltiples o "pleiotróficas" que afectaban el sitio reactivo, el sitio de unión de la heparina y la concentración sanguínea de antitrombina. En un sistema revisado de clasificación adoptado por el Comité Científico y de Normalización de la Sociedad Internacional de Trombosis y Hemostasia, los casos de tipo Ib ahora se designan como EP de tipo II, efecto pleiotrófico. [46]
La mayoría de los casos de deficiencia tipo I se deben a mutaciones puntuales , deleciones o inserciones menores dentro del gen de la antitrombina. Estas mutaciones genéticas dan como resultado la deficiencia tipo I a través de una variedad de mecanismos:
La deficiencia de antitrombina tipo II se caracteriza por niveles normales de antitrombina pero actividad antitrombina reducida en la sangre de los individuos afectados. Originalmente se propuso dividir la deficiencia de tipo II en tres subgrupos (IIa, IIb y IIc) dependiendo de qué actividad funcional de antitrombina se reduzca o se retenga. [45]
En el sistema revisado de clasificación adoptado nuevamente por el Comité Científico y de Normalización de la Sociedad Internacional de Trombosis y Hemostasia, la deficiencia de antitrombina de tipo II permanece subdividida en tres subgrupos: el tipo II PE ya mencionado, junto con el RS de tipo II, donde las mutaciones afectan la sitio reactivo y HBS tipo II, donde las mutaciones afectan el sitio de unión de heparina antitrombina. [46] A los efectos de una base de datos de mutaciones de antitrombina compilada por miembros del Subcomité de Inhibidores de la Coagulación Plasmática del Comité Científico y de Normalización de la Sociedad Internacional de Trombosis y Hemostasia, los casos de tipo IIa se clasifican ahora como EP de tipo II, los casos de tipo IIb como RS tipo II y casos tipo IIc como HBS tipo II. [49]
Actualmente es relativamente fácil caracterizar una mutación genética de antitrombina específica. Sin embargo, antes del uso de técnicas modernas de caracterización, los investigadores denominaban las mutaciones según el pueblo o ciudad donde residía el individuo que padecía la deficiencia, es decir, la mutación de antitrombina se designaba como topónimo . [50] Desde entonces, la caracterización mutacional moderna ha demostrado que muchos topónimos de antitrombina individuales son en realidad el resultado de la misma mutación genética, por ejemplo, antitrombina-Toyama, es equivalente a antitrombina-Kumamoto, -Amien, -Tours, -Paris-1, -Paris. -2, -Alger, -Padua-2 y -Barcelona. [49]
La antitrombina se utiliza como una proteína terapéutica que puede purificarse a partir de plasma humano [51] o producirse de forma recombinante (por ejemplo, Atryn, que se produce en la leche de cabras genéticamente modificadas [52] [53] ).
Está aprobado por la FDA como anticoagulante para la prevención de coágulos antes, durante o después de una cirugía o el parto en pacientes con deficiencia hereditaria de antitrombina. [51] [53]
Se ha estudiado en la sepsis para reducir la coagulación intravascular difusa y otros resultados. No se ha descubierto que confiera ningún beneficio en personas críticamente enfermas con sepsis. [54]

La escisión en el sitio reactivo da como resultado el atrapamiento de la trombina proteasa, con el movimiento del bucle del sitio reactivo escindido junto con la proteasa unida, de modo que el bucle forma una sexta hebra adicional en el medio de la lámina beta A. Este movimiento del sitio reactivo El bucle también se puede inducir sin escisión, siendo la estructura cristalográfica resultante idéntica a la de la conformación fisiológicamente latente del inhibidor-1 del activador del plasminógeno (PAI-1). [55] Por esta razón, la conformación de la antitrombina en la que el bucle del sitio reactivo se incorpora sin escindir en el cuerpo principal de la proteína se denomina antitrombina latente. A diferencia de PAI-1, la transición de la antitrombina de una conformación normal o nativa a una conformación latente es irreversible.
La antitrombina nativa se puede convertir en antitrombina latente (L-antitrombina) calentando sola o calentando en presencia de citrato . [56] [57] Sin embargo, sin calentamiento extremo y a 37 °C (temperatura corporal), el 10% de toda la antitrombina que circula en la sangre se convierte en L-antitrombina durante un período de 24 horas. [58] [59] La estructura de la L-antitrombina se muestra en la Figura 6 .
La estructura tridimensional de la antitrombina nativa se determinó por primera vez en 1994. [31] [32] Inesperadamente, la proteína cristalizó como un heterodímero compuesto por una molécula de antitrombina nativa y una molécula de antitrombina latente. La antitrombina latente al formarse se une inmediatamente a una molécula de antitrombina nativa para formar el heterodímero, y no es hasta que la concentración de antitrombina latente excede el 50% de la antitrombina total que puede detectarse analíticamente. [59] No sólo la forma latente de antitrombina es inactiva contra sus proteasas de coagulación objetivo, sino que su dimerización con una molécula de antitrombina nativa que de otro modo sería activa también da como resultado la inactivación de las moléculas nativas. El impacto fisiológico de la pérdida de actividad antitrombina, ya sea a través de la formación de antitrombina latente o mediante la formación posterior de dímeros, se ve exacerbado por la preferencia por que se produzca la dimerización entre la β-antitrombina activada con heparina y la antitrombina latente en contraposición a la α-antitrombina. [59]
También se ha aislado una forma de antitrombina que es un intermediario en la conversión entre las formas nativa y latente de antitrombina y se la denomina antitrombina prelatente . [60]
La angiogénesis es un proceso fisiológico que implica el crecimiento de nuevos vasos sanguíneos a partir de vasos preexistentes. En condiciones fisiológicas normales, la angiogénesis está estrechamente regulada y controlada por un equilibrio de estimuladores angiogénicos e inhibidores angiogénicos . El crecimiento del tumor depende de la angiogénesis y durante el desarrollo del tumor se requiere una producción sostenida de factores estimuladores angiogénicos junto con una reducción en la cantidad de factores inhibidores angiogénicos que producen las células tumorales. [61] La forma escindida y latente de antitrombina inhibe potentemente la angiogénesis y el crecimiento tumoral en modelos animales. [62] Se ha demostrado que la forma prelatente de antitrombina inhibe la angiogénesis in vitro , pero hasta la fecha no se ha probado en modelos animales experimentales.