La α 2 -macroglobulina ( α 2 M ) o alfa-2-macroglobulina es una proteína plasmática de gran tamaño (720 KDa) que se encuentra en la sangre . Es producido principalmente por el hígado y también sintetizado localmente por macrófagos , fibroblastos y células suprarrenocorticales . En humanos está codificado por el gen A2M .
La α 2 -Macroglobulina actúa como antiproteasa y es capaz de inactivar una enorme variedad de proteinasas. Funciona como inhibidor de la fibrinólisis al inhibir la plasmina y la calicreína . Funciona como inhibidor de la coagulación al inhibir la trombina . La α 2 -macroglobulina puede actuar como proteína portadora porque también se une a numerosos factores de crecimiento y citocinas, como el factor de crecimiento derivado de plaquetas, el factor de crecimiento de fibroblastos básico, TGF-β, insulina e IL-1β.
No se ha reconocido ninguna deficiencia específica con enfermedad asociada y ningún estado patológico se atribuye a bajas concentraciones de α 2 -macroglobulina. La concentración de α 2 -macroglobulina aumenta 10 veces o más en el síndrome nefrótico cuando otras proteínas de menor peso molecular se pierden en la orina. Su gran tamaño evita la pérdida de α 2 -macroglobulina en la orina. El resultado neto es que la α 2 -macroglobulina alcanza niveles séricos iguales o superiores a los de albúmina en el síndrome nefrótico, lo que tiene el efecto de mantener la presión oncótica .
La α 2 -macroglobulina humana está compuesta de cuatro subunidades idénticas unidas por enlaces -SS- . [5] [6] Además de las formas tetraméricas de α 2 -macroglobulina, se han identificado inhibidores de proteasa αM diméricos y, más recientemente, monoméricos . [7] [8]
Cada monómero de la α 2 -macroglobulina humana está compuesto por varios dominios funcionales, incluidos dominios de macroglobulina, un dominio que contiene tioéster y un dominio de unión al receptor. [9] En general, la α 2 -macroglobulina es la proteína no inmunoglobulina más grande del plasma humano.
Se ha demostrado que la secuencia de aminoácidos de la α 2 -macroglobulina es 71% igual a la de la proteína de la zona del embarazo (PZP; también conocida como α 2 -glicoproteína asociada al embarazo ). [10]
La familia de proteínas α-macroglobulina (αM) incluye inhibidores de proteasa , [11] tipificados por la α 2 -macroglobulina tetramérica humana (α 2 M); pertenecen a la familia I39 de inhibidores de la proteinasa MEROPS , clan IL. Estos inhibidores de proteasas comparten varias propiedades definitorias, que incluyen (1) la capacidad de inhibir proteasas de todas las clases catalíticas , (2) la presencia de una "región cebo" (también conocida como secuencia de aminoácidos en una molécula de α 2 -macroglobulina , o una proteína homóloga, que contiene enlaces peptídicos escindibles para aquellas proteinasas que inhibe) y un éster de tiol , (3) un mecanismo inhibidor de proteasa similar y (4) la inactivación de la capacidad inhibidora por reacción del éster de tiol con pequeñas moléculas primarias. aminas . Los inhibidores de la proteasa αM inhiben por impedimento estérico . [12] El mecanismo implica la escisión por proteasa de la región del cebo, un segmento de la αM que es particularmente susceptible a la escisión proteolítica , que inicia un cambio conformacional tal que la αM colapsa alrededor de la proteasa. En el complejo αM-proteasa resultante, el sitio activo de la proteasa está estéricamente protegido, lo que disminuye sustancialmente el acceso a los sustratos proteicos . Se producen dos eventos adicionales como consecuencia de la escisión de la región del cebo, a saber, (1) el éster de h-cisteinil-g-glutamil tiol se vuelve altamente reactivo y (2) un cambio conformacional importante expone un dominio de unión al receptor COOH-terminal conservado [13] ( RBD). La exposición a RBD permite que el complejo de proteasa αM se una a los receptores de eliminación y se elimine de la circulación. [14] Se han identificado inhibidores de la proteasa αM tetraméricos, diméricos y, más recientemente, monoméricos. [7] [8]
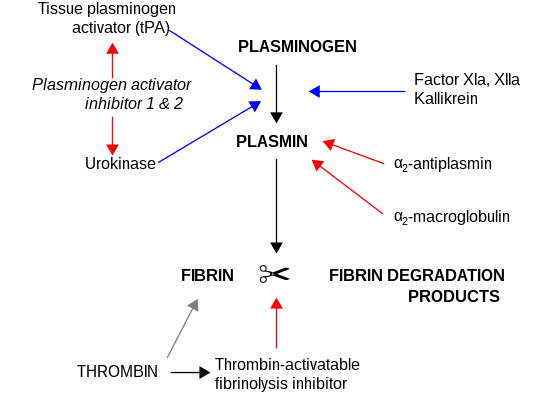
La α 2 -macroglobulina es capaz de inactivar una enorme variedad de proteinasas (incluidas las serina , cisteína , aspártico y metaloproteinasas ). Funciona como inhibidor de la fibrinólisis al inhibir la plasmina y la calicreína. Funciona como inhibidor de la coagulación al inhibir la trombina . [15] La α 2 -Macroglobulina tiene en su estructura una región "cebo" de 35 aminoácidos. Las proteinasas que se unen y escinden la región del cebo quedan unidas a α 2 M. El complejo proteinasa-α 2 M es reconocido por los receptores de macrófagos y eliminado del sistema.
Se sabe que la α 2 -macroglobulina se une al zinc y al cobre en el plasma, incluso con más fuerza que la albúmina, por lo que también se la conoce como transcupreína . [16] Del 10 al 15% del cobre en el plasma humano está quelado por α 2 -macroglobulina. [17]
Los niveles de α 2 -macroglobulina aumentan cuando los niveles de albúmina sérica son bajos, [18] lo que se observa con mayor frecuencia en el síndrome nefrótico , una afección en la que los riñones comienzan a filtrar algunas de las proteínas sanguíneas más pequeñas. Debido a su tamaño, la α 2 -macroglobulina se retiene en el torrente sanguíneo. El aumento de la producción de todas las proteínas significa que aumenta la concentración de α 2 -macroglobulina. Este aumento tiene pocos efectos adversos sobre la salud pero se utiliza como pista de diagnóstico.
Un aumento de α 2 -macroglobulina con una cantidad normal de albúmina indica principalmente inflamación aguda y/o crónica. [19]
Una variante común (29,5%) ( polimorfismo ) de la α2 - macroglobulina aumenta el riesgo de enfermedad de Alzheimer . [20] [21]
La α 2 -macroglobulina se une a las formas activas de la gelatinasa ( MMP-2 y MMP-9 ) y las elimina de la circulación a través de receptores eliminadores de los fagocitos.