En química supramolecular , [1] la química huésped-huésped describe complejos que se componen de dos o más moléculas o iones que se mantienen unidos en relaciones estructurales únicas mediante fuerzas distintas a las de los enlaces covalentes completos . La química huésped-huésped abarca la idea de reconocimiento molecular e interacciones a través de enlaces no covalentes . El enlace no covalente es fundamental para mantener la estructura tridimensional de moléculas grandes, como las proteínas, y está involucrado en muchos procesos biológicos en los que las moléculas grandes se unen de manera específica pero transitoria entre sí.
Aunque las interacciones no covalentes podrían dividirse a grandes rasgos en aquellas con contribuciones más electrostáticas o dispersivas, existen pocos tipos de interacciones no covalentes comúnmente mencionados: enlaces iónicos , enlaces de hidrógeno , fuerzas de van der Waals e interacciones hidrofóbicas . [2]
La interacción anfitrión-huésped ha despertado una atención espectacular desde su descubrimiento. Es un campo importante, porque muchos procesos biológicos requieren la interacción huésped-huésped y puede resultar útil en algunos diseños de materiales. Hay varias moléculas huésped típicas, como ciclodextrina, éter corona, et al .


Aunque van der Waals postuló la interacción intermolecular en 1873, en 1894 Fischer construyó una raíz filosófica para la química supramolecular . Señaló que las interacciones enzima-proteína se comportan como "llave y candado". Esta interacción es la base de la química entre anfitrión e invitado. Con una comprensión más profunda de las interacciones no covalentes, por ejemplo, el esclarecimiento claro de la estructura del ADN , los químicos comenzaron a enfatizar la importancia de las interacciones no covalentes. [5] En 1967, Charles J. Pedersen descubrió los éteres corona, que son estructuras en forma de anillos capaces de quelar ciertos iones metálicos. Luego, en 1969, Jean-Marie Lehn descubrió una clase de moléculas similares a los éteres corona, llamadas criptandos. Después de eso, Donald J. Cram sintetizó muchas variaciones de los éteres corona, además de moléculas separadas capaces de interactuar selectivamente con ciertas sustancias químicas. Los tres científicos recibieron el Premio Nobel de Química en 1987 por el "desarrollo y uso de moléculas con interacciones estructurales específicas de alta selectividad". [6] En 2016, Bernard L. Feringa, Sir J. Fraser Stoddart y Jean-Pierre Sauvage recibió el Premio Nobel de Química "por el diseño y la síntesis de máquinas moleculares " [7] .
La química supramolecular se refiere a los sistemas químicos que contienen componentes químicos en números discretos. Las fuerzas de los sistemas varían desde fuerzas intermoleculares hasta uniones covalentes. Los investigadores mencionados anteriormente crearon y ampliaron el área de interacción huésped-huésped, uno de los conceptos más importantes en los campos de la química supramolecular. Hay dos componentes importantes en la interacción anfitrión-huésped. Una son las "moléculas huésped", que generalmente tienen una estructura "similar a un poro" que puede capturar otras moléculas. La otra son las "moléculas invitadas", que generalmente son más pequeñas que las moléculas huésped y capaces de unirse a las moléculas huésped. Las fuerzas impulsoras de la interacción pueden variar en diferentes casos, como el efecto hidrofóbico, el efecto quelato, la fuerza de van der Waals, et al. [8] Diferentes uniones proporcionarán propiedades variantes para los materiales, es decir, capacidad de respuesta a estímulos, autocuración y rigidez de la matriz. Como consecuencia, la interacción anfitrión-huésped se puede aplicar a materiales autocurativos, materiales que responden a estímulos, fosforescencia a temperatura ambiente (RTP), mejora de propiedades mecánicas, etc. Los tamaños de las moléculas huésped y huésped desempeñan un papel esencial en las interacciones, y a continuación se analizarán algunos ejemplos típicos de interacciones con el huésped. [8] [9] [10] [11]
La química huésped-huésped es una rama de la química supramolecular en la que una molécula huésped se une a una denominada molécula o ion huésped. Los dos componentes del complejo interactúan mediante fuerzas no covalentes, más comúnmente mediante enlaces de hidrógeno . La unión entre huésped y huésped puede ser muy selectiva, en cuyo caso la interacción se denomina reconocimiento molecular . A menudo, existe un equilibrio dinámico entre los estados ligados y libres:
El componente "huésped" es a menudo la molécula más grande y encierra a la molécula más pequeña, "huésped". En los sistemas biológicos, los términos análogos de huésped y huésped se denominan comúnmente enzima y sustrato, respectivamente. [12]

Los éteres corona son estructuras en forma de anillos compuestas de varias unidades de etilenglicol. Debido a que el radio de sus poros es similar al de los iones de metales alcalinos, los éteres corona son bien conocidos por su capacidad para unir iones metálicos. Por ejemplo, 12-corona-4, 15-corona-5, 18-corona-6, 21-corona-7 y 24-corona-8 interactúan con iones de potasio, sodio, amonio y calcio, respectivamente. [8] Entre los éteres de corona antes mencionados, todos los iones tienen la afinidad de unión más fuerte con 18-crown-6 porque el tamaño de 18-crown-6 se asemeja más al de los iones. Además de las especies iónicas, los éteres corona también pueden unirse a moléculas neutras, por ejemplo , 1, 2, 3-triazol. Los éteres corona también pueden estar entrelazados con moléculas y/o polímeros largos y lineales, dando lugar a estructuras supramoleculares llamadas rotaxanos. Dado que los éteres de la corona no están unidos a las cadenas, pueden moverse hacia arriba y hacia abajo a lo largo de la molécula. [11]
La ciclodextrina (CD) se compone de varias unidades de glucosa y se conecta mediante enlaces éter. Hay tres tipos de CD, α-CD (6 unidades), β-CD (7 unidades) y γ-CD (8 unidades). Las alturas de la estructura rondan los 8 Å, mientras que los tamaños de las cavidades son diferentes, alrededor de 5, 6 y 8 Å, respectivamente. Comparando el tamaño de la molécula huésped y el CD, se puede predecir el comportamiento de unión. Por ejemplo, si la molécula huésped es más grande que la CD, se puede suponer que no se producirá la unión. Normalmente, la α-CD puede enhebrarse en una cadena de PEG, mientras que la γ-CD puede enhebrarse en 2 cadenas de PEG. La β-CD puede unirse a una molécula basada en tiofeno. [8]

La estructura de los criptofanos contiene 6 anillos de fenilo, principalmente conectados de 4 formas. Debido a los grupos fenilo y las cadenas alifáticas, las jaulas dentro de los criptofanos son altamente hidrofóbicas, lo que sugiere la capacidad de capturar moléculas no polares. En base a esto, se pueden emplear criptófanos para capturar xenón en solución acuosa, lo que podría resultar útil en estudios biológicos. [8]
A continuación se muestra una de las estructuras clásicas de resorcinarenos y pirogalolarenos. Debido al grupo fenol, se forman algunos enlaces de hidrógeno entre las moléculas. A veces, la proporción de vinculación entre el anfitrión y el huésped puede llegar a 2: 1. [8]
Los cucurbit[n]urilos tienen un tamaño similar de γ-CD, que también se comportan de manera similar ( por ejemplo , 1 cucurbit[n]uril puede enhebrarse en 2 cadenas de PEG). [8]
La termodinámica de la interacción entre el anfitrión y el huésped se puede evaluar mediante espectroscopia de RMN, espectroscopia UV/visible y calorimetría de titulación isotérmica. [13] El análisis cuantitativo de valores constantes vinculantes proporciona información termodinámica útil. [12]
Una constante de asociación se puede definir mediante la expresión
donde {HG} es la actividad termodinámica del complejo en equilibrio. {H} representa la actividad del anfitrión y {G} la actividad del invitado. Las cantidades , y son las concentraciones correspondientes y es un cociente de coeficientes de actividad .
En la práctica, la constante de equilibrio suele definirse en términos de concentraciones.
Cuando se utiliza esta definición, se da a entender que el cociente de coeficientes de actividad tiene un valor numérico de uno. Entonces parece que la constante de equilibrio tiene la dimensión 1/concentración, pero eso no puede ser cierto ya que el cambio de energía libre de Gibbs estándar es proporcional al logaritmo de K.
Esta aparente paradoja se resuelve cuando la dimensión de se define como el recíproco de la dimensión del cociente de concentraciones. La implicación es que se considera que tiene un valor constante en todas las condiciones experimentales relevantes. Sin embargo, es una práctica común asignar una dimensión, como milimoles por litro o micromoles por litro, a un valor de K que se ha determinado experimentalmente.
Un valor Grande indica que las moléculas huésped e huésped interactúan fuertemente para formar el complejo huésped-huésped.
Cuando las moléculas huésped y huésped se combinan para formar un solo complejo, el equilibrio se representa como
y la constante de equilibrio, K, se define como
donde [X] denota la concentración de una especie química X (se supone que todos los coeficientes de actividad tienen un valor numérico de 1). Las ecuaciones de balance de masa, en cualquier punto de datos,
donde y representan las concentraciones totales, de anfitrión y huésped, se pueden reducir a una única ecuación cuadrática en, digamos, [G] y, por lo tanto, se puede resolver analíticamente para cualquier valor dado de K. Las concentraciones [H] y [HG] pueden luego derivado.
El siguiente paso en el cálculo es calcular el valor, , de una cantidad correspondiente a la cantidad observada . Entonces, una suma de cuadrados, U, sobre todos los puntos de datos, np, se puede definir como
y esto se puede minimizar con respecto al valor de la constante de estabilidad, K, y un parámetro tal como el desplazamiento químico de la especie HG (datos de RMN) o su absorbencia molar (datos de uv/vis). La minimización se puede realizar en una aplicación de hoja de cálculo como EXCEL utilizando la utilidad SOLVER incorporada.
Este procedimiento es aplicable a aductos 1:1.
Con los espectros de resonancia magnética nuclear (RMN), el valor de desplazamiento químico observado, δ , que surge de un átomo dado contenido en una molécula de reactivo y uno o más complejos de ese reactivo, será el promedio ponderado por concentración de todos los desplazamientos de esas especies químicas. Se supone que el intercambio químico es rápido en la escala de tiempo de RMN. términos de fracciones molares ,
es el desplazamiento químico de la i -ésima especie química que contiene el núcleo y es la concentración/fracción molar ( c es una concentración/mol dm −3 ) de esa especie. Esta expresión tiene la misma forma matemática que la ley de Beer . Se pueden obtener valores de desplazamiento químico para más de un núcleo de forma análoga a la medida de la absorbancia en más de una longitud de onda. Los isótopos típicos que se pueden utilizar en este contexto son 1 H, 13 C y 31 P. Es habitual utilizar un disolvente deuterado al medir los valores de desplazamiento químico de 1 H.

Se supone que la absorbancia de cada especie es proporcional a la concentración de esa especie, según la ley de Beer-Lambert .
donde λ es una longitud de onda, es la longitud del camino óptico de la cubeta que contiene la solución de los N compuestos ( cromóforos ), es la absorbancia molar (también conocida como coeficiente de extinción) de la i -ésima especie química en la longitud de onda λ, c i es su concentración. Cuando las concentraciones se han calculado como se indicó anteriormente y se ha medido la absorbancia para muestras con diversas concentraciones de huésped y huésped, la ley de Beer-Lambert proporciona un conjunto de ecuaciones, a una longitud de onda determinada, que se pueden resolver mediante mínimos cuadrados lineales. proceso para los valores desconocidos del coeficiente de extinción en esa longitud de onda.
El tratamiento de este tipo de datos es similar al tratamiento de los datos de absorbancia. De hecho, la ecuación que define la relación entre la intensidad fluorescente y las concentraciones de especies es muy similar.
¿Dónde está la intensidad fluorescente de la iésima especie en concentración unitaria?
El calor desprendido cuando se agrega una alícuota de la solución huésped a una solución que contiene el huésped es la suma de las contribuciones de cada reacción.
donde es un valor de cambio de calor medido (corregido por todas las contribuciones de calor extraño) en el punto de datos j , es la cantidad de calor absorbido o emitido cuando se forma 1 mol del iésimo producto de reacción y es el cambio real en el número de moles de ese producto en ese punto de datos. se calcula resolviendo las ecuaciones de equilibrio de masa con valores dados de las constantes de equilibrio. Si se conocen los valores de la constante de equilibrio, el cambio de entalpía estándar puede calcularse mediante un proceso lineal de mínimos cuadrados; de lo contrario, se debe utilizar un método no lineal de ajuste de datos.
La calorimetría de titulación isotérmica se utiliza comúnmente para determinar los valores tanto de una constante de equilibrio como de la entalpía de reacción estándar correspondiente. Los fabricantes de instrumentos ITC suministran algún software con el que se pueden obtener estas cantidades a partir de valores de datos experimentales.
Para cada equilibrio que involucra un anfitrión, H, y un huésped G
la constante de equilibrio, , se define como
Los valores de las concentraciones libres, y se obtienen resolviendo las ecuaciones de balance de masa con valores conocidos o estimados para las constantes de estabilidad.
Luego, las concentraciones de cada especie compleja también se pueden calcular como La relación entre la concentración de una especie y la cantidad medida es específica de la técnica de medición, como se indica en cada sección anterior. Utilizando esta relación, el conjunto de parámetros, los valores de las constantes de estabilidad y los valores de propiedades como la absortividad molar o los desplazamientos químicos específicos, pueden refinarse mediante un proceso de refinamiento no lineal de mínimos cuadrados . Para una exposición más detallada de la teoría véase Determinación de constantes de equilibrio . Algunos programas informáticos dedicados se enumeran en Implementaciones .
El proceso de unión es reversible, lo que indica que la constante asociada (k a ) no es mucho mayor que la constante disociada (k d ). Combinando la velocidad de la reacción, ka , kd , la concentración y el tiempo, se puede calcular la relación entre la molécula huésped libre y el tiempo. [14] Calculando la integración del espectro UV o RMN , [15] [14] se puede obtener la concentración en función de la curva de tiempo.
En cooperatividad, la unión inicial del ligando afecta la afinidad del huésped por los ligandos posteriores. En la cooperatividad positiva, el primer evento de unión mejora la afinidad del huésped por otro ligando. Ejemplos de cooperatividad positiva y negativa son la hemoglobina y el receptor de aspartato, respectivamente. [dieciséis]

Se han estudiado las propiedades termodinámicas de la cooperatividad con el fin de definir parámetros matemáticos que distingan la cooperatividad positiva o negativa. La ecuación tradicional de energía libre de Gibbs establece: . Sin embargo, para cuantificar la cooperatividad en un sistema huésped-huésped, es necesario considerar la energía de enlace. El esquema de la derecha muestra la unión de A, la unión de B, la unión cooperativa positiva de A – B y, por último, la unión cooperativa negativa de A – B. Por lo tanto, una forma alternativa de la ecuación de energía libre de Gibbs sería
dónde:
Se considera que si es mayor que la suma de y , es positivamente cooperativo. Si es menor, entonces es cooperativa negativa. [17] La química huésped-huésped no se limita a las interacciones entre receptor y huésped. También se demuestra en sistemas de emparejamiento de iones. Estas interacciones se estudian en un medio acuoso utilizando huéspedes organometálicos sintéticos y moléculas invitadas orgánicas. Por ejemplo, un receptor policatiónico que contiene cobre (el huésped) está coordinado con moléculas como tetracarboxilatos, tricarbalato, aspartato y acetato (los huéspedes). Este estudio ilustra que la entropía , más que la entalpía, determina la energía de enlace del sistema, lo que conduce a una cooperatividad negativa. El gran cambio de entropía se origina por el desplazamiento de las moléculas de disolvente que rodean al ligando y al receptor. Cuando varios acetatos se unen al receptor, se liberan más moléculas de agua al medio ambiente que un tetracarboxilato. Esto provocó una disminución de la energía libre, lo que implica que el sistema está cooperando negativamente. [18] En un estudio similar, utilizando guanidinio y Cu (II) y policarboxilato invitados, se demuestra que la cooperación positiva está determinada en gran medida por la entalpía. [19] Además de los estudios termodinámicos, la química huésped-huésped también tiene aplicaciones biológicas.

Debido a la interacción huésped-huésped no covalente, la columna vertebral del polímero puede tener suficiente flexibilidad para difundirse. Si existe una grieta en los materiales, después de comprimir los dos materiales alrededor de la grieta, debido al rápido intercambio de la estructura molecular huésped-huésped, la grieta se volverá a unir revelando buenas propiedades de autocuración. Harada et al informaron sobre un hidrogel autorreparable construido con ciclodextrina modificada con grupos vinilo y adamantano. [20] [22] Otra estrategia es utilizar la interacción entre la columna vertebral del polímero y la molécula huésped (la molécula huésped se enrosca en el polímero). Si el proceso de enhebrado es lo suficientemente rápido, también se puede lograr la autocuración. [21]
Generalmente, no es fácil lograr fosforescencia orgánica pura, en parte debido a la inestabilidad del estado triplete (puede apagarse fácilmente con humedad, oxígeno, etc.). Las estructuras anfitrión-huésped pueden proporcionar una matriz rígida, que protege el estado triplete para que no se apague. En esta circunstancia, se podrían utilizar α-CD y CB, [23] [24] en los que el fósforo sirve como invitado para interactuar con el huésped. Por ejemplo, los derivados de 4-fenilpiridio interactúan con CB y se copolimerizan con acrilamida . El polímero resultante produjo ~2 s de vida útil de fosforescencia. Además, Zhu et al utilizaron éter corona e iones de potasio para modificar el polímero y mejorar la emisión de fosforescencia. [25]
Algunas moléculas invitadas son compuestos cargados que pueden oxidarse o reducirse mediante determinadas sustancias químicas. Este tipo de molécula invitada puede presentar capacidad de respuesta redox. Algunas moléculas huésped ( es decir , α-CD) o moléculas invitadas ( es decir , ion tetraamonio) son sensibles al pH; un pH diferente puede dar como resultado especies diferentes, lo que influye significativamente en el comportamiento de unión, dando al material propiedades de respuesta al pH. Algunas moléculas invitadas pueden cambiar sus configuraciones bajo diferentes luces, lo que hace que el material sea fotorresponsivo. [26] Cai et al emplearon un enlace halógeno para preparar un sistema huésped-huésped, y los materiales responden al calor y a los mecanismos con una emisión prolongada y persistente. [27]
Wang et al construyeron un sistema de cifrado construido con pilar [5] areno, espiropirano y pentanonitrilo (en estado libre e injertado en polímero) . Después de la irradiación ultravioleta, el espiropirano se transformaría en merocianina. Cuando la luz visible incidió sobre el material, la merocianina cercana al complejo de pentanonitrilo libre de pilar [5] areno tuvo una transformación más rápida a espiropirano; por el contrario, el complejo de pentanonitrilo injertado cerca del areno pilar [5] tiene una tasa de transformación mucho más lenta. Esta transformación de espiropirano-merocianina se puede utilizar para cifrar mensajes. [28] Otra estrategia se basa en las jaulas metálicas y los hidrocarburos aromáticos policíclicos. [29] Debido a las diferencias de emisión fluorescente entre el complejo y las jaulas, la información podría cifrarse.
Aunque algunas interacciones anfitrión-huésped no son fuertes, aumentar la cantidad de interacción anfitrión-huésped puede mejorar las propiedades mecánicas de los materiales. Como ejemplo, unir las moléculas huésped al polímero es una de las estrategias comúnmente utilizadas para aumentar las propiedades mecánicas del polímero. A las moléculas huésped les lleva tiempo desenroscarse del polímero, lo que puede ser una forma de disipación de energía. [22] [30] [31] Otro método es utilizar la interacción de intercambio lento entre anfitrión e invitado. Aunque el intercambio lento mejora las propiedades mecánicas, al mismo tiempo se sacrifican las propiedades de autocuración. [32]
Tradicionalmente, la detección química se ha abordado con un sistema que contiene un indicador unido covalentemente a un receptor a través de un conector. Una vez que el analito se une, el indicador cambia de color o se vuelve fluorescente. Esta técnica se denomina enfoque indicador-espaciador-receptor (ISR). [33] A diferencia del ISR, el ensayo de desplazamiento de indicador (IDA) utiliza una interacción no covalente entre un receptor (el huésped), un indicador y un analito (el huésped). Al igual que ISR, IDA también utiliza indicadores colorimétricos (C-IDA) y de fluorescencia (F-IDA). En un ensayo IDA, se incuba un receptor con el indicador. Cuando se agrega el analito a la mezcla, el indicador se libera al medio ambiente. Una vez que se libera el indicador, cambia de color (C-IDA) o se vuelve fluorescente (F-IDA). [34]
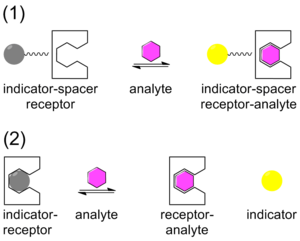
IDA ofrece varias ventajas frente al enfoque tradicional de detección química ISR. En primer lugar, no requiere que el indicador esté unido covalentemente al receptor. En segundo lugar, al no existir enlace covalente, se pueden utilizar varios indicadores con el mismo receptor. Por último, los medios en los que se puede utilizar el ensayo son diversos. [35]

Las técnicas de detección química como el C-IDA tienen implicaciones biológicas. Por ejemplo, la protamina es un coagulante que se administra habitualmente después de la cirugía cardiopulmonar y que contrarresta la actividad anticoagulante de la herapina. Para cuantificar la protamina en muestras de plasma, se utiliza un ensayo de desplazamiento colorimétrico. El tinte Azure A es azul cuando no está unido, pero cuando está unido a herapina, muestra un color púrpura. La unión entre Azure A y la heparina es débil y reversible. Esto permite que la protamina desplace a Azure A. Una vez que se libera el tinte, muestra un color púrpura. El grado en que se desplaza el tinte es proporcional a la cantidad de protamina en el plasma. [36]
Kwalczykowski y sus colaboradores han utilizado F-IDA para monitorear las actividades de la helicasa en E. coli . En este estudio utilizaron naranja de tiazol como indicador. La helicasa desenrolla el dsDNA para producir ssDNA. La intensidad de fluorescencia del naranja de tiazol tiene una mayor afinidad por el ADNds que el ADNss y su intensidad de fluorescencia aumenta cuando está unido al ADNds que cuando no está unido. [37] [38]
Un sólido cristalino ha sido visto tradicionalmente como una entidad estática donde los movimientos de sus componentes atómicos se limitan a su equilibrio vibratorio. Como se ve en la transformación de grafito en diamante, la transformación de sólido a sólido puede ocurrir bajo presión física o química. Se ha propuesto que la transformación de una disposición cristalina a otra se produzca de forma cooperativa. [39] [40] La mayoría de estos estudios se han centrado en el estudio de una estructura orgánica o metal-orgánica. [41] [42] Además de los estudios de transformación cristalina macromolecular, también hay estudios de moléculas monocristalinas que pueden cambiar su conformación en presencia de disolventes orgánicos. Se ha demostrado que un complejo organometálico se transforma en varias orientaciones dependiendo de si está expuesto a vapores de disolvente o no. [43]
Se han utilizado sistemas de huéspedes anfitriones para eliminar materiales peligrosos del medio ambiente. Se pueden fabricar en diferentes tamaños y formas para atrapar una variedad de invitados químicos. Una aplicación es la capacidad del p-terc-butycalix[4]areno para atrapar un ion de cesio. El cesio-137 es radiactivo y es necesario eliminarlo de los desechos nucleares de manera eficiente. La química huésped-huésped también se ha utilizado para eliminar del agua aminas aromáticas cancerígenas y sus derivados N-nitroso. Estos materiales de desecho se utilizan en muchos procesos industriales y se encuentran en una variedad de productos como: pesticidas, medicamentos y cosméticos. [44] [45]
{{cite book}}: CS1 maint: location missing publisher (link) CS1 maint: others (link)