La estreptavidina / ˌ s t r ɛ p ˈ t æ v ɪ d ɪ n / es una proteína (tetrámero) de 52 kDa purificada a partir de la bacteria Streptomyces avidinii . Los homotetrámeros de estreptavidina tienen una afinidad extraordinariamente alta por la biotina (también conocida como vitamina B7 o vitamina H). Con una constante de disociación (K d ) del orden de ≈10 −14 mol/L, [1] la unión de la biotina a la estreptavidina es una de las interacciones no covalentes más fuertes conocidas en la naturaleza. La estreptavidina se utiliza ampliamente en biología molecular y bionanotecnología debido a la resistencia del complejo estreptavidina-biotina a disolventes orgánicos, desnaturalizantes (p. ej., cloruro de guanidinio ), detergentes (p. ej. , SDS , Triton X-100 ), enzimas proteolíticas y temperaturas y pH extremos.
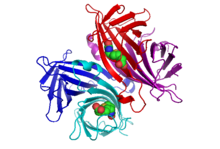
La estructura cristalina de la estreptavidina unida a biotina fue informada por dos grupos en 1989. La estructura fue resuelta mediante difracción anómala de múltiples longitudes de onda por Hendrickson et al. [2] en la Universidad de Columbia y utilizando reemplazo isomorfo múltiple por Weber et al. [3] en el Departamento Central de Investigación y Desarrollo de EI DuPont. A septiembre de 2017, existen 171 estructuras depositadas en el Protein Data Bank . Consulte este enlace para obtener una lista completa. Los extremos N y C de la proteína de longitud completa de 159 residuos se procesan para dar una estreptavidina "central" más corta, generalmente compuesta por los residuos 13 a 139; La eliminación de los extremos N y C es necesaria para lograr la mayor afinidad de unión a biotina. La estructura secundaria de un monómero de estreptavidina está compuesta por ocho cadenas β antiparalelas, que se pliegan para dar una estructura terciaria de barril β antiparalela. Un sitio de unión de biotina está ubicado en un extremo de cada barril β. Cuatro monómeros de estreptavidina idénticos (es decir, cuatro barriles β idénticos) se asocian para dar la estructura cuaternaria tetramérica de la estreptavidina. El sitio de unión de biotina en cada barril consta de residuos del interior del barril, junto con un Trp120 conservado de una subunidad vecina. De esta manera, cada subunidad contribuye al sitio de unión de la subunidad vecina, por lo que el tetrámero también puede considerarse un dímero de dímeros funcionales.
Las numerosas estructuras cristalinas del complejo estreptavidina-biotina han arrojado luz sobre el origen de esta notable afinidad. En primer lugar, existe una alta complementariedad de forma entre la bolsa de unión y la biotina. En segundo lugar, se forma una extensa red de enlaces de hidrógeno con la biotina cuando se encuentra en el sitio de unión. Hay ocho enlaces de hidrógeno formados directamente con residuos en el sitio de unión (la llamada "primera capa" de enlaces de hidrógeno), que involucran los residuos Asn23, Tyr43, Ser27, Ser45, Asn49, Ser88, Thr90 y Asp128. También hay una "segunda capa" de enlaces de hidrógeno que involucra residuos que interactúan con los residuos de la primera capa. Sin embargo, la afinidad estreptavidina-biotina excede la que se podría predecir a partir de las interacciones de los enlaces de hidrógeno únicamente, lo que sugiere otro mecanismo que contribuye a la alta afinidad. [4] La bolsa de unión de biotina es hidrofóbica , y existen numerosos contactos mediados por la fuerza de Van der Waals e interacciones hidrofóbicas realizadas con la biotina cuando está en la bolsa, lo que también se cree que explica la alta afinidad. En particular, la bolsa está revestida de residuos de triptófano conservados. Por último, la unión de la biotina va acompañada de la estabilización de un bucle flexible que conecta las cadenas β 3 y 4 (L3/4), que se cierra sobre la biotina unida, actuando como una "tapa" sobre el bolsillo de unión y contribuyendo a la biotina extremadamente lenta. tasa de disociación.
La mayoría de los intentos de mutar la estreptavidina dan como resultado una menor afinidad de unión a la biotina, lo que es de esperar en un sistema tan altamente optimizado. Sin embargo, se descubrió que un mutante de estreptavidina diseñado recientemente, llamado traptavidina, tiene una disociación de biotina diez veces más lenta, además de una mayor estabilidad térmica y mecánica. [5] Esta disminución de la tasa de disociación estuvo acompañada por una disminución del doble en la tasa de asociación.
La afinidad de unión a la biotina puede verse afectada por el marcaje químico de la estreptavidina, como con los fluoróforos reactivos con aminas ; La flavidina es un mutante de estreptavidina sin cadenas laterales de lisina, que conserva buenas características de unión a biotina después del marcaje con tinte fluorescente donde el tinte se acopla al extremo amino. [6]
Entre los usos más comunes de la estreptavidina se encuentran la purificación o detección de diversas biomoléculas. La fuerte interacción estreptavidina-biotina se puede utilizar para unir varias biomoléculas entre sí o sobre un soporte sólido. Se necesitan condiciones duras para romper la interacción estreptavidina-biotina, que a menudo desnaturaliza la proteína de interés que se está purificando. Sin embargo, se ha demostrado que una breve incubación en agua por encima de 70 °C romperá reversiblemente la interacción (al menos para el ADN biotinilado) sin desnaturalizar la estreptavidina, lo que permitirá la reutilización del soporte sólido de estreptavidina. [7] Otra aplicación de la estreptavidina es la purificación y detección de proteínas modificadas genéticamente con el péptido Strep-tag . La estreptavidina se usa ampliamente en transferencias Western e inmunoensayos conjugados con alguna molécula informadora, como la peroxidasa de rábano picante . La estreptavidina también se ha utilizado en el campo en desarrollo de la nanobiotecnología , el uso de moléculas biológicas como proteínas o lípidos para crear dispositivos/estructuras a nanoescala . En este contexto, la estreptavidina se puede utilizar como componente básico para unir moléculas de ADN biotinilado para crear estructuras de nanotubos de carbono de pared simple [8] o incluso poliedros de ADN complejos. [9] La estreptavidina tetramérica también se ha utilizado como centro alrededor del cual se pueden organizar otras proteínas, ya sea mediante una etiqueta de afinidad como Strep-tag o AviTag o mediante fusión genética con SpyTag . [10] Fusion to SpyTag permitió la generación de ensamblajes con 8 o 20 subunidades de estreptavidina. Además de una sonda de fuerza molecular para estudios de microscopía de fuerza atómica , [11] también se han creado nuevos materiales como redes cristalinas tridimensionales [12] . La estreptavidina tiene un punto isoeléctrico (pI) ligeramente ácido de ~5, pero también está disponible comercialmente una forma recombinante de estreptavidina con un pI casi neutro.
La inmunoterapia predirigida utiliza estreptavidina conjugada con un anticuerpo monoclonal contra antígenos específicos de las células cancerosas, seguida de una inyección de biotina radiomarcada para administrar la radiación solo a la célula cancerosa. Los obstáculos iniciales implican la saturación de los sitios de unión de biotina en la estreptavidina con biotina endógena en lugar de la biotina radiomarcada inyectada, y un alto grado de exposición radiactiva en los riñones debido a las fuertes propiedades de adsorción celular de la estreptavidina. Actualmente se cree que este alto nivel de unión a tipos de células adherentes, como plaquetas activadas y melanomas, es el resultado de la unión de integrinas mediada por la secuencia RYD en la estreptavidina. [13]

La estreptavidina es un tetrámero y cada subunidad se une a la biotina con igual afinidad. La multivalencia es una ventaja en aplicaciones como la tinción de tetrámeros de MHC , donde los efectos de avidez mejoran la capacidad de las moléculas de MHC unidas a la estreptavidina para detectar células T específicas. [14] En otros casos, como el uso de estreptavidina para obtener imágenes de proteínas específicas en las células, la multivalencia puede perturbar la función de la proteína de interés. La estreptavidina monovalente es una forma recombinante diseñada de estreptavidina que es un tetrámero pero sólo uno de los cuatro sitios de unión es funcional. Este sitio de unión único tiene una afinidad de 10 −14 mol/L y no puede causar reticulación. [15] Las aplicaciones de la estreptavidina monovalente han incluido el seguimiento fluorescente de receptores de la superficie celular , la decoración de origami de ADN y la actuación como puntero para identificar regiones específicas para microscopía crioelectrónica .
La estreptavidina monomérica es una forma recombinante de estreptavidina con mutaciones para romper el tetrámero en un monómero y mejorar la solubilidad de la subunidad aislada resultante. Las versiones monoméricas de estreptavidina tienen una afinidad por la biotina de 10 −7 mol/L 10 −8 mol/L y, por lo tanto, no son ideales para aplicaciones de etiquetado, pero son útiles para la purificación, donde es deseable la reversibilidad. [16] [17]

Se puede producir una estreptavidina con exactamente dos sitios de unión de biotina por tetrámero mezclando subunidades con y sin un sitio de unión de biotina funcional y purificando mediante cromatografía de intercambio iónico . Los sitios de unión funcionales aquí tienen la misma estabilidad de unión a biotina que la estreptavidina de tipo salvaje. La estreptavidina divalente con los dos sitios de unión de biotina juntos (cis-divalente) o separados (trans-divalente) se puede purificar por separado. [18]
También se puede producir una estreptavidina con exactamente tres sitios de unión de biotina por tetrámero utilizando el mismo principio que para producir estreptavidinas divalentes. [19]
Las estreptavidinas de mayor valencia se han obtenido utilizando la química de la conjugación de enlaces isopeptídicos utilizando la tecnología SpyTag/SpyCatcher . [20] Esto implica tener un tetrámero de estreptavidina con tres sitios de unión a biotina y una estreptavidina muerta fusionada a SpyTag o SpyCatcher. Cuando los diferentes tetrámeros se mezclan, se produce un enlace covalente para permitir un mayor número de sitios de unión de biotina. Con este método se han creado seis y doce sitios de unión de biotina por molécula.
La estreptavidina no es la única proteína capaz de unirse a la biotina con alta afinidad. La avidina es la otra proteína de unión a biotina más notable. Originalmente aislada de la yema de huevo, la avidina solo tiene un 30% de identidad de secuencia con la estreptavidina, pero una estructura secundaria, terciaria y cuaternaria casi idéntica. La avidina tiene una mayor afinidad por la biotina ( K d ~ 10 −15 M), pero a diferencia de la estreptavidina, la avidina está glicosilada, tiene carga positiva y tiene actividad pseudocatalítica (la avidina puede mejorar la hidrólisis alcalina de un enlace éster entre la biotina y un nitrofenilo). grupo) y tiene una mayor tendencia a la agregación. Por otro lado, la estreptavidina es el mejor aglutinante del conjugado de biotina; La avidina tiene una afinidad de unión menor que la estreptavidina cuando la biotina se conjuga con otra molécula, a pesar de que la avidina tiene mayor afinidad por la biotina libre no conjugada. Debido a que la estreptavidina carece de modificaciones de carbohidratos y tiene un pI casi neutro , tiene la ventaja de una unión no específica mucho menor que la avidina. La avidina desglicosilada (NeutrAvidin) es más comparable al tamaño, pI y unión no específica de la estreptavidina.
Grupos que investigan y desarrollan estreptavidina o proteínas de la familia de la avidina (orden alfabético)