Los estados de espín al describir los complejos de coordinación de metales de transición se refieren a las posibles configuraciones de espín de los electrones d del metal central. Para varios estados de oxidación, los metales pueden adoptar configuraciones de alto y bajo espín . La ambigüedad sólo se aplica a los metales de la primera fila, porque los metales de la segunda y tercera fila son invariablemente de bajo giro. Estas configuraciones pueden entenderse a través de los dos modelos principales utilizados para describir complejos de coordinación; teoría del campo cristalino y teoría del campo del ligando (una versión más avanzada basada en la teoría de los orbitales moleculares ). [1]

La división Δ de los orbitales d juega un papel importante en el estado de espín electrónico de un complejo de coordinación. Tres factores afectan a Δ: el período (fila en la tabla periódica) del ion metálico, la carga del ion metálico y la intensidad de campo de los ligandos del complejo como se describe en la serie espectroquímica . Sólo los complejos octaédricos de metales de transición de primera fila adoptan estados de alto espín.
Para que se produzca una división de espín baja, el costo de energía de colocar un electrón en un orbital ya ocupado individualmente debe ser menor que el costo de colocar el electrón adicional en un orbital eg con un costo de energía de Δ. Si la energía requerida para emparejar dos electrones es mayor que el costo energético de colocar un electrón en un, por ejemplo , Δ, se produce una alta división de espín.
Si la separación entre los orbitales es grande, entonces los orbitales de menor energía se llenan completamente antes de que se poblaran los orbitales superiores según el principio de Aufbau . Los complejos como este se denominan de "bajo espín", ya que llenar un orbital coincide con los electrones y reduce el espín total de los electrones. Si la separación entre los orbitales es lo suficientemente pequeña, entonces es más fácil colocar electrones en los orbitales de mayor energía que colocar dos en el mismo orbital de baja energía, debido a la repulsión resultante de hacer coincidir dos electrones en el mismo orbital. Por lo tanto, se coloca un electrón en cada uno de los cinco orbitales d antes de que se produzca cualquier emparejamiento de acuerdo con la regla de Hund, lo que da como resultado lo que se conoce como un complejo de "alto espín". Complejos como este se denominan de "alto espín", ya que ocupar el orbital superior evita coincidencias entre electrones con espín opuesto.

La carga del centro metálico juega un papel en el campo del ligando y en la división Δ. Cuanto mayor es el estado de oxidación del metal, más fuerte es el campo de ligando que se crea. En el caso de que existan dos metales con la misma configuración electrónica d, es más probable que el que tenga mayor estado de oxidación tenga bajo espín que el que tenga menor estado de oxidación; por ejemplo, Fe 2+ y Co 3+ son ambos d 6 ; sin embargo, la mayor carga de Co 3+ crea un campo de ligando más fuerte que el Fe 2+ . En igualdad de condiciones, es más probable que el Fe 2+ tenga un alto espín que el Co 3+ .
Los ligandos también afectan la magnitud de la división Δ de los orbitales d según la intensidad de su campo, como se describe en la serie espectroquímica . Los ligandos de campo fuerte, como CN − y CO, aumentan la división Δ y es más probable que tengan bajo espín. Los ligandos de campo débil, como I − y Br −, provocan una división Δ más pequeña y es más probable que tengan un alto espín.
Algunos complejos octaédricos exhiben cruce de espín , donde los estados de espín alto y bajo existen en equilibrio dinámico.

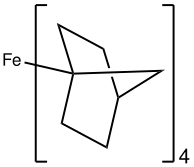
La energía de división Δ para complejos metálicos tetraédricos (cuatro ligandos), Δ tet, es menor que la de un complejo octaédrico. En consecuencia, los complejos tetraédricos son casi siempre de alto espín [3] Ejemplos de complejos tetraédricos de bajo espín incluyen Fe(2-norbornilo) 4 , [4] [Co(4-norbornilo) 4 ] + , y el complejo de nitrosilo Cr(NO)( (N(tms) 2 ) 3 .
Muchos complejos d 8 de los metales de la primera fila existen en geometría plana tetraédrica o cuadrada. En algunos casos, estas geometrías existen en equilibrios mensurables. Por ejemplo, el diclorobis (trifenilfosfina) níquel (II) se ha cristalizado en geometrías planas tanto tetraédricas como cuadradas. [5]
En términos de división de orbitales d, la teoría del campo de ligandos (LFT) y la teoría del campo cristalino (CFT) dan resultados similares. CFT es un modelo más antiguo y simple que trata a los ligandos como cargas puntuales. LFT es más químico, enfatiza el enlace covalente y se adapta explícitamente al enlace pi.
En el caso de complejos octaédricos, la cuestión de espín alto versus espín bajo surge primero para d 4 , ya que tiene más de 3 electrones para llenar los orbitales d no enlazantes según la teoría del campo de ligandos o los orbitales d estabilizados según el cristal. división de campos.
Todos los complejos de metales de la segunda y tercera fila son de bajo giro.
El estado de espín del complejo afecta el radio iónico de un átomo . Para un recuento de electrones d determinado, los complejos de alto espín son más grandes. [7]
Generalmente, las tasas de disociación de ligandos de complejos de bajo espín son más bajas que las tasas de disociación de complejos de alto espín. En el caso de complejos octaédricos, los electrones en los niveles eg son antienlazantes con respecto a los enlaces metal-ligando. Los famosos complejos "inertes al intercambio" son los complejos octaédricos de iones metálicos d 3 y d 6 de bajo espín , ilustrados respetuosamente por Cr 3+ y Co 3+ . [8]