
En química orgánica , un enlace peptídico es un tipo de enlace químico covalente de tipo amida que une dos alfa-aminoácidos consecutivos desde C1 ( carbono número uno) de un alfa-aminoácido y N2 ( nitrógeno número dos) de otro, a lo largo de una cadena peptídica o proteica . [1]
También se puede llamar enlace eupeptídico [1] para distinguirlo de un enlace isopeptídico , que es otro tipo de enlace amida entre dos aminoácidos.

Cuando dos aminoácidos forman un dipéptido a través de un enlace peptídico , [1] se trata de un tipo de reacción de condensación . [2] En este tipo de condensación, dos aminoácidos se aproximan entre sí, y la fracción de ácido carboxílico no lateral (C1) de uno se acerca a la fracción de amino no lateral (N2) del otro. Uno pierde un hidrógeno y oxígeno de su grupo carboxilo (COOH) y el otro pierde un hidrógeno de su grupo amino (NH 2 ). Esta reacción produce una molécula de agua (H 2 O) y dos aminoácidos unidos por un enlace peptídico (−CO−NH−). Los dos aminoácidos unidos se denominan dipéptido.
El enlace amida se sintetiza cuando el grupo carboxilo de una molécula de aminoácido reacciona con el grupo amino de la otra molécula de aminoácido, provocando la liberación de una molécula de agua (H 2 O), por lo tanto el proceso es una reacción de síntesis por deshidratación .
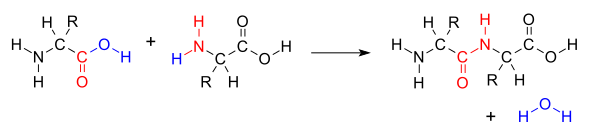
La formación del enlace peptídico consume energía, que, en los organismos, se deriva del ATP . [3] Los péptidos y las proteínas son cadenas de aminoácidos unidas por enlaces peptídicos (y, a veces, por algunos enlaces isopeptídicos ). Los organismos utilizan enzimas para producir péptidos no ribosómicos , [4] y ribosomas para producir proteínas mediante reacciones que difieren en detalles de la síntesis por deshidratación. [5]
Algunos péptidos, como la alfa-amanitina , se denominan péptidos ribosómicos porque están formados por ribosomas, [6] pero muchos son péptidos no ribosómicos porque son sintetizados por enzimas especializadas en lugar de ribosomas. Por ejemplo, el tripéptido glutatión se sintetiza en dos pasos a partir de aminoácidos libres , por dos enzimas : la glutamato-cisteína ligasa (forma un enlace isopeptídico , que no es un enlace peptídico) y la glutatión sintetasa (forma un enlace peptídico). [7] [8]
Un enlace peptídico se puede romper por hidrólisis (la adición de agua). La hidrólisis de enlaces peptídicos en agua libera de 8 a 16 kJ / mol (2 a 4 kcal / mol ) de energía de Gibbs . [9] Este proceso es extremadamente lento, con una vida media a 25 °C de entre 350 y 600 años por enlace. [10]
En los organismos vivos, el proceso normalmente es catalizado por enzimas conocidas como peptidasas o proteasas , aunque hay informes de hidrólisis de enlaces peptídicos causada por tensión conformacional a medida que el péptido/proteína se pliega a la estructura nativa. [11] Por lo tanto, este proceso no enzimático no se acelera por la estabilización del estado de transición, sino por la desestabilización del estado fundamental.
La longitud de onda de absorción de un enlace peptídico es de 190 a 230 nm, [12] lo que lo hace particularmente susceptible a la radiación UV .
La deslocalización significativa del par solitario de electrones en el átomo de nitrógeno le da al grupo un carácter de doble enlace parcial . El doble enlace parcial hace que el grupo amida sea planar , y se presenta en los isómeros cis o trans . En el estado desplegado de las proteínas, los grupos peptídicos son libres de isomerizarse y adoptar ambos isómeros; sin embargo, en el estado plegado, solo se adopta un único isómero en cada posición (con raras excepciones). La forma trans es la preferida abrumadoramente en la mayoría de los enlaces peptídicos (aproximadamente una proporción de 1000:1 en las poblaciones trans:cis). Sin embargo, los grupos peptídicos X-Pro tienden a tener una proporción de aproximadamente 30:1, presumiblemente porque la simetría entre los átomos C α y C δ de la prolina hace que los isómeros cis y trans sean casi iguales en energía, como se muestra en la figura siguiente.
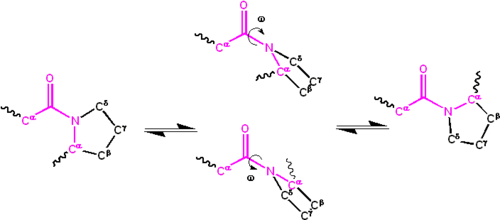
El ángulo diedro asociado con el grupo peptídico (definido por los cuatro átomos C α –C'–N–C α ) se denota ; para el isómero cis ( conformación sinperiplanar ), y para el isómero trans ( conformación antiperiplanar ). Los grupos amida pueden isomerizarse alrededor del enlace C'–N entre las formas cis y trans, aunque lentamente ( segundos a temperatura ambiente). Los estados de transición requieren que se rompa el doble enlace parcial, de modo que la energía de activación sea de aproximadamente 80 kJ/mol (20 kcal/mol). Sin embargo, la energía de activación se puede reducir (y la isomerización catalizada ) mediante cambios que favorezcan la forma de enlace simple, como colocar el grupo peptídico en un entorno hidrófobo o donar un enlace de hidrógeno al átomo de nitrógeno de un grupo peptídico X-Pro. Ambos mecanismos para reducir la energía de activación se han observado en las peptidil prolil isomerasas (PPIasas), que son enzimas naturales que catalizan la isomerización cis-trans de los enlaces peptídicos X-Pro.
El plegamiento conformacional de proteínas suele ser mucho más rápido (normalmente, entre 10 y 100 ms) que la isomerización cis-trans (entre 10 y 100 s). Un isómero no nativo de algunos grupos peptídicos puede alterar significativamente el plegamiento conformacional, ya sea ralentizándolo o impidiendo que se produzca hasta que se alcance el isómero nativo. Sin embargo, no todos los grupos peptídicos tienen el mismo efecto sobre el plegamiento; los isómeros no nativos de otros grupos peptídicos pueden no afectar en absoluto al plegamiento.
Debido a su estabilización por resonancia, el enlace peptídico es relativamente poco reactivo en condiciones fisiológicas, incluso menos que compuestos similares como los ésteres . Sin embargo, los enlaces peptídicos pueden sufrir reacciones químicas, generalmente a través de un ataque de un átomo electronegativo al carbono carbonílico , rompiendo el doble enlace carbonílico y formando un intermedio tetraédrico. Esta es la vía seguida en la proteólisis y, de forma más general, en reacciones de intercambio de N–O acilo como las de las inteínas . Cuando el grupo funcional que ataca al enlace peptídico es un tiol , hidroxilo o amina , la molécula resultante puede denominarse ciclol o, más específicamente, tiaciclol, oxaciclol o azaciclol, respectivamente.
{{cite book}}: |journal=ignorado ( ayuda )