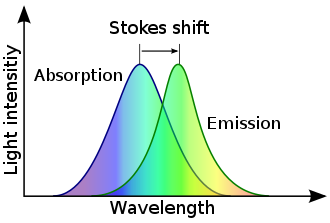
El desplazamiento de Stokes es la diferencia (en unidades de energía , número de onda o frecuencia ) entre las posiciones de los máximos de banda de los espectros de absorción y emisión ( la fluorescencia y el Raman son dos ejemplos) de la misma transición electrónica. [1] Recibe su nombre en honor al físico irlandés George Gabriel Stokes . [2] [3] [4]

Cuando un sistema (ya sea una molécula o un átomo ) absorbe un fotón , gana energía y entra en un estado excitado . El sistema puede relajarse emitiendo un fotón. El desplazamiento de Stokes se produce cuando la energía del fotón emitido es menor que la del fotón absorbido, lo que representa la diferencia de energía entre los dos fotones.
El desplazamiento de Stokes es principalmente el resultado de dos fenómenos: relajación o disipación vibracional y reorganización del disolvente. Un fluoróforo es una parte de una molécula con un momento dipolar que exhibe fluorescencia. Cuando un fluoróforo entra en un estado excitado, su momento dipolar cambia, pero las moléculas de disolvente circundantes no pueden ajustarse tan rápidamente. Solo después de la relajación vibracional sus momentos dipolares se realinean. [5]
Los desplazamientos de Stokes se expresan en unidades de longitud de onda, pero esto es menos significativo que las unidades de energía, número de onda o frecuencia porque depende de la longitud de onda de absorción. Por ejemplo, un desplazamiento de Stokes de 50 nm a partir de una absorción a 300 nm es mayor en términos de energía que un desplazamiento de Stokes de 50 nm a partir de una absorción a 600 nm.

La fluorescencia de Stokes es la emisión de un fotón de longitud de onda más larga (menor frecuencia o energía) por una molécula que ha absorbido un fotón de longitud de onda más corta (mayor frecuencia o energía). [6] [7] [8] Tanto la absorción como la radiación (emisión) de energía son distintivas para una estructura molecular particular. Si un material tiene una banda prohibida directa en el rango de la luz visible, la luz que brilla sobre él es absorbida, lo que excita a los electrones a un estado de mayor energía. Los electrones permanecen en el estado excitado durante unos 10 −8 segundos. Este número varía en varios órdenes de magnitud, dependiendo de la muestra, y se conoce como el tiempo de vida de fluorescencia de la muestra. Después de perder una pequeña cantidad de energía a través de la relajación vibracional, la molécula regresa al estado fundamental y se emite energía.
Si el fotón emitido tiene más energía que el fotón absorbido, la diferencia de energía se denomina desplazamiento anti-Stokes ; [9] esta energía adicional proviene de la disipación de fonones térmicos en una red cristalina, enfriando el cristal en el proceso. Los desplazamientos anti-Stokes también pueden deberse a procesos de aniquilación triplete-triplete, lo que resulta en la formación de estados singlete superiores que emiten a energías más altas.
En la espectroscopia Raman , cuando una molécula se excita por la radiación incidente, sufre un desplazamiento de Stokes, ya que emite radiación a un nivel de energía inferior al de la radiación incidente. El análisis de la intensidad y la frecuencia del desplazamiento espectral proporciona información valiosa sobre los modos vibracionales de las moléculas, lo que permite la identificación de enlaces químicos, grupos funcionales y conformaciones moleculares.
El oxisulfuro de itrio ( Y2O2S ) dopado con oxisulfuro de gadolinio (Gd2O2S ) es un pigmento anti-Stokes industrial común , que absorbe en el infrarrojo cercano y emite en la región visible del espectro. [10] Este material compuesto se utiliza a menudo en aplicaciones luminiscentes, donde absorbe fotones de menor energía y emite fotones de mayor energía. Esta propiedad única lo hace particularmente valioso en varios campos tecnológicos, incluida la impresión de seguridad, las medidas contra la falsificación y las pantallas luminiscentes. Al aprovechar la fluorescencia anti-Stokes, este pigmento permite la creación de tintas, recubrimientos y materiales vibrantes y duraderos con capacidades mejoradas de visibilidad y autenticación.
La conversión ascendente de fotones es un proceso anti-Stokes en el que los fotones de menor energía se convierten en fotones de mayor energía. Un ejemplo de este último proceso se demuestra mediante la conversión ascendente de nanopartículas . Se observa más comúnmente en la espectroscopia Raman , donde se puede utilizar para determinar la temperatura de un material. [11]
En las capas semiconductoras de película delgada con banda prohibida directa, la emisión desplazada de Stokes puede tener su origen en tres fuentes principales: dopaje, deformación y desorden. [12] Cada uno de estos factores puede introducir variaciones en los niveles de energía del material semiconductor, lo que lleva a un desplazamiento de la luz emitida hacia longitudes de onda más largas en comparación con la luz incidente. Este fenómeno es particularmente relevante en los dispositivos optoelectrónicos, donde el control de estos factores puede ser crucial para optimizar el rendimiento del dispositivo.