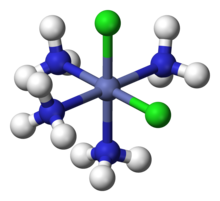
En química de coordinación , la primera esfera de coordinación se refiere al conjunto de moléculas e iones (los ligandos ) directamente unidos al átomo metálico central . La segunda esfera de coordinación consta de moléculas e iones que se unen de diversas formas a la primera esfera de coordinación.
La primera esfera de coordinación se refiere a las moléculas que están unidas directamente al metal. Las interacciones entre la primera y la segunda esfera de coordinación suelen implicar enlaces de hidrógeno. Para los complejos cargados, el apareamiento iónico es importante.
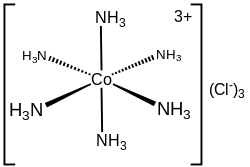
En el cloruro de hexaminocobalto (III) ([Co(NH 3 ) 6 ]Cl 3 ), el catión cobalto más los 6 ligandos de amoníaco comprenden la primera esfera de coordinación. La esfera de coordinación de este ion consta, por tanto, de un núcleo central MN 6 "decorado" por 18 enlaces N-H que irradian hacia el exterior.

Se puede describir que los iones metálicos consisten en series de dos esferas de coordinación concéntricas, la primera y la segunda. Más alejadas de la segunda esfera de coordinación, las moléculas de disolvente se comportan más como " disolvente en masa ". La simulación de la segunda esfera de coordinación es de interés en química computacional . La segunda esfera de coordinación puede consistir en iones (especialmente en complejos cargados), moléculas (especialmente aquellas que forman enlaces de hidrógeno con ligandos en la primera esfera de coordinación) y porciones de la estructura principal de un ligando. En comparación con la primera esfera de coordinación, la segunda esfera de coordinación tiene una influencia menos directa sobre la reactividad y las propiedades químicas del complejo metálico. No obstante, la segunda esfera de coordinación es relevante para comprender las reacciones del complejo metálico, incluidos los mecanismos de intercambio de ligandos y catálisis.
Los mecanismos de las metaloproteínas a menudo invocan la modulación de la segunda esfera de coordinación por parte de la proteína. [1]

Las velocidades a las que los ligandos se intercambian entre la primera y la segunda esfera de coordinación son el primer paso en las reacciones de sustitución de ligandos. En la sustitución asociativa de ligando , el nucleófilo entrante reside en la segunda esfera de coordinación. Estos efectos son relevantes para aplicaciones prácticas como los agentes de contraste utilizados en la resonancia magnética . [4]
La energía de las reacciones de transferencia de electrones de la esfera interna se analiza en términos de la segunda esfera de coordinación. Algunas reacciones de transferencia de electrones acoplados a protones implican la transferencia de átomos entre las segundas esferas de coordinación de los reactivos:
Los efectos de los disolventes sobre los colores y la estabilidad suelen ser atribuibles a cambios en la segunda esfera de coordinación. Estos efectos pueden ser pronunciados en complejos donde los ligandos en la primera esfera de coordinación son fuertes donantes y aceptores de enlaces de hidrógeno, por ejemplo, respectivamente [Co(NH 3 ) 6 ] 3+ y [Fe(CN) 6 ] 3− . Los éteres de corona se unen a complejos de poliaminas a través de su segunda esfera de coordinación. Los cationes de poliamonio se unen a los centros de nitrógeno de los cianometalatos. [5]
Las moléculas macrocíclicas, como las ciclodextrinas, actúan a menudo como segunda esfera de coordinación de los complejos metálicos. [6] [7]