
Los complejos de metales de transición de aldehídos y cetonas describen complejos de coordinación con ligandos de aldehído (RCHO) y cetona (R 2 CO) . Como los aldehídos y las cetonas son comunes, el área es de fundamental interés. Algunas reacciones que son útiles en química orgánica involucran este tipo de complejos.
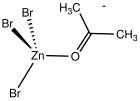
En los complejos monometálicos, los aldehídos y las cetonas pueden unirse a metales en cualquiera de dos modos: η 1 -O-enlazado y η 2 -C,O-enlazado. Estos modos de enlace a veces se denominan enlaces sigma y pi. Estas formas a veces pueden interconvertirse.
El modo de enlace sigma es más común para centros metálicos ácidos de Lewis de valencia superior (p. ej., Zn 2+ ). [1] El modo de enlace pi se observa en centros metálicos ricos en electrones y de baja valencia (p. ej., Fe(0) y Os(0)). [2]
A los efectos del recuento de electrones, los ligandos con enlaces O cuentan como "ligandos L" de 2 electrones : son bases de Lewis. Los ligandos η2 - C ,O se describen como análogos de los ligandos de alqueno , es decir, el modelo de Dewar-Chatt-Duncanson . [3]
Las cetonas y aldehídos η 2 -C,O pueden funcionar como ligandos puente, utilizando un par de electrones libres en el oxígeno. Uno de esos complejos es [(C 5 H 5 ) 2 Zr (CH 2 O)] 3 , que presenta un anillo Zr 3 O 3 . [4]
Relacionados con los complejos de aldehídos y cetonas con enlaces η 1 -O están los acetilacetonatos metálicos y especies relacionadas, que pueden verse como una combinación de ligandos de cetona y enolato .

Algunos complejos de η 2 -aldehído insertan alquenos para dar metalaciclos de cinco miembros . [5]
Los complejos η 1 de carbonilos alfa-beta insaturados exhiben una reactividad mejorada hacia los dienos . Esta interacción es la base de las reacciones de Diels-Alder catalizadas por ácido de Lewis .